第三章索引
第三章 血液
血液是一种流体组织,充满于心血管系统中,在心脏的推动下不断循环流动。如果流经体内任何器官的血流量不足,均可能造成严重的组织损伤;人体大量失血或血液循环严重障碍,将危及生命。血液在医学诊断上有重要价值,因为很多疾病可导致血液组成成分或性质发生特征性的变化。
血液与内环境的演化血液是在动物进化过程中出现的。生命最初出现在海洋中。当在远古的海洋中出现比较复杂的多细胞生物时,机体的部分细胞已不可能与浸浴着整个机体的海洋环境直接接触;这时,机体内开始出现了细胞外液,它一方面作为细胞直接生活的内环境,同时又是机体与外环境进行物质交换的媒介。可以认为在进化中,最初的细胞外液可能是由包绕在机体内部的那部分海水形成的,因而它主要是一种盐溶液,其基本成分可能与远古的海水十分相似。以后,机体内出现了循环系统,细胞外液也进一步分化成为血管内的血浆和血管外的组织间隙液(简称组织液)。组织液仍然主要是盐溶液,是直接浸浴着绝大部分机体细胞的液体环境;而血管内的液体,则又溶入了多种蛋白质,并逐步出现了各种血细胞,于是形成了血液。
人体内除细胞外液外,尚有更多的液体(约为前者的2倍)存在于细胞内部,称为细胞内液。细胞外液和细胞内液总称为体液,约占机体总重量的60%。一般来说,细胞内液是细胞内各种生物化学反应得以进行的场所,细胞外液则是细胞直接生活的液体环境。因此,如果大气是整个人体的外环境,细胞外液就是第一个细胞生活的具体环境,故称为内环境。在细胞外液中,4/5在血管外构成组织液,1/5在血管内成为血浆的组成部分;而后者由于能在血管中不断循环流动,是内环境中最为活跃的部分,成为沟通各部分组织液以及和外环境进行物质交换的中间环节。
血液与内环境稳态在一些疾病情况下,常可出现内环境理化性质的较大变化,如高热、酸中毒、缺氧等,均将引起机体细胞功能的严重紊乱。在灌流离体器官的动物实验中,所用灌流液的化学成分、含氧量、Ph、温度与渗透压等,必须与这些动物的血浆十分相近(表3-1),离体器官才能在一段时间内保持接近于正常功能的活动状态。这些都说明,内环境理化性质的相对稳定,对于维持整个人体和体内所有细胞的正常功能都是非常必要的。这就是为什么早在19世纪时,Claude Bernard就指出:内环境的稳定是“机体自由独立生活的必要条件”。
然而在机体生活期间,干扰内环境理化性质的因素是不断出现的。机体细胞与细胞外液的物质交换,经常改变着内环境的理化性质;一些外环境因素的急剧变化也倾向于直接或间接(通过机体活动变化)改变内环境的理化性质。但与此同时,消化道不断补充营养物质,肺不断补充氧和排出二氧化碳,肾不断排出各种代谢尾产物、调整水与各种无机盐及小分子物质的排泄量,皮肤也不断散失代谢所产生的热量;而且,这些活动都处于整体的神经和体液调节之下,从而使内环境的理化性质只能作较小幅度的波动,保持着动态平衡。这一状态称为稳态(homeostasis)。
表3-1 血浆与生理盐溶液成分对照
|
任(Ringer)氏液(用于蛙心灌流)(g) |
蛙血浆(g) |
乐(Locke)氏液(用于哺乳动物)(g) |
哺乳动物血浆(g) |
| NaCI |
0.65 |
0.55 |
0.9 |
0.7 |
| KCI |
0.014 |
0.023 |
0.042 |
0.038 |
| CaCI2 |
0.012 |
0.025 |
0.024 |
0.028 |
| NaHCO3 |
0.02 |
0.1 |
0.02 |
0.23 |
| NaH2PO4 |
0.001 |
0.002 |
- |
0.036 |
| 葡萄糖 |
- |
0.04 |
0.1-0.25 |
0.07 |
| 水 |
到100ml |
100ml |
到100ml |
100ml |
血液对内环境某些理化性质的变化有一定的“缓冲”作用。例如血液中含有多种缓冲物质,可以减轻酸性代谢产物引起的pH变化;血液中的水比热较大,可以吸收大量的热量而使温度升高不多。这类缓冲作用虽然有限,但在血液运输各种物质的过程中可防止其理化性质发生太大的变化。
血量 人体内血液的总量称为血量,是血浆量和血细胞量的总和;但是,除红细胞外,其它血细胞数量很少,常可忽略不计。血浆量和红细胞量均可按稀释原理分别测定。例如可由静脉注射一定量不易透出血管的大分子染料(通常用T1824)或131I标记的血浆蛋白,待与体内血浆混匀后,再抽血测定T1824或131I被稀释的倍数,即可计算出血浆量。同样,可由静脉注射一定量用51Cr或32P标记的红细胞,待与体内的红细胞混匀后,抽血以测定标记的红细胞稀释的倍数,即可计算出红细胞总量。但由于标记的血浆白蛋白可逸出血管,因而从血流中“消失”较快,会影响测定结果,因此一般可先测出红细胞总量后,再按红细胞在血液中所占容积的百分比来推算血液总量。正常成年人的血液总量约相当于体重的7%~8%,或相当于每公斤体重70~80ml,其中血浆量为40~50ml。幼儿体内的含水量较多,血液总量占体重的90%。
第一节 血液的组成与特性
一、血液的组成
人类的血液由血浆和血细胞组成。1L血浆中含有900~910g水(90%~91%)。65~85g蛋白质(6.5%~8.5%)和20g低分子物质(2%).低分子物质中有多种电解质和小分子有机化合物,如代谢产物和其他某些激素等。血浆中电解质含量与组织液基本相同(表3-2)。由于这些溶质和水分都很容易透过毛细血管与组织液交流,这一部分液体的理化性质的变化常与组织液平行。在血液不断循环流动的情况下。血液中各种电解质的浓度,基本上代表了组织液中这些物质的浓度。
血浆蛋白的浓度是血浆和组织液的主要区别所在(表3-2),因为血浆蛋白的分子很大,不能透过毛细血管管壁。在生物化学研究中,曾经用盐析法将血浆蛋白分为白蛋白、球蛋白与纤维蛋白原三大类。以后,用电泳法又将白蛋白区分为白蛋白和前白蛋白,将球蛋白区分为a1-、a2-、a3-、β-、γ-球蛋白等。用其他方法,如免疫电泳,还可以将血浆蛋白作更进一步的区分。这说明血浆蛋白包括了很多分子大小和结构都不相同的蛋白质。
表3-2 人体各部分体液中电解质含量
|
血浆 |
组织液 |
细胞内液 |
| MEq/L(血浆) |
MEq/L(水) |
MEq/L(水) |
MEq/L(水) |
| 正离子 |
Na+ |
142.0 |
153.0 |
140.7 |
10 |
| K+ |
5.0 |
5.4 |
4.0 |
140 |
| Ca2+ |
5.0 |
5.4 |
2.5 |
5 |
| Mg2+ |
3.0 |
3.2 |
2.0 |
27 |
| 总计 |
155.0 |
167.0 |
155.5 |
182 |
| 负离子 |
HCO3- |
27.0 |
29.0 |
30.0 |
10 |
| CI- |
103.0 |
111.0 |
114.0 |
25 |
| HPO42- |
2.0 |
2.2 |
2.0 |
80 |
| SO42- |
1.0 |
1.1 |
1.0 |
20 |
| 有机酸 |
6.0 |
6.5 |
7.5 |
? |
| 蛋白质 |
16.0 |
17.2 |
1.0 |
47 |
| 总计 |
155.0 |
167.0 |
155.5 |
182 |
引自Koushanpour,E.1976(血浆依含水93%计算)
各种血浆蛋白具有不同的生理机能,主要有以下六下方面:
1、营养功能 每个成人3L左右的血浆中约含有200g蛋白质,它们起着营养贮备的功能。虽然消化道一般不吸收蛋白质,吸收的是氨基酸,但是,体内的某些细胞,特别是单核吞噬细胞系统,吞饮完整的血浆蛋白,然后由细胞内的酶类将吞入细胞的蛋白质分解为氨基酸。这样生成的氨基酸扩散进入血液,随时可供其它细胞合成新的蛋白质之用。
2、运输功能蛋白质巨大的表面上分布有众多的亲脂性结合位点,它们可以与脂容性物质结合,使之成为水溶性,便于运输;血浆蛋白还可以与血液中分子较小的物质(如激素、各种正离子)可逆性的结合,即可防止它们从肾流失,又由于结合状态与游离状态的物质处于动态平衡之中,可使处于游离状态的这些物质在血中的浓度保持相对稳定。
3、缓冲功能血浆白蛋白和它的钠盐组成缓冲对,和其它无机盐缓冲对(主要是碳酸和碳酸氢钠)一起,缓冲血浆中可能发生的酸碱变化,保持血液pH的稳定。
4、形成胶体渗透压,调节血管内外的水份分布(详见血液的理化特性一节)。
5、参与机体的免疫功能在实现免疫功能中有重要作用的免疫抗体、补体系统等,都是由血浆球蛋白构成的。
6、参与凝血和抗凝血功能绝大多数的血浆凝血因子、生理性抗凝物质以及促进血纤维溶解的物质都是血浆蛋白(参见本章第三节)。
二、血液的理化特性
(一)血液的比重
血液的比重为1.050~1.060,血浆的比重约为1.025~1.030。血液中红细胞数愈多则血液比重愈大,血浆中蛋白质含量愈多则血浆比重愈大。血液比重大于血浆,说明红细胞比重大于血浆。
红细胞的悬浮稳定性将与抗凝剂混匀的血液静置于一支玻璃管(如分血计)中,红细胞由于比重较大,将因重力而下沉,但正常时下沉十分缓慢。通常以红细胞在一小时内下沉的距离来表示红细胞沉降的速度,称为红细胞沉降率。正常男性的红细胞沉降率第一小时不超过3mm,女性不超过10mm。红细胞下降缓慢,说明它有一定的悬浮稳定性;红细胞沉降率愈小,表示悬浮稳定性愈大。
红细胞因比重较大而在血浆中下沉时,红细胞与血浆之间的磨擦则阻碍其下沉,特别是双凹碟形的红细胞,表面积与容积之比较大,因而所产生的磨擦也较大。红细胞沉降率在某些疾病时(如活动性肺结核、风湿热等)加快,这主要是由于许多红细胞能较快地互相以凹面相贴,形成一叠红细胞,称为叠连;红细胞叠连起来,其外表面积与容积之比减小,因而磨擦力减小,下沉加快。叠连形成的快慢主要决定于血浆的性质,而不在于红细胞自身。若将血沉快的病人的红细胞,置于正常人的血浆中,则形成叠连的程度和红细胞沉降的速度并不加大;反过来,若将正常人的红细胞置于这些病人的血浆中,则红细胞会迅速叠连而沉降。这清楚地说明促使红细胞发生叠连的因素在于血浆中。一般血浆中白蛋白增多可使红细胞沉降减慢;而球蛋白与纤维蛋白原增多时,红细胞沉降加速。其原因可能就在于白蛋白可使红细胞叠连(或聚集成其他形式有团粒)减少,而球蛋白与纤维蛋白原则可促使叠连(或其他形式的聚集)增多,但其详细作用机制尚不清楚。
(二)血液的粘滞性
通常是在体外测定血液或血浆与水相比的相对粘滞性,这时血液的相对粘滞性为4-5,血浆为1.6-2.4。全血的粘滞性主要决定于所含的红细胞数,血浆的粘滞性主要决定于血浆蛋白质的含量。水、酒精等在物理学上所谓“理想液体”的粘滞性是不随流速改变的,而血液在血流速度很快时类似理想液体(如在动脉内),其粘滞性不随流速而变化;但当血流速度小于一定限度时,则粘滞性与流速成反变的的关系。这主要是由于血流缓慢时,红细胞可叠连或聚集成其他形式的团粒,使血液的粘滞性增大。在人体内因某种疾病使微环境血流速度显着减慢时,红细胞在其中叠连和聚集,对血流造成很大的阻力,影响循环的正常进行;这时可以通过输入血浆白蛋白或低分子右旋糖酐以增加血流冲刷力量,使红细胞分散。
(三)血浆渗透压
血浆渗透压约为313mOsm/kgH2O,相当于7个大气压708.9kPa(5330mmHg)。血浆的渗透压主要来自溶解于其中的晶体物质,特别是电解质,称为晶体渗透压。由于血浆与组织液中晶体物质的浓度几乎相等,所以它们的晶体渗透压也基本相等。血浆中虽含有多量蛋白质,但蛋白质分子量大,所产生的渗透压甚小,不超过1.5mOsm/kgH2O,约相当于3.3kPa(25mmHg),称为胶体渗透压.由于组织液中蛋白质很少,所以血浆的胶体渗透压高于组织液.在血浆蛋白中,白蛋白的分子量远小于球蛋白,故血浆胶体渗透压主要来自白蛋白。若白蛋白明显减少,即使球蛋白增加而保持血浆蛋白总含量基本不变,血浆胶体渗透压也将明显降低。
血浆蛋白一般不能透过毛细血管壁,所以血浆胶体渗透压虽小,但对于血管内外的水平衡有重要作用(参见第四章第三节)。由于血浆和组织液的晶体物质中绝大部分不易透过细胞膜,所以细胞外液的晶体渗透压的相对稳定,对于保持细胞内外的水平衡极为重要。
等渗溶液与等张溶液在临床或生理实验使用的各种溶液中,其渗透压与血浆渗透压相等的称为等渗溶液(如0.85%NaCI溶液),高于或低于血浆渗透压的则相应地称为高渗或低渗溶液。将正常红细胞悬浮于不同浓度的NaCI溶液中即可看到:在等渗溶液中的红细胞保持正常大小和双凹圆碟形;在渗透压递减的一系列溶液中,红细胞逐步胀大并双侧凸起,当体积增加30%时成为球形;体积增加45%~60%则细胞膜损伤而发生溶血,这时血红蛋白逸出细胞外,仅留下一个双凹圆碟形细胞膜空壳,称为影细胞(ghost cell)。正常人的红细胞一般在0.42%NaCI溶液中时开始出现溶血,在0.35%NaCI溶液中时完全溶血.在某些溶血性疾病中,病人的红细胞开始溶血及完全溶血的NaCI溶液浓度均比正常人高,即红细胞的渗透抵抗性减小了,渗透脆性增加了。不同物质的等渗溶液不一定都能使红细胞的体积和形态保持正常;能使悬浮于其中的红细胞保持正常体积和形状的盐溶液,称为等张溶液.所谓“张力”实际是指溶液中不能透过细胞膜的颗粒所造成的渗透压。例如NaCI不能自由透过细胞膜,所以0.85%NaCI既是等渗溶液,也是等张溶液;但如尿素,因为它是能自由通过细胞膜的,1.9%尿素溶液虽然与血浆等渗,但红细胞置入其中后立即溶血。所以不是等张溶液。
(四)血浆的pH值
正常人的血浆的pH值约为7.35-7.45。血浆pH值主要决定于血浆中主要的缓冲对,即NaHCO3/H2CO3的比值。通常NaHCO3/H2CO3比值为20。血浆中NaHCO3/H2CO3外,尚有其他缓冲对。在血浆中有蛋白质钠盐/蛋白质、Na2HPO4/NaH2PO4,在红细胞内尚有血红蛋白钾盐/血红蛋白、氧合血红蛋白钾盐/氧合血红蛋白、Na2HPO4/NaH2PO4、KH2PO4、KHCO3/H2CO3等缓冲对,都是很有效的缓冲对系统。一般酸性或碱性物质进入血液时,由于有这些缓冲系统的作用,对血浆pH值的影响已减至很小,特别是在肺和肾不断的排出体内过多的酸或碱的情况下,通常血浆pH值的波动范围极小。
第二节 血细胞及其功能
血细胞包括红细胞、白细胞和血小板三类细胞,它们均起源于造血干细胞。在个体发育过程中,造血器官有一个变迁的程序。在胚胎发育的早期,是在卵黄囊造血,从胚胎第二个月开始,由肝、脾造血;胚胎发育到第五个月以后,肝、脾的造血活动逐渐减少,骨髓开始造血并逐渐增强;到婴儿出生时,几乎完全依靠骨髓造血,但在造血需要增加时,肝、脾可再参与造血以补充骨髓功能的不足。因此,此时的骨髓外造血具有代偿作用。儿童到4岁以后,骨髓腔的增长速度已超过了造血组织增长的速度,脂肪细胞逐步填充多余的骨髓腔。到18岁左右,只有脊椎骨、肋骨、胸骨、颅骨和长骨近端骨骺处才有造血骨髓,但造血组织的总量已很充裕。成年人如果出现骨髓外造血,已无代偿的意义,而是造血功能紊乱的表现。
造血过程,也就是各类血细胞的发育、成熟的过程,是一个连续而又区分为阶段的过程。首先是造血干细胞(hemopietic stem cells)阶段,处于这一阶段的造血细胞为干细胞,它们既能通过自我复制(self renewal)以保持本身数量的稳定,又能分化形成各系定向祖细胞(committedprogenitors);第二个阶段是定向祖细胞阶段,处于这个阶段的造血细胞,进一步分化方向已经限定,它们可以区分为:红系祖细胞,即红系集落形成细胞(CFU-E),粒-单核系祖细胞(CFU-GM),巨核系祖细胞( CFU-MK)和 TB淋巴系祖细胞(CFU-TB);第三个阶段是形态可辩认的前体细胞(precursors)阶段,此时的造血细胞已经发育成为形态上可以辨认的各系幼稚细胞,这些细胞进一步分别成熟为具有特殊细胞功能的各类终末血细胞,然后释放进入血液循环。造血细胞在经历上述发育成熟过程中,细胞自我复制的能力逐渐降低,而分化、增殖的能力逐渐增强,细胞数量逐步增大(图3-1)
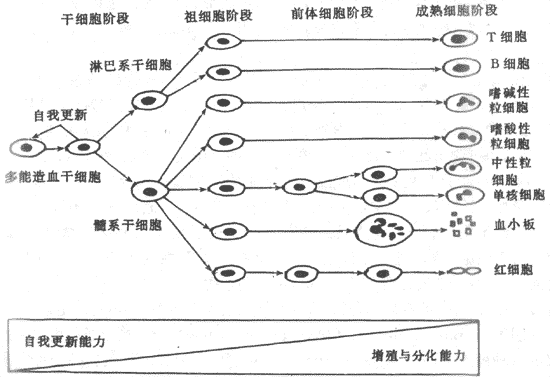
图3-1造血细胞发育模式图
一、红细胞生理
1.红细胞的数量、形态和功能 红细胞(erythuocyte)是血液中数量最多的一种血细胞,正常男性每微升血液中平均约500万个(5.0×1012/L),女性较少,平均约420万个(4.2×1012/L).红细胞含有血红蛋白,因而使血液呈红色.红细胞在血液的气体运输中有极重要的作用.在血液中由红细胞运输的氧约为溶解于血浆的70倍;在红细胞参与下,血浆运输二氧化碳的能力约为直接溶解于血浆的18倍(详见第五章第三节).正常红细胞呈双凹圆碟形,平均直径约8μm,周边稍厚.这种细胞开头的表面积与体积之比,较球形时为大,因而气体可通过的面积也较大;由细胞中心到大部分表面的距离较短,因此气体进出红细胞的扩散距离也较短.这种形状也有利于红细胞的可塑性变形.红细胞在全身血管中循环运行,常要挤过口径比它小的毛细血管和血窦间隙,这时红细胞将发生卷曲变形,在通过后又恢复原状,这种变形称为塑性变形.表面积与体积的比值愈大,变形能力愈大,故双凹圆碟形红细胞的变形能力远大于异常情况下可能出现的球形红细胞.红细胞保持双凹圆碟形需要消耗能量。
红细胞膜是以脂质双分子层为骨架的半透膜。氧和二氧化碳等脂溶性气体可以自由通过,尿素也可以自由透入。在电解质中,负离子(如CI-、HCO3-)一般较易通过红细胞膜,而正离子却很难通过。红细胞内Na+ 浓度远低于细胞外,而细胞内K+浓度远高于细胞外,这种细胞内外的Na+、K+浓度差主要是依靠细胞膜上Na+泵的活动来维持的。低温贮存较久的血液,血浆内K+浓度升高,就是由于低温下代谢几乎停止,Na+泵不能活动的缘故。
红细胞结合和携带氧的过程并不消耗能量,血红蛋白中的Fe2+也不被氧化,若Fe2+被氧化成Fe3+成为高铁血红蛋白,即失去携氧能力。红细胞消耗葡萄糖,主要是通过糖酵解和磷酸戊糖旁路,所产生的能量(以结合于ATP的形式)主要是用于供应细胞膜上Na+泵的活动,用于保持低铁血红蛋白不致被氧化,也用于保持红细胞膜的完整性和细胞的双凹圆碟形。
2.红细胞比容 红细胞在血液中所占的容积百分比,称为红细胞比容(hematocritvalue),可以用分血计(hematocrit)来测定。通常是将一定量的血液与抗凝剂混匀,置于用直径2.5mm的平底玻璃管制成的分血计中,以每分钟3000转的速度离心半小时,使血细胞下沉压紧,即可测出红细胞比容。正常成年人的红细胞比容,男性为40%-50%,女性为37%-48%。但这是从手臂等处浅静脉抽血测定的数值,并且这时在压紧的红细胞之间有很少量血浆;同时,全身各类血管中,血液的红细胞比容值也不尽相同。
3.正常红细胞生成所必需的原料和其它因素 在幼红细胞的发育成熟过程中,细胞核的存在对于细胞分裂和合成血红蛋白有着重要的作用。在这些阶段,合成细胞核的主要构成物质—DNA必须有维生素B12和叶酸作为辅酶。
维生素B12是含钴的有机化合物,多存在于动物性食品中。机体对维生素B12的吸收必须要有内因子(intrinsic factor)和R结合蛋白(Rprotein)参与。内因子是由胃腺的壁细胞所分泌的一种糖蛋白,分子量在50000-60000之间,而R(rapid)蛋白是一种电泳速度很快的血浆蛋白。在酸性的胃液中,维生素B12主要与R蛋白结合,到了小肠上段处胰蛋白酶将这种结合断裂,维生素B12转而与内因子结合。内因子有两个活性部位,一个部位可与维生素B12结合,另一个部位则可与回肠上皮细胞膜上的特异受体结合。在正常情况下,内因子-B12复合物在小肠上段可保护维生素B12不受小肠内蛋白水解酶的破坏。当复合物运行至回肠段,便与回肠粘膜受体结合而被吸收进入门脉系统血流,一部分贮存在肝,一部分又与运输维生素B12的转钴蛋白Ⅱ(transcobalamineⅡ)结合,沿血液输送到造血组织,参与红细胞生成过程。当胃的大部分被切除或胃腺细胞受损伤,机体缺乏内因子,或体内产生抗内因子的抗体时,即可发生维生素B12吸收障碍,影响幼红细胞的分裂和血红蛋白合成,出现巨幼红细胞性贫血,即大细胞性贫血。
叶酸是以蝶酰单谷氨酸的形式吸收的。吸收之后,在双氢叶酸还原酶的催化下,形成四氢叶酸。存在于血浆中的叶酸几乎全是四氢叶酸的单谷氨酸盐。但进入组织细胞后,又通过酶促作用,再转变为多谷氨酸盐,才具有活性。叶酸缺乏时也引起与维生素B12缺乏时相似的巨幼红细胞性贫血。只是在维生素B12缺乏时,还可伴有神经系统和消化道症状。
合成血红蛋白还必须有铁作为原料,每亳升红细胞需要1mg铁,每天需要20-25mg铁用于红细胞生成,但人每天只需从食物中吸收1mg(约5%)以补充排泄的铁,其余95%均来自人体铁的再利用。机体贮存的铁主要来自于破坏了的红细胞。衰老的红细胞被巨噬细胞吞噬后,血红蛋白被消化而释出血红素中的Fe2+。这样释出的铁即与铁蛋白(ferritin)结合,此时的铁为Fe3+,聚集成铁黄素颗粒而沉淀于巨噬细胞内。血浆中有一种运铁蛋白(transferrin),可以来往运行于巨噬细胞与幼红细胞之间,以运送铁。贮存于铁蛋白中的Fe3+,先还原成Fe2+再脱离铁蛋白,而后与运铁蛋白结合。每分子运铁蛋白可以运送两个Fe2+,运送到幼红细胞后,又可反复作第二次运输。此外,还可以通过巨噬细胞与红母细胞直接接触,以提供合成血红蛋白所需的铁。由于慢性出血等原因,体内贮存的铁减少,或造血功能增强而供铁不够,均可引起小细胞性贫血,这主要是合成血红蛋白不足。此外,红细胞生成还需要氨基酸和蛋白质、维生素B6、B2、C、E,微量元素铜、锰、钴和锌等。
4.红细胞生成的调节 每个成年人体内约有25×1012个红细胞,每24小时便有0.8%的红细胞进行更新,也就是说每分钟约有160×106个红细胞生成;当机体有需要时,如失血或某些疾病使红细胞寿命缩短时,红细胞的生成率还能在正常基础上增加数倍。目前已经证明有两种调节因子分别调制着两个不同发育阶段红系祖细胞的生长。一种是早期的红系祖细胞,称为爆式红系集落形成单位(burst forming unit-erythroid,BFU-E),这是因为它们在体外培养中能形成很大的细胞集落,组成集落的细胞散布成物体爆炸的形状,这种早期祖细胞的生长和在体外形成集落都依赖于一种称为爆式促进因子(burst promoting activitor,BPA)的刺激作用。BPA是一类分子量为25000-40000的糖蛋白,以早期红系祖细胞BFU-E为作用的靶细胞,可能是促进更多的BFU-E从细胞周期中的静息状态(G0期)进入DNA合成期(S期),因而使早期祖细胞加强增殖活动。另一种是晚期的红系祖细胞,称为红系集落形成单位(colony forming unit-erythroid,CFU-E),它们在体外培养中只能形成较小的集落。晚期红系祖细胞对BPA不敏感,但主要接受促红细胞生成素(erythropoietin,EPO)的调节。促红细胞生成素是一种热稳定(80℃)的糖蛋白,分子量为34000。当组织中氧分压降低时,血浆中的促红细胞生成素的浓度增加,它促进红系祖细胞向前体细胞分化,又加速这些细胞的增殖,结果使骨髓中能合成血红蛋白的幼红细胞数增加,网织红细胞加速从骨髓释放。早在本世纪50年代,动物实验已显示了促红细胞生成素活性的存在,以后又确定促红细胞生成素主要由肾组织产生。切除双肾后,血浆中促红细胞生成素的浓度急剧降低。用分子生物学手段进一步证明,从肾组织细胞中已提取出编码促红细胞生成素的Mrna 和Cdna,还确定促红细胞生成素和mRNA和cDNA,还确定促红细胞生成素基因定位在7号染色体上。近年来有迹象提示人类的某些血液病,如再生障碍性贫血是红系祖细胞促红细胞生成素受体有缺陷所致(图3-2)。
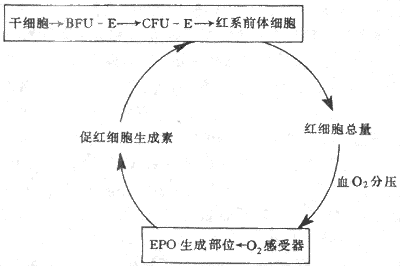
图3-2 EPOA调节红细胞生成的反馈调节环
促红细胞生成素主要由肾组织产生,但肾外,如肝脏,也有小量生成。晚期肾病患者,肾脏产生EPO已基本停止,但体内仍有小量EPO促使骨髓继续产生红细胞。
其他一些激素,包括雄激素、甲状腺激素和生长激素,都可增强促红细胞生成素的作用;雌激素则有抑制红细胞生成的作用。这可能是男性的红细胞数和血红蛋白量高于女性的原因。
二、白细胞生理
白细胞(leukocyte)是一类有核的血细胞。正常成年人白细胞总数是4000-10000/μ1,每日不同的时间和机体不同的功能状态下,白细胞在血液中的数目是有较大范围变化的。当每微升超过10000个白细胞时,称为白细胞增多,而每微升少于4000个白细胞时,称为白细胞减少。机体有炎症时常出现白细胞增多。
白细胞不是一个均一的细胞群,根据其形态、功能和来源部位可以分为三大类:粒细胞、单核细胞和淋巴细胞(表3-3)。白细胞与红细胞和血小板一样都起源于骨髓中的造血干细胞,在细胞发育过程中又都是经历定向祖细胞、前体细胞,而后成为具有各种细胞功能的成熟白细胞。
表3-3 血液中各类白细胞计数(细胞/μL)
|
均数 |
% |
范围 |
| 粒细胞 |
|
|
|
| 中性粒细胞 |
4150 |
(59) |
1712~7588 |
| 嗜酸性粒细胞 |
165 |
(2) |
0~397 |
| 嗜碱性粒细胞 |
44 |
(<1) |
0~112 |
| 单核细胞 |
456 |
(7) |
66~846 |
| 淋巴细胞 |
2185 |
(31) |
1029~3341 |
| 白细胞 |
7000 |
|
2800~11200 |
引自Schmidt,R.F.&Thews,G,1989
白细胞的分化和增殖受到一组造血76生长因子(hematopoietic growth factor,HGF)的调节。这些因子从淋巴细胞、单核细胞和成纤维细胞生成并分泌,是一类糖蛋白。由于有些造血生长因子在体外可刺激造血细胞生成集落,故又称为集落刺激因子(clony stimulating factor, CSF)。目前从结构到功能已经充分阐明的集落刺激因子有M-CSF、G-CSF、GM-CSF、Multi-CSF、Meg-CSFt 和EPO等6种,除了EPO是调节红细胞生成因子之外,其余因子均参与调节白细胞的生成。这些因子中有的作用是广谱的,如Multi-CSF和GM-CSF(G是粒细胞缩写,M是单核细胞的缩写)的作用可以影响多系造血祖细胞的生成和发育,而其它一些因子(如G-CSF、M-CSF、GM-CSF)作用较为局限,只作用于某一系的造血祖细胞。所有这些因子除了作用于祖细胞,还能影响成熟白细胞的功能。此外,还有一类抑制性因子,如粒细胞抑素、乳铁蛋白和转化生成因子-β等,它们或是直接抑制白细胞的增殖、生长、或是限制上述的一些生长因子的释放或作用。
淋巴细胞的生成过程与其它白细胞有一些不同。在干细胞分化的早期,淋巴干细胞首先从多能干细胞分化出来。这些淋巴干细胞随血流进入初级(或中枢)淋巴器官,即骨髓和胸腺,在这里它们发育成定向淋巴细胞(commmittde lymphocyte)。在骨髓中发育的称为B细胞;在胸腺中发育的称为T细胞。随后,B和T细胞均随血流转移到二级(或外周)淋巴器官,即淋巴结和脾,在那里它们与某种抗原接触后即分化和增殖成为真正具有免疫功能的细胞,如浆细胞和T效应细胞(t effector cell)。淋巴细胞在生长成熟过程中接受一组称为白细胞介素(interleukins,ILs)的细胞因子的调节,T细胞在胸腺中还接受胸腺激素的作用(图3-3)。
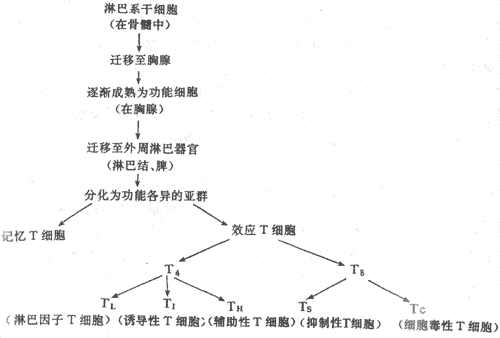
图3-3 T细胞的成熟和分化
所有的白细胞都能作变形运动,凭藉这种运动白细胞得以穿过血管壁,这一过程称作血细胞渗出(diapedisis)。白细胞具有趋向某些化学物质游走的特性,称为趋化性。体内具有趋化作用的物质包括:细菌毒素、细菌或人体细胞的降解产物,以及抗原-性体复合物等。白细胞按照这些物质的浓度梯度游走到这些物质的周围,把异物包围起来并吞入胞浆内,这称为吞噬作用。每类白细胞都具有某些酶类,如蛋白酶、多肽酶、淀粉酶、脂酶和脱氧核糖核酸酶等。在白细胞总数中,有一半以上存在于血管外的细胞间隙内,有30%以上贮存在骨髓内,其余的才是在血管中流动的。这些白细胞凭藉血液的运输,从它们生成的器官,即骨髓和淋巴组织,到达发挥作用的部位。
(一)粒细胞
约有60%的白细胞的胞质内具有颗粒,因而把它们称为粒细胞。又根据胞质中颗粒的染色性质不同将粒细胞区分为:中性、嗜酸性和嗜碱性粒细胞,这三类细胞的比例见表3-3。粒细胞在血流中停留时间很短暂,一般从数小时至2天。
1.中性粒细胞绝大部分的粒细胞属中性粒细胞。每微升血液中约有4500个中性粒细胞。由于这些细胞的细胞核的形态特殊,又称为多形核白细胞。中性粒细胞在血管内停留的时间平均只有6-8小时,它们很快穿过血管壁进入组织发挥作用,而且进入组织后不再返回血液中来。在血管中的中性粒细胞,约有一半随血流循环,通常作白细胞计数只反映了这部分中性粒细胞的情况;另一半则附着在小血管壁上。同时,在骨髓中尚贮备了约2.5×1012个成熟中性粒细胞,在机体需要时可立即动员大量这部分粒细胞进入循环血流。
中性粒细胞在血液的非特异性细胞免疫系统中起着十分重要的作用,它处于机体抵御微生物病原体,特别是在化脓性细菌入侵的第一线,当炎症发生时,它们被趋化性物质吸引到炎症部位。由于它们是藉糖酵解获得能量,因此在肿胀并血流不畅的缺氧情况下仍能够生存,它们在这里形成细胞毒存在破坏细菌和附近组织的细胞膜。由于中性粒细胞内含有大量溶酶体酶,因此能将吞噬入细胞内的细菌和组织碎片分解,这样,入侵的细菌被包围在一个局部,并消灭,防止病原微生物在体内扩散。当中性粒细胞本身解体时,释出各溶酶体酶类能溶解周围组织而形成脓肿。
中性粒细胞的细胞膜能释放出一种不饱和脂肪酸——花生四烯酸,在酶的作用下,由它再进一步生成一组旁分泌激素物质,如血栓素和前列腺素等,这类物质对调节血管口径和通透性有明显的作用,还能引起炎症反应和疼痛,并影响血液凝固(参看本章第三节及图3-8)。
2.嗜碱性粒细胞 在白细胞中嗜碱性细胞占0.5%-1%,即50个细胞/μ1。平均循环时间是12小时。这类粒细胞的胞质中存在较大和碱性染色很深的颗粒。颗粒内含有肝素和组织胺。近年来发现嗜碱性粒细胞参与体内的脂肪低谢。当食物中的脂肪被肠吸收后,周围血液中的嗜碱性粒细胞数随即增加。嗜碱性粒细胞释放出肝素(heparin),激活在血浆中的脂肪分解。这是由于肝素作为脂酶的辅基增强了脂酶的作用。结果加快了由脂肪分解为游离脂肪酸的过程。
嗜碱性粒细胞释放的组胺与某些异物(如花粉)引起过敏反应的症状有关(请参考免疫学教材)。
此外,嗜碱性粒细胞被激活时还释放一种称为嗜酸性粒细胞趋化因子A(eosinophile chemotactic factor A)的小肽,这种因子能把嗜酸性粒细胞吸引过来,聚集于局部以限制嗜碱性粒细胞在过敏反应中的作用。
3.嗜酸性粒细胞 血液中嗜酸性粒细胞占白细胞总数的2%-4%,即100-350个细胞/μ1。血液中嗜酸性粒细胞的数目有明显的昼夜周期性波动,清晨细胞数减少,午夜时细胞数增多。这种细胞数的周期性变化是与肾上腺皮质释放糖皮质激素量的昼夜波动有关的。当血液中皮质激素浓度增高时,嗜酸性粒细胞数减少;而当皮质激素浓度降低时,细胞数增加。嗜酸性粒细胞的胞质内含有较大的、椭圆形的嗜酸性颗粒。这类白细胞也具有吞噬功能。嗜酸性粒细胞在体内的作用是:①限制嗜碱性粒细胞在速发性过敏反应中的作用。当嗜碱性粒细胞被激活时,释放出趋化因子,使嗜酸性粒细胞聚集到同一局部,并从三个方面限制嗜碱性粒细胞的活性:一是嗜酸性粒细胞可产生前列腺素E使嗜碱性粒细胞合成释放生物活性物质的过程受到抑制;二是嗜酸性粒细胞可吞噬嗜碱性粒细胞所排出的颗粒,使其中含有生物活性物质不能发挥作用;三是嗜酸性粒细胞能释放组胺酶等酶类,破坏嗜碱性粒细胞所释放的组胺等活性物质。②参与对蠕虫的免疫反应。在对蠕虫的免疫反应中,嗜酸性粒细胞有重要的作用。这类粒细胞的细胞膜上分布有免疫球蛋白Fc片断和补体C3的受体。在已经对这种蠕虫具有免疫性的动物体内,产生了特异性的免疫球蛋白IgE。蠕虫经过特异性IgE和C3的调理作用后,嗜酸性粒细胞可借助于细胞表现的Fc受体和C3受体粘着于蠕虫上,并且利用细胞溶酶体内所含的过多氧化物酶等酶类损伤蠕虫体。在有寄生虫感染、过敏反应等情况时,常伴有嗜酸性粒细胞增多。
(二)单核细胞
第二类白细胞称为单核细胞,胞体较大,直径约为15-30酶μm,胞质内没有颗粒,它们约占血液中白细胞数的4%-8%。单核细胞来源于骨髓中的造血干细胞,并在骨髓中发育。当它们从骨髓进入血流时仍然是尚未成熟的细胞。与其他血细胞比较,单核细胞内含有更多的非特异性脂酶,并且具有更强的吞噬作用。单核细胞在血液中停留2-3天后迁移到周围组织中,细胞体积继续增大,直径可达50-80μm,细胞内所含的溶酶体颗粒和线粒体的数目也增多,成为成熟的细胞。固定在组织中的单核细胞称为组织巨噬细胞,它们经常大量存在于淋巴结、肺泡壁、骨髓、肝和脾等器官。激活了的单核细胞和组织巨噬细胞能生成并释放多种细胞毒、干扰素和白细胞介素,参与机体防卫机制,还产生一些能促进内皮细胞和平滑肌细胞生长的因子。在炎症周围单核细胞能进行细胞分裂,并包围异物。
(三)淋巴细胞
淋巴细胞是免疫细胞中的一大类,它们在免疫应答过程中起着核心作用。根据细胞成长发育的过程和功能的不同,淋巴细胞分成T细胞和B细胞两类。在功能上T细胞主要与细胞免疫有关,B细胞则主要与体液免疫有关。
1.T细胞 在血液的淋巴细胞中,约占70%-80%,在血液和淋巴组织之间反复循环,还可以停留在外周淋巴器官如淋巴结中。淋巴细胞的寿命较长,一般为数月,有的长达一年以上。T细胞被特异性的抗原物质激活后,进行增殖和分化,形成在功能上各异的两类细胞,即T免疫效应细胞T记忆细胞(t memory cell)。
根据T效应细胞的细胞表面特征的不同可区分为T4和T8两个亚群,而这些亚群还可根据不同的功能再分为不同类型。属于T4亚群的有:淋巴因子T细胞(t lymphokine cell,TL)、诱导性T细胞(T inductor cells,T1)和辅助性T细胞(t helper cells, TH)。淋巴因子T细胞能通过释放淋巴因子激活巨噬细胞和造血干细胞;T诱导性细胞能释放白细胞介素-2(interlukin-2),促进其他T细胞的成熟分化,而辅助性T细胞能产生一种B细胞生长因子(b cell growth factor),促使B细胞分化为浆细胞,影响抗体的产生。
T8亚型细胞,根据其功能可以再分为能抑制B细胞和T细胞活性的抑制性T细胞(t suppressor cells,Ts),和对带有特异抗原的靶细胞具有杀伤作用的细胞毒性T细胞(t cytotoxic cells, Tc)。由此可见,T细胞除了具有细胞免疫作用外,它们还具有调节其他免疫细胞特别是B细胞的功能。
长寿命的记忆T细胞在血液中不断循环,当他们再次遇到曾经接触过的抗原时,即使相隔几年之久仍能加以“识别”。在第二次与抗原体接触时能激发一种继发反应,这种反应比原发反应更强烈的引起细胞增殖,在短时间内形成大量的效应T细胞。T细胞各亚群的关系见图3-3。
2.B细胞 在血液中B细胞约占淋巴细胞总数的15%。固定在B细胞膜表面的免疫球蛋白(主要是单体IgM和IgD)是抗原的特异性受体。当它们初次与某一个抗原接触而被致敏时,一部分B细胞即分化成熟为浆细胞,浆细胞即开始生成对该抗原特异的免疫球蛋白并将它们释放到周围的组织液中,这就是免疫抗体。只有当某些调节性因子,如由辅助性T细胞所释放的淋巴因子和巨噬细胞释放的白细胞介素-1存在时,B细胞才能被抗原激活。浆细胞不再在血液中循环,在它们生存的2-3天时间里一直停留在组织中。
有小部分受抗原刺激的B细胞发展成为记忆性B细胞,寿命很长,且保持特异性,由它们增殖生成的后代细胞也保持着这种特异性。当它们再次接触具有同样特异性的抗原时,便能迅速被激活,成为特异B淋巴母细胞。由记忆性B细胞增殖生成的后代细胞愈多,被特异性抗原、激活的B细胞数也愈多。可见B细胞系统的“记忆”能力是取决于具有抗原特异性的记忆细胞数目的多少。
在血液中,除了T细胞和B细胞之外还有一类淋巴细胞,根据它们的细胞表面标志既不归属于B细胞,也不归属于T细胞。这类细胞称为裸细胞(null cell),约占血液中淋巴细胞总数的5%-10%。目前受注意的裸细胞有杀伤细胞(killer cell,K细胞)和自然杀伤细胞(matiral killer cell,NK细胞),K细胞上具有免疫球蛋白IgG的Fc片段受体,当表面覆盖有IgG(抗体)的靶细胞与K细胞接触时,IgG分子的Fc片段可与K细胞表面的Fc受体结合,激发K细胞的杀伤作用。由此可见,K细胞的杀伤作用是抗原依赖性的,但抗原是非特异的。至于NK细胞,虽然也是杀伤细胞,但其杀伤作用不依赖于抗原和抗体的存在。NK细胞广泛分布在血液和外周淋巴器官,对杀伤肿瘤细胞有重要作用。干扰素能活化NK细胞,而白细胞介素-2能刺激NK细胞的增殖和产生干扰素,因而增强NK细胞的杀伤作用。
三、血小板生理
血小板(platelets, thrombocyte)是从骨髓成熟的巨核细胞胞浆解脱落下来的小块胞质。巨核细胞虽然在骨髓的造血细胞中为数最少,仅占骨髓有核细胞总数的0.05%,但其产生的血小板却对机体的止血功能极为重要。每个巨核细胞均可产生1000-6000个血小板。
正常成年人的血小板数量是150000-350000个/μ/(150-350×109/L)。血小板有维护血管壁完整性的功能。当血小板数减少到50000个/μl(50×109/L)以下时,微小创伤或仅血压增高也使皮肤和粘膜下出现血瘀点,甚至出现大块紫癜。可能由于血小板能随时沉着于血管壁以填充内皮细胞脱落留下的空隙;而且,用同位素标记血小板示踪和电子显微镜观察,发现血小板可以融合入血管内皮细胞,因而可能对保持内皮细胞完整或对内皮细胞修复有重要作用。当血小板太少时,这些功能就难以完成而产生出血倾向。
循环血液中的血小板一般处于“静止”状态。但当血管受损伤时,通过表面接触和某些凝血因子的作用,血小板转入激活状态。激活了的血小板能释放一系列对止血过程必需的物质,关于血小板在止血过程中的作用可参看本章第三节。
生成血小板的巨核细胞也是从骨髓中的造血干细胞分化发展来的。造血干细胞首先分化生成巨核系祖细胞,也称巨核系集落形成单位(colony forming unit-megakaryocyte,CFU-Meg)。祖细胞阶段的细胞核内的染色体一般是2-3倍体。当祖细胞是2倍体或4倍体时,细胞具有增殖能力,因此这是巨核细胞系增加细胞数量的阶段。当巨核系祖细胞进一步分化为8-32倍体的巨核细胞时,胞质开始分化,内膜系统逐渐完备。最后有一种膜性物质把巨核细胞的胞质分隔成许多小区。当每个小区被完全隔开时即成为血小板,一个个血小板通过静脉窦窦壁内皮间的空隙从巨核细胞脱落,进入血流。
巨核细胞增殖、分化的调节机制类似于红细胞系生成的调节,至少受两种调节因子分别对两个分化阶段进行调节。这两种调节因子是:巨核系集落刺激因子(Meg-CSF)和促血小板生成素(thrombopoietin,TPO)。
巨核系集落刺激因子是主要作用于祖细胞阶段的调节因子,它的作用是调节巨核系祖细胞的增殖。骨髓中巨核细胞总数减少时促使该调节因子的生成增加,Meg-CSF是一种低分子糖蛋白,分子量约为46000,它与促血小板生成素具有完全不同的免疫学性质。
促血小板生成素也是一种糖蛋白,当血流中血小板减少时,促血小板生成素在血液中的浓度即增加。该调节因子的作用包括:①增强祖细胞的DNA合成和增加细胞多倍体的倍数;②刺激巨核细胞合成蛋白质;③增加巨核细胞的总数,结果增加了血小板的生成。根据去肾大鼠出现血小板减少时血液中促血小板生成素的浓度不增加的事实,推测肾是产生促血小板生成素的部位。
四、血细胞的破坏
血细胞常因衰老而被破坏,但也可因意外和各种病理原因而被破坏。破坏的方式各种血细胞不尽相同,这与各种细胞功能不同有关。
(一)红细胞的破坏
红细胞的平均寿命约为120天。在这期间,平均每个红细胞血管内循环流动约27km,在“旅途”中常常需要挤过去比它小的毛细血管及孔隙,因而不得不变形。当红细胞逐渐衰老时,细胞变形能力减退而脆性增加,在血流湍急处可因机械冲击而破损,在通过微小孔隙时也发生困难,因而特别容易停滞在脾和骨髓中被巨噬细胞所吞噬。事实上,任何组织都能使红细胞解体,这可从皮下出血的青紫块都会逐渐消失的事实证明。
红细胞在血管内破损而发生溶血,所释出的血红蛋白立即与一种血浆a2-球蛋白—触珠蛋白结合;但溶血严重达到每100m1血浆有100mg血红蛋白时,血浆中的触珠蛋白已不够用,未能与触珠蛋白结合的血红蛋白将经肾从尿中排出。与触珠蛋白结合的血红蛋白虽不致被排出,但将被肝摄取,脱铁血红素转变为胆色素,铁则以铁黄素的形式沉着于肝细胞内。在脾内被吞蚀的衰老红细胞,经消化后,铁可再利用,而脱铁血红素也转变为胆色素,运送到肝处理。
(二)血小板的破坏
血小板进入血液后,只在开始两天具有生理功能,但平均寿命可有7-14天。
在生理止血活动中,血小板聚集后本身将解体并释出全部活性物质;它也可能融入血管内皮细胞。这样看来,血小板除衰老破坏外,还可能在发挥其生理功能时被消耗。但是用51Cr或32P标记血小板观察其破坏的情况,发现血小板的破坏也随血小板的“日龄”而增多,即主要是衰老尔后被破坏。曾经对一些接受了抗凝处理的人进行观察,发现这时血凝过程虽被阻止,但血小板的寿命也不延长。这些事实,倾向于说明了平时的血管内凝血并不强(也可能这种凝血程度很小),不致影响全部血小板的平均寿命。衰老的血小板是在脾、肝和肺组织中被吞噬的。
白细胞的寿命较难准确判断。因为,粒细胞和单核细胞主要是在组织中发挥作用的;淋巴细胞则往返循环于血液-组织液-淋巴之间,而且尚可增殖分化。一般来说,中性粒细胞在循环血液中停留8小时左右即进入组织,一般三、四天后将衰老死亡;若有细菌入侵,粒细胞在吞噬活动中可释出溶酶体酶过多而发生“自我溶解”,与破坏的细菌和组织片共同构成脓。
第三节 生理止血、血液凝固与纤维蛋白溶解
小血管损伤后血液将从血管流出,但在正常人,数分钟后出血将自行停止,称为生理止血。用一个小撞针或注射针刺破耳垂或指尖使血液流出,然后测定出血延续的时间,这一段时间称为出血时间(bleeding time)。出血时间的长短可以反映生理止血功能的状态。正常出血时间为1-3分钟。血小板减少,出血时间即相应延长,这说明血小板在生理止血过程中有重要作用;但是血浆中一些蛋白质因子所完成的血液凝固过程也十分重要。凝血有缺陷时常可出血不止。
生理止血过程包括三部分功能活动。首先是小血管于受伤后立即收缩,若破损不大即可使血管封闭;主要是由损伤刺激引起的局部缩血管反应,但持续时间很短。其次,更重要的是血管内膜损伤,内膜下组织暴露,可以激活血小板和血浆中的凝血系统;由于血管收缩使血流暂停或减缓,有利于激活的血小板粘附于内膜下组织并聚集成团,成为一个松软的止血栓以填塞伤口。接着,在局部又迅速出现血凝块,即血浆中可溶的纤维蛋白源转变成不溶的纤维蛋白分子多聚体,并形成了由血纤维与血小板一道构成的牢固的止血栓,有效地制止了出血。与此同时,血浆中也出现了生理的抗凝血活动与纤维蛋白溶解活性,以防止血凝块不断增大和凝血过程漫延到这一局部以外。显然,生理止血主要由血小板和某些血浆成分共同完成。
一、血凝、抗凝与纤维蛋白溶解
血液离开血管数分钟后,血液就由流动的溶胶状态变成不能流动的胶冻状凝块,这一过程称为血液凝固(blood coagulation)或血凝。在凝血过程中,血浆中的纤维蛋白源转变为不溶的血纤维。血纤维交织成网,将很多血细胞网罗在内,形成血凝块。血液凝固后1-2小时,血凝块又发生回缩,并释出淡黄色的液体,称为血清。血清与血浆的区别,在于前者缺乏纤维蛋白原和少量参与血凝的其他血浆蛋白质,但又增添了少量血凝时由血小板释放出来的物质。
血浆内具备了发生凝血的各种物质,所以将血液抽出放置于玻璃管内即可凝血。血浆内又有防止血液凝固的物质,称为抗凝物质(anticoagulant)。血液在血管内能保持流动,除其他原因外,抗凝物质起了重要的作用。血管内又存在一些物质可使血纤维再分解,这些物质构成纤维蛋白溶解系统(简称纤溶系统)(fibrinloytic system)。
在生理止血中,血凝、抗凝与纤维蛋白溶解相互配合,既有效地防止了失血,又保持了血管内血流畅通。
(一)血液凝固
凝血因子血浆与组织中直接参与凝血的物质,统称为凝血因子(bloodclotting factors),其中已按国际命名法用罗马数字编了号的有12种(表3-4)。此外,还有前激肽释放酶、高分子激肽原以及来自血小板的磷脂等直接参与凝血过程。除因子Ⅳ与磷脂外,其余已知的凝血因子都是蛋白质,而且因子Ⅱ、Ⅶ、Ⅸ、Ⅹ、Ⅺ、Ⅻ以及前激肽释放酶都是蛋白酶。这些蛋白酶都属于内切酶,即每一种酶只能水解某两种氨基酸所形成的肽键。因而不能将某一知肽链分解成很多氨基酸,而只能是对某一条肽链进行有限的水解。通常在血液中,因Ⅱ、Ⅶ、Ⅸ、Ⅹ、Ⅺ、Ⅻ都是无活性的酶原,必须通过有限水解在其肽链上一定部位切断或切下一个片段,以暴露或形成活性中心,这些因子才成为有活性的酶,这个过程称为激活。被激活的酶,称为这些因子的“活性型”,习惯上于该因子代号的右下角加一“a”字来表示。如凝血酶原被激活为凝血酶,即由因子Ⅱ变成因子Ⅱa。因子Ⅶ是以活性型存在于血液中的,但必须有因子Ⅲ(即组织凝血激酶)同时存在才能起作用,而在正常时因子Ⅲ只存在于血管外,所以通常因子Ⅶ在血流中也不起作用。
表3-4 按国际命名法编号的凝血因子
| 编 号 |
同 义 名 |
| 因子Ⅰ |
纤维蛋白原(fibrinogen) |
| 因子Ⅱ |
凝血酶原(prothrombin) |
| 因子Ⅲ |
组织凝血激素(tissue thromboplastin) |
| 因子Ⅳ |
Ca2+ |
| 因子Ⅴ |
前加速素(proaccelerin) |
| 因子Ⅶ |
前转变素(proconvertin) |
| 因子Ⅷ |
抗血友病因子(antihemophilic factor,AHF) |
| 因子Ⅸ |
血浆凝血激酶(plasma thromboplastin component,PTC) |
| 因子Ⅹ |
Stuart-Prower因子 |
| 因子Ⅺ |
血浆凝血激酶前质(plasma thromboplastin antecedent,PTA) |
| 因子Ⅻ |
接触因子(contact factor) |
| 因子ⅩⅢ |
纤维蛋白稳定因子(fibrin-stabilizing factor) |
凝血过程凝血过程基本上是一系列蛋白质有限水解的过程,凝血过程一旦开始,各个凝血因子便一个激活另一个,形成一个“瀑布”样的反应链直至血液凝固。凝血过程大体
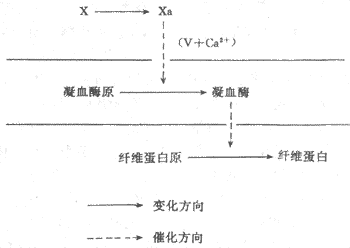
图3-4凝血过程的三个阶段简图
上可分为三个阶段(图3-4):即因子χ激活成χa;因子Ⅱ(凝血酶原)激活成Ⅱa(凝血酶);因子Ⅰ(纤维蛋白原)转变成Ⅰa(纤维蛋白)。
因子χ的激活可以通过两种途径。如果只是损伤血管内膜或抽出血液置于玻璃管内,完全依靠血浆内的凝血因子逐步使因子χ激活从而发生凝血的,称为径内源性激活途径(intrinsic route);如果是依靠血管外组织释放的因子Ⅲ来参与因子χ的激活的,称为外源性激活途径(extrinxic route),如创伤出血后发生凝血的情况。
1.内源性途径一般从因子Ⅻ的激活开始。血管内膜下组织,特别是胶原纤维,与因子Ⅻ接触,可使因子Ⅻ激活成Ⅻa。Ⅻa可激活前激肽释放酶使之成为激肽释放酶;后者反过来又能激活因子Ⅻ,这是一种正反馈,可使因子Ⅻa大量生成。Ⅻa又激活因子Ⅺ成为Ⅺa。由因子Ⅻ激活到Ⅺa形成为止的步骤,称为表面激活。表面激活过程还需有高分子激肽原*参与,但其作用机制尚不清楚。表面激活所形成的Ⅺa再激活因子Ⅸ生成Ⅸa,这一步需要有Ca2+(即因子Ⅳ)存在。Ⅸa再与因子Ⅷ和血小板3因子(PF3)及Ca2+组成因子Ⅷ复合物,即可激活因子Χ生成Χa。血小板3因子可能就是血小板膜上的磷脂,它的作用主要是提供一个磷脂的吸附表面。因子Ⅸa和因子χ分别通过Ca2+而同时连接于这个磷脂表面,这样,因子Ⅸa即可使因子χ发生有限水解而激活成为χa。但这一激活过程进行很缓慢,除非是有因子Ⅷ参与。因子Ⅷ本身不是蛋白酶,不能激活因子х,但能使Ⅸa激活因子χ的作用加快几百倍。所以因子Ⅷ虽是一种辅助因子,但是十分重要。遗传性缺乏因子Ⅷ将发生甲型血友病(hemophilia A),这时凝血过程非常慢,甚至微小的创伤也出血不止。先天性缺乏因子Ⅸ时,内源性途径激活因子χ的反应受阻,血液也就不易凝固,这种凝血缺陷称为B型血友病(hemophilia B)。
2.外源性途径由因子Ⅶ与因子Ⅲ组成复合物,在有Ca2+存在的情况下,激活因子χ生成χa。因子Ⅲ,原名组织凝血激酶,广泛存在于血管外组织中,但在脑、肺和胎盘组织中特别丰富。因子Ⅲ为磷脂蛋白质。Ca2+的作用就是将因子Ⅶ与因子χ都结合于因子Ⅲ所提供的磷脂上,以便因子Ⅶ催化因子χ的有限水解,形成χa。
Χa又与因子Ⅴ、PE3和Ca2+形成凝血酶原酶复合物,激活凝血酶原(因子Ⅱ)生成凝血酶(Ⅱa)。在凝血酶原酶复合物中的PF3也是提供磷脂表面,因子Χa和凝血酶原(因子Ⅱ)通过Ca2+而同时连接于磷脂表面,χa催化凝血酶原进行有限水解,成为凝血酶(Ⅱa)。因子Ⅴ也是辅助因子,它本身不是蛋白酶,不能催化凝血酶原的有限水解,但可使χa的作用增快几十倍。
因子χ与凝血酶原的激活,都是在PF3提供的磷脂表面上进行的,可以将这两个步骤总称为磷脂表面阶段。在这一阶段中,因子Ⅱ(凝血酶原)、因子Ⅶ、因子Ⅸ和因子χ,都必须通过Ca2+连接于磷脂表面。因此,在这些因子的分子上必须有能与Ca2+结合的部位。现已知,因子Ⅱ、Ⅶ、Ⅸ、х都是在肝中合成。这些因子在肝细胞的核糖体处合成肽链后,还需依靠维生素K的参与,使肽链上某些谷氨酸残基于γ位羧化成为γ-羧谷氨酸残基,构成这些因子的Ca2+结合部位。因此,缺陷维生素K,将出现出血倾向。
凝血酶(thrombin)有多方面的作用。它可以加速因子Ⅶ复合物与凝血酶原酶复合物的形成并增加其作用,这也是正反馈;它又能激活因子ⅩⅢ生成ⅩⅢa;但它的主要作用是催化纤维蛋白原的分解,使每一分子纤维蛋白原从N-端脱下四段小肽,转变成为纤维蛋白单体(fibrin monomer),然后互相连接,特别是在ⅩⅢa作用下形成牢固的纤维蛋白多聚体(fibrin polymers),即不溶于水的血纤维。上述凝血过程可见图3-5表示。
一般来说,通过外源性途径凝血较快,内源性途径较慢,但在实际情况中,单纯由一种途径引起凝血的情况不多。
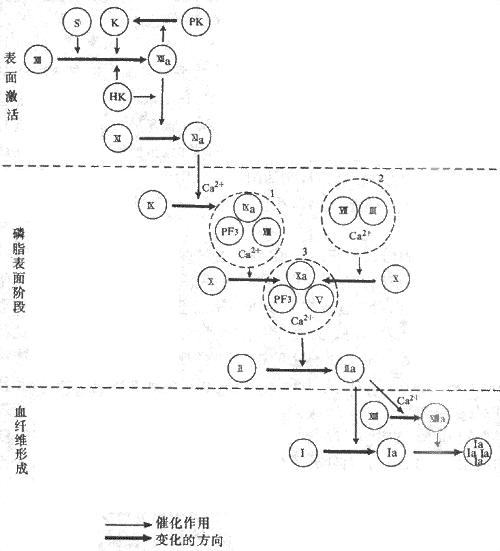
图3-5血液凝固过程示意图
S;血管内皮下组织 PF3:血小板3因子PK:前激肽释放酶 1:因子Ⅷ复合物
K:激肽释放酶 2:因子Ⅶ复合物 HK:高分子激肽原 3:凝血酶原酶复合物
在凝血的某些阶段,内源性途径与外源性途径之间存在着功能的交叉,也就是说,这两条途径之间具有某些“变通”的途径。例如,外源性的因子Ⅶa和Ⅲ可以形成复合物直接激活因子Ⅸ,从而部分代替了因子Ⅺ和Ⅻa的功能。这一机制得以解释为什么在因子Ⅸ缺乏时的出血倾向,较因子Ⅺ和Ⅻ缺乏时更为严重。另一方面,内源性因子Ⅻ的裂解产物和因子Ⅸa也能激活外源性的因子Ⅶ。
(二)抗凝系统的作用
正常人1ml血浆含凝血酶原约300单位,在凝血时通常可以全部激活。10ml血浆在凝血时生成的凝血酶就足以使全身血液凝固。但在生理止血时,凝血只限于某一小段血管,而且1ml血浆中出现的凝血酶活性很少超出8-10单位,说明正常人血浆中有很强的抗凝血酶活性。
现在已经查明,血浆中最重要的抗凝物质是抗凝血酶Ⅲ(antithrombinⅢ)和肝素,它们的作用约占血浆全部抗凝血酶活性的75%。抗凝血酶Ⅲ是血浆中一种丝氨酸蛋白酶抑制物(serine protease inhibitor)。因子 Ⅱa、Ⅶ、Ⅸa、χa、Ⅻa的活性中心均含有丝氨酸残基,都属于丝氨酸蛋白酶(serine protease)。抗凝血酶Ⅲ分子上的精氨酸残基,可以与这些酶活性中心的丝氨酸残基结合,这样就“封闭”了这些酶的活性中心而使之失活。在血液中,每一分子抗凝血酶Ⅲ,可以与一分子凝血酶结合形成复合物,从而使凝血酶失活。
肝素是一种酸性粘多糖,主要由肥大细胞和嗜碱性粒细胞产生,存在于大多数组织中,在肝、肺、心和肌组织中更为丰富。
肝素在体内和体外都具有抗凝作用,肝素抗凝的主要机制在于它能结合血浆中的一些抗凝蛋白,如抗凝血酶Ⅲ和肝素辅助因子Ⅱ(heparincofactorⅡ)等,使这些抗凝蛋白的活性大为增强。当肝素与抗凝血酶Ⅱ的某一个ε-氨基赖氨酸残基结合,则抗凝血酶Ⅲ与凝血酶的亲和力可增强100倍,使两者结合得更快,更稳定,使凝血酶立即失活。当肝素与肝素辅助因子Ⅱ结合而激活后者时,被激活的肝素辅助因子Ⅱ特异性地与凝血酶结合成复合物,从而使凝血酶失活,在肝素的激活作用下,肝素辅助因子灭活凝血酶的速度可以加快约1000倍。
肝素还可以作用血管内皮细胞,使之释放凝血抑制物和纤溶酶原激活物,从而增强对凝血的抑制和纤维蛋白的溶解。此外,肝素能激活血浆中的脂酶,加速血浆中乳糜微粒的清除,因而减轻脂蛋白对血管内皮的损伤,有助于防止与血脂有关的血栓形成。
天然肝素是一种分子量不均一的混合物,分子量为3000-57000不等。这种不均一是生物合成过程有差异所致。不同分子量肝素的生物作用也不完全相同。一般将分子量在7000以下肝素称为低分子量肝素。低分子量肝素只与抗凝血酶Ⅱ结合,而分子量较大的肝素除了能与抗凝血酶Ⅲ结合外,还能与血小板结合,结果不仅抑制血小板表面凝血酶的形成,而且抑制血小板的聚集与释放。由于分子量较大的肝素抗凝作用的环节较多,作用较为复杂,易引起出血倾向,而低分子时肝素具有半衰期较长,抗凝效果好和引起出血倾向少等优点,因而更适于作为外源性抗凝剂。
从化学本质看,凝血过程是一系列酶促反应链,其中主链是一系列丝氨酸蛋白酶的作用。组成抗凝系统的一类物质是血浆中存在的多种丝氨酸蛋白酶抑制物。上述抗凝血酶Ⅲ是其中最为重要的一种。属于丝氨酸蛋白酶抑制物的抗凝物质还有能抑制补体第1成分和因子Ⅻa、Ⅺa、的C1抑制物(C1inhibitor),广谱的蛋白酶抑制物a2-巨球蛋白(a2-macroglobulin)等。抗凝系统中的另一类物质是辅因子抑制物,这类抑制物通过对凝血辅因子如因子Ⅴ和Ⅷ活性的抑制而实现抗凝作用。下述的蛋白质C和凝血酶调制素都是属于这类抗凝物质。
蛋白质 C(proteinC)是近年来引起注意的另一种具有抗凝作用的血浆蛋白,分子量为62000,它由肝合成,并有赖于维生素K的存在。蛋白质C以酶原形式存在于血浆中,蛋白质C在凝血酶的作用下发生有限的酶解过程,从分子上裂解下一个小肽后即具有活性。激活的蛋白质C与血管内皮表面存在的辅因子凝血酶调制素(thrombomodulin)结合成复合物,在Ca2+存在的条件下这种复合物使蛋白质C的激活过程大大加快。激活的蛋白质C具有多方面的抗凝血、抗血栓功能,主要的作用包括:①灭活凝血因子Ⅴ和Ⅷ。这种灭活也是一种酶解过程,即是把因子Ⅴ和Ⅷ的重链进行水解,使他们与磷脂的结合力降低。这种灭活反应需要有Ca2+的存在,反应的速度是很快的;②限制因子Χa与血小板结合。存在于血小板表面的因子Ⅴa是因子Χa的受体。当因子Χa与这种受体结合后,可使因子Χa的活性大为增强。由于激活的蛋白质C能使因子Ⅴa灭活,使因子Χa与血小板的结合受到阻碍,结果可使因子Χa激活凝血酶原的作用大为减弱;③增强纤维蛋白的溶解。激活的蛋白质C能刺激溶酶原激活物的释放,从而增强纤溶活性。激活的蛋白质C的这一作用只有在内皮细胞存在的情况下才能实现。维生素K缺乏或患肝病可使蛋白质C的合成减少;某些病理情况造成血管内皮广泛损伤时使凝血酶调制减少,这种减少转而使蛋白质C的激活受阻。不论是蛋白质C减少或活化受阻都增加了形成血栓的倾向。
体外延缓或阻止血液凝固的因素:①降低温度,当反应系统的温度降低至10℃以下时,很多参与凝血过程的酶的活性下降,因些可延缓血液凝固,但不能完全阻止凝血的发生;②光滑的表面,也称不湿表面,可减少血小板的聚集和解体,减弱对凝血过程的触发,因而延缓了凝血酶的形成。例如,将血液盛放在内表面涂有硅胶或石蜡的容器内,即可延缓血凝,③去Ca2+,由于血液凝固的多个环节中都需要Ca2+的参加,因此如在体外向血液中加入某些能与钙结合形成不易解离但可溶解的络合物,从而减少了血浆中的Ca2+,防止了血液凝固。由于少量枸橼酸钠进入血液循环不致产生毒性,因此常用它作抗凝剂来处理输血用的血液。此外,实验室中可使用草酸铵、草酸钾和螯合剂乙二胺四乙酸(ECTA)作抗凝剂,它们能与Ca2+结合不易溶解的复合物。但它们对机体有害,因而不能进入体内。
(三)纤维蛋白溶解
在生理止血过程中,小血管内的血凝块常可成为血栓,填塞了这一段血管。出血停止、血管创伤愈合后,构成血栓的血纤维可逐渐溶解,先形成一些穿过血栓的通道,最后可以达到基本畅通。血纤维溶解的过程,称为纤维蛋白溶解(简称纤溶)。
纤维蛋白溶解(纤溶)系统包括四种成分,即纤维蛋白溶解酶原(plasminogen)(纤溶酶原,血浆素原)、纤维蛋白溶解酶(plasmin)(纤溶酶,血浆素)、纤溶原激活物与纤溶抑制物。纤溶的基本过程可分两个阶段,即纤溶酶原的激活与纤维蛋白(或纤维蛋白原)的降解(图3-6)。
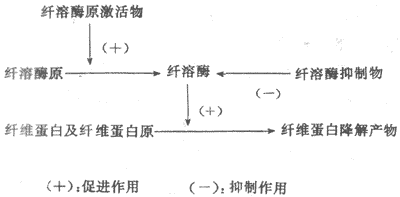
图3-6纤维蛋白溶解系统
1.纤溶酶原激活纤溶酶原很可能是在肝、骨髓、嗜酸性粒细胞与肾中合成的;在正常成年人每100ml血浆中约含10-20mg纤溶酶原,婴儿较少,妇女晚期妊娠时增多。
纤溶酶原激活物分布广而种类多,主要有三类:第一类为血管激活物,在小血管内皮细胞中合成后释放于血中,以维持血浆内激活物浓度于基本水平。血管内出现血纤维凝块时,可使内皮细胞释放大量激活物。所释放的激活物大都吸附于血纤维凝块上,进入血流的很少。肌肉运动、静脉阻断、儿茶酚胺与组胺等也可使血管内皮细胞合成和释放的激活物增多。第二类为组织激活物,存在于很多组织中,主要是在组织修复、伤口愈合等情况下,在血管外促进纤溶。肾合成与分泌的尿激酶就属于这一类激活物,活性很强,有助于防止肾小管中纤维蛋白沉着。第三类为依赖于因子Ⅻ的激活物,例如前激肽释放酶被Ⅻa激活后,所生成的激肽释放酶即可激活纤溶酶原。这一类激活物可能使血凝与纤溶互相配合并保持平衡。
血浆中的激活物的半衰期约13分钟,通常迅速被肝清除。
纤溶酶原的激活也是有限水解的过程,在激活物的作用下,脱下一段肽链成为纤溶酶。
2.纤维蛋白(与纤维蛋白原)的降解 纤溶酶和凝血酶一样,也是蛋白酶,但是它对纤维蛋白原的作用与凝血酶不同。凝血酶只是使纤维蛋白原从其中两对肽链的N-端各脱下一个小肽,使纤维蛋白原转变成纤维蛋白。纤溶酶却是水解肽链上各单位的赖氨酸-精氨酸键,从而逐步将整个纤维蛋白或纤维蛋白原分割成很多可溶的小肽,总称为纤维蛋白降解产物。纤维蛋白降解产物一般不能再出现凝固,而且其中一部分有抗血凝的作用。
纤溶酶是血浆中活性最强的蛋白酶,但特异性较小,可以水解凝血酶、因子Ⅴ、因子Ⅷ、激活因子Ⅻa;促使血小板聚集和释放5-羟色胺、ADP等;还能激活血浆中的补体系统;但它的主要作用是水解纤维蛋白原和纤维蛋白。血管内出现血栓时,纤溶主要局限于血栓,这可能是由于血浆中有大量抗纤溶物质(即抑制物)存在,而血栓中的纤维蛋白却可吸附或结合较多的激活物所致。正常情况下,血管内膜表面经常有低水平的纤溶活动,很可能血管内也经常有低水平的凝血过程,两者处于平衡状态。
3.抑制物及其作用血液中存在的纤溶抑制物主要是抗纤溶酶(antiplasmin) ,但其特异性不大,例如,a2-巨球蛋白能普遍抑制各种内切酶,包括纤溶酶、胰蛋白酶、凝血酶、激肽释放酶等。每一分子a2-巨球蛋白可结合一分子纤溶酶,然后迅速被吞噬细胞清除。血浆中a1-抗胰蛋白酶也对纤溶酶有抑制作用,但作用较慢,然而它分子量小,可渗出血管,控制血管外纤溶活动。看来这些抑制物的作用,是广泛控制在血凝与纤溶两个过程中起作用的一些酶类。这对于将血凝与纤溶局限于创伤部位,有重要意义。
(四)表面激活与血液的其他防卫功能
血管损伤后暴露出内膜下组织,通过表面激活使因子Ⅻ激活成因子Ⅻa,因子Ⅻa 又激活肽释放酶成为激肽释放酶,而激肽释放酶又可激活因子Ⅻ,从而形成一个正反馈环,可形成足够的Ⅻa 和激肽释放酶。这样,不但同时激活了血凝和纤溶系统,也激活了补体系统和激肽系统(图3-7)。补体激活的一些产物和激肽都是作用很强的趋化因子,能吸收吞噬细胞到受损伤的部位,产生非特异性免疫反应;这样使生理止血功能与免疫功能相配合,有效的保护机体,减少创伤带来的损害。
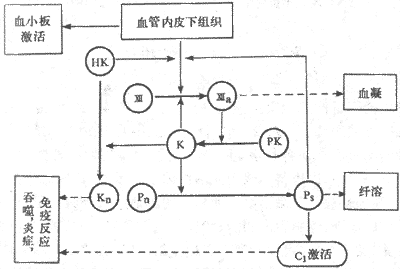
图3-7表面激活也血液各种防卫功能关系示意图
PK:前激肽释放酶 Pn:纤溶酶原 K:激肽释放酶 Pn:纤溶酶
HK:高分子激肽原 CI:补体 Kn:激肽 Ⅻ与Ⅻa,因子Ⅻ及其激活型
二、血小板的止血功能
因血管创伤而失血时,血小板在生理止血过程中的功能活动大致可以分为两段,第一段主要是创伤发生后,血小板迅速粘附于创伤处,并聚集成团,形成较松软的止血栓子;第二段主要是促进血凝并形成坚实的止血栓子。
(一)血小板粘附与聚集
止血中较松软的血小板止血栓子的形成,要经过血小板粘附与聚集两个过程。
血管损伤后,流经此血管的血小板被血管内皮下组织表面激活,立即粘附于损伤处暴露的胶原纤维上。参与血小板粘附过程的主要因素包括:血小板膜糖蛋白I(GPI)、vonWillebrand因子(vW因子)和内皮下组织中的胶原。当血小板缺乏GPI或胶原纤维变性时,血小板粘附(thrombocyte adhesion)功能便受损。发生血小板粘附过程的可能机制是vW因子再与血小板膜上的特异受体结合。此外,血小板膜上的糖苷移换酶活性和胶原蛋白分子的构型与粘附也有着密切关系。
粘附主要是一种表面现象,粘附一旦发生了,血小板的聚集过程(thrombocyteaggregation)也随即发生。聚集是指一些血小板相互粘连在一起的过程。聚集开始时,血小板由圆盘形变成球形,并伸出一些貌似小刺的伪足;同时血小板脱粒,即原来贮存于致密颗粒内的ADP、5-羟色胺等活性物质被释放。ADP释放和某些前列腺素的生成,对聚集的引起十分重要。
1.ADP的作用 在体外实验中看到,ADP是使血小板聚集最重要的物质,特别是从血小板释放出来的这种内源性ADP尤其重要。在血小板悬液中加入小量ADP(浓度在0.9μmol/L以下),能迅速引起血小板聚集,但很快又解聚;若加入中等剂量的ADP(1.0μmol/L左右),则在第一聚集时相结束和解聚后不久,又出现第二个不可逆的聚集时相,这是由于血小板释放的内源性ADP所引起的;若是加入大量ADP,则迅速引起不可逆的聚集,即直接进入聚集的第二时相.以不同剂量的凝血酶加入血小板悬液,也可使血小板发生聚集;而且与ADP相似,随着加入剂量的逐渐增加,可看到从只有第一时相可逆性聚集,到出现两个时相的聚集,再到直接进入第二时相的聚集.因为,用腺苷阻断内源性ADP的释放或用腺苷三磷酸双磷酸酶(apyrase)以破坏ADP,均可抑制凝血酶引起的聚集,说明凝血酶的作用可能是由于凝血酶与血小板细胞膜上的凝血酶受体结合后,引起内源性ADP释放所引起的。加入胶原也可引进悬液中的血小板聚集,然而只有第二时相的不可逆聚集,一般认为这也是由于胶原引起内源性的ADP释放所致。
一般能引起血小板聚集的物质均可使血小板内cAMP减少,而抑制血小板聚集的则使cAMP增多。因而目前认为,可能是cAMP减少引起血小板内Ca2+增加,促使内源性ADP释放。
ADP引起血小板聚集,还必须有Ca2+和纤维蛋白原存在,而且要消耗能量。将血小板悬浮于缺乏葡萄糖的溶液中数小时,或用药物阻断或减弱血小板产生ATP的代谢过程,均将抑制血小板的聚集。ADP也不能使洗净了的血小板聚集,除非加入纤维蛋白原;但凝血酶和胶原可使洗净了的血小板聚集。因为在这种情况下,可使血小板a 颗粒内的纤维蛋白原释放。
ADP是通过血小板膜上的ADP受体引起聚集的。目前认为,血小板膜上有表面ATP酶,这是防止血小板相互粘聚所必需的,而ADP可抑制表面ATP酶的活性;ADP还可使血小板暴露出磷脂表面,因而可以通过Ca2+“搭桥”而互相粘聚。
2.血小板前列腺素类物质的作用血小板质膜的磷脂中含有花生四烯酸,血小板细胞内有磷脂酸A2。在血小板被表面激活时,磷脂酶A2也被激活。在磷脂酶A2的催化作用下,花生四烯酸从质膜的磷脂中分离出来。花生四烯酸在血小板的环氧化酶作用下,产生前列腺素G2和H2 (PGG2、PGH2)。PGG2和PGH2都是环内过氧化物,有很强的引起血小板聚集的作用。但是PGG2和PGH2都很不稳定,可以直接生成小量PGE2和PGF2。PGH2可以在血栓素合成酶的催化作用下,形成大量血栓素A2(thromboxane A2,TXA2)。TXA2 使血小板内cAMP减少,因而有很强的聚集血小板的作用,也有很强的收缩血管的作用。TXA2也不稳定迅速转变成无活性的血栓素B2(TXB2)。咪唑(imidazole)可抑制血栓素合成酶,所以有防止血小板聚集的作用。此外,正常血管壁内皮细胞中有前列腺环素合成酶,可以催化血小板生成的PGH2 生成前列腺环素(prostacyclin,PGI2)。PGI2可使血小板内cAMP增多,因而有很强抑制血小板聚集的作用,也有很强的抑制血管收缩的作用。PGI2也很不稳定,迅速变成无活性的6-酮-PGF1a。关于由花生四烯酸衍变成TXA2与PGI2的过程可参看图3-8。
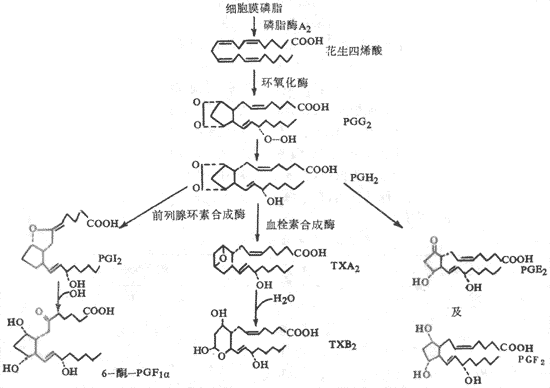
图3-8血小板前列腺素与血栓素的合成
在发现TXA2和PGI2之后,曾设想在正常情况下可能是血管壁的PGI2与血小板的TXA2之间保持了平衡,因而使血小板不致聚集。可以设想,血管损伤暴露内皮下组织时,一方面激活血小板和激活内源性凝血途径,损坏的血管组织释放凝血因子Ⅲ又激活外源性凝血途径,于是在此局部迅速形成凝血酶;另一方面血管损伤使局部血管壁PGI2减少。这样,由此血管通过的血小板即粘附于损伤处的胶原纤维上,随即血小板也发生变形、聚集,并激活磷脂酶A2,导致合成TXA2,TXA2可使血小板内cAMP减少而游离Ca2+增多,以致血小板脱粒释放内源性ADP,又使更多的血小板聚集,迅速形成松软的止血栓子。
(二)血小板与凝血
血小板对于血液凝固有重要的促进作用,如将血液置于管壁涂一薄层硅胶的玻璃管中,使血小板不易解体,虽然未加入任何抗凝剂,血液可保持液态达72小时以上;若加入血小板匀浆则立即发生凝血。这说明血小板破裂后的产物对于凝血过程有很强的促进作用。
血小板表面的质膜结合有多种凝血因子,如纤维蛋白原、因子Ⅴ、因子Ⅺ、因子ⅩⅢ等。a-颗粒中也含有纤维蛋白原、因子因子ⅩⅢ和一些血小板因子(PE),其中PF2和PF3都是促进血凝的。PF4可中和肝素,PF6则抑制纤溶。当血小板经表面激活后,它能加速凝血因子Ⅻ和Ⅺ的表面激活过程。血小板所提供的磷脂表面(PF3),据估计可使凝血酶原的激活加快两万倍。因子Ⅹa和因子Ⅴ连接于此磷脂表面后,还可以免受抗凝血酶Ⅲ和肝素对它们的抑制作用。
当血小板聚集形成止血栓时,凝血过程已在此局部进行,血小板已暴露大量磷脂表面,为因子Ⅹ和凝血酶原的激活提供了极为有利的条件。血小板聚集后,其α颗粒中的各种血小板因子释放出来,促进血纤维的形成和增多,并网罗其它血细胞形成凝块。因而血小板虽逐渐解体,止血栓子仍可增大。血凝块中留下的血小板有伪足伸入血纤维网中,这些血小板中的收缩蛋白收缩,使血凝块回缩,挤压出其中的血清而成为坚实的止血栓,牢牢地封住血管缺口。
在表面激活血小板和血凝系统时,同时也激活了纤溶系统。血小板内所含的纤溶酶及其激活物将释放出来。血纤维和血小板释放的5-羟色胺等,也能使内皮细胞释放激活物。但是由于血小板解体,同时释放出PF6和另一些抑制蛋白酶的物质,所以在形成血栓时,不致受到纤溶活动的干扰。
第四节 血型与输血原则
一、血型与红细胞凝集
若将血型不兼容的两个人的血滴放在玻片上混合,其中的红细胞即聚集成簇,这种相容称为凝集(agglutination)。红细胞的凝集有时还伴有溶血。当血型(bolld group)不相容的血液输入循环血液中时,在血管内可发生同样的情况,此凝集成簇的红细胞可以堵塞毛细血管,溶血将损害肾小管,同时常伴发过敏反应,其结果可危及生命。
造成红细胞凝集的机制是抗原-抗体反应。凝集原的特异性完全取决于镶嵌入红细胞膜上的一些特异糖蛋白,在凝集反应中糖蛋白起着抗原的作用,因而称它们为凝集原(agglutinogen)。能与红细胞膜上的凝集原起反应的特异抗体则称为凝集素(agglutinin)。凝集素是由γ-球蛋白构成的,它们溶解在血浆中。发生抗原-抗体反应时,由于每个抗体上具有10个左右与抗原结合的部位,抗体在若干个带有相应抗原的红细胞之间形成桥梁,因而使它们聚集成簇。
人血液中,在红细胞上都具有一套特异的凝集原。目前在红细胞上已确定有许多种不同的抗原,大约有30种抗原能引发相当剧烈的机体反应。血型是指红细胞上特异抗原的类型。表3-5中列出了ABO、Rh、MNSs、P等9个最重要的血型系统和它们所具有的特异抗体。动用现代免疫学手段可以在红细胞膜上鉴别出约400种不同特征的抗原。如果只将其中已经分类的抗原型作为依据,就有3亿种不同的可能组合,可见血型抗原最为重要的血型是ABO系统和Rh系统。
表3-5 重要血型及其特异抗体
| 血型系统 |
抗体 |
溶血性输血反应 |
| ABO |
抗A |
有 |
|
抗B |
有 |
|
抗A1 |
很少 |
|
抗H |
无 |
| Rh |
抗C |
有 |
|
抗c |
有 |
|
抗Cw |
有 |
|
抗D |
有 |
|
抗E |
有 |
|
抗e |
有 |
| MNSs |
抗M,N,S,s |
很少 |
| P |
抗P1 |
无 |
| Lutheran |
抗Lub |
有 |
| Kell |
抗K |
有 |
| Lewis |
抗Lea,b |
有 |
| Duffy |
抗Fya |
有 |
| Kidd |
抗JKa |
有 |
虽然通常所说的血型是指红细胞的血型,但是存在于红细胞上的血型抗原也存在于白细胞、血小板和一般组织细胞上,引外在白细胞和血小板上还存在它们本身特有的抗原。
二、红细胞血型
1901年 Landsteiner发现了第一个血型系统,即ABO血型系统,从此为人类揭开了血型的奥秘,并使输血成为安全度较大的临床治疗手段。
(一)ABO血型系统
1.ABO血型的分型及其物质基础ABO血型是根据红细胞膜上存在的凝集原A与凝集原B的情况而将血液分为4型。凡红细胞只含A凝集原的,即称A型;如存在B凝集原的,称为B型;若A与B两种凝集原都有的称为AB型;这两种凝集原都没有的,则称为O型。不同血型的人的血清中各含有不同的凝集素,即不含有对抗内他自身红细胞凝集原的凝集素。在A型人的血清中,只含有抗B凝集素;B型人的血清中,只含有抗A凝集素;AB型人的血清中没有抗A和抗B凝集素;而O型人的血清中则含有抗A和抗B凝集素(表3-6)。后来进一步发现4种血型的红细胞上都含有H抗原,O型的红细胞上也含有H抗原。H抗原是形成A、B抗原的结构基础,但是H物质的抗原性很弱,因此血清中一般都没有抗H抗体。利用抗血清作细致的检测可以发现,A型还可再区分为A1、和A2亚型。在A1亚型红细胞上含有A和A1抗原,而A2型红细胞上仅含有A抗原。相应的在A1型血清中只有抗B凝集素,而A2型血清中除抗B凝集素之外,还含有抗A1凝集素。因此当将A1型的血液输给A2型的人时,血清中的抗A1凝集素可能与A1型的人红细胞上的A1抗原结合产生凝集反应。据调查,我国汉族人中A2型和A2B型分别不超过A型和AB型人群的1%,即使如此,在测定血型和输血时都应注意到A亚型的存在。
表3-6 ABO血型系统中的凝集原和凝集素
| 血型 |
凝集原 |
凝集素 |
| A型 |
A |
抗B |
| B型 |
B |
抗A |
| AB型 |
A+B |
无 |
| O型 |
无 |
抗A+抗B |
上述ABO系统各种血型抗原的特异必理决定于糖蛋白上所含的糖链。这些糖链都是由少数糖基所组成的寡糖链(oligosaccharide)。这些寡糖链都暴露在红细胞的表面,图3-9示意了ABO系统中H、A和B抗原的寡糖链结构差异。
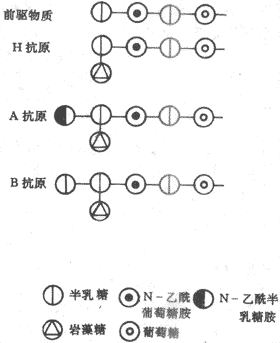
图3-9 ABH抗原物质化学结构
2.血型的遗传学特征血型是先天遗传的。出现在某一染色体的同一位置上的不同基因,称为等们基因(allele)。ABOA(H)系统中控制A、B、H抗原生成的基因即为等位基因。在染色体二倍体上只可能出现上述三个等们基因中的两个,其中一个来自父体,另一个来自母体,这两个等位基因就决定了子代血型的基因型(genotype)。这两种基因型首先决定了转糖酶的氨基酸组成和顺序,也即决定了生成的转糖酶的种类,后者转而决定表现血型抗原特异性的寡糖链的组成,也即这个人的血型表型(phenotype)。表3-7上显示了ABO系统中决定每种血型表型的可能基因型。从表上可以看出,A基因和B基因是显性基因,O基因则为隐性基因。因此,红细胞上表型O只可能来自两个O基因,而表型A或b 由于可能分别来自AO和BO基因型,因而,A型或B型的父母完全可能生下O型的子女。知道了血型的遗传规律,就可以从子女的血型表型来推断亲子关系。例如,AB型的人决不可能是O型子女的父亲。但必须注意的是,法医学上需要依据血型表型来判断亲子关系时,只能作为否定的参考依据,而不能据此作出肯定的的判断。由于血细胞上有许多种血型,测定血型的种类愈多,那么作出否定性判断的可靠性也愈高。
表3-7 ABO(H) 血型系统中的结构
| 表现型 |
遗传型 |
红细胞抗原 |
血清中天然抗体 |
| A |
A1A1 |
A+A1 |
抗B |
|
A10 |
|
|
| A2 |
A2A2 |
A+H |
抗B,10%的人有抗A1 |
|
A2O |
|
|
| B |
BB |
B |
抗A |
|
BO |
|
|
| AB |
AB |
A+A1+B |
--- |
| A2B |
A2B |
A+B+H |
25%的人有抗A1 |
| O |
OO |
H |
抗A及抗B |
新生儿的血液中还不具有ABO系统的抗体;在出生后的第一年中这种抗体才逐渐出现在血浆中,可以对抗自已血细胞上所没有的抗原。这类天然抗体多属IgM,其产生的原因尚未完全阐明,据推测,由肠道细菌所释放的物质或某些食物成分进入体内能够刺激血型抗体的产生。因为某些肠道具有与红细胞同样的抗原决定簇。
血型抗原在人群中的分布,在不同地域不同民族中是有差异的。以研究较多的ABO系统为例,在中欧地区人群中,40%以上为A型,稍低于40%为O型,10%左右为B型,6%左右为Ab 型;而在美洲土著民族中则90%属O型。在我国各族人民中ABO血型的分布也不尽相同。详见表3-8以了解各地域、各民族的血型分布规律,将有助于人类学研究各民族的来源和相互关系。
| 调查对象 |
调查人数(个) |
A |
B |
AB |
O |
| 人数(个) |
% |
人数(个) |
% |
人数(个) |
% |
人数(个) |
% |
| 汉族 |
40,980 |
12,831 |
31.31 |
11,501 |
28.06 |
4002 |
9.77 |
12,646 |
30.86 |
| 维吾尔族 |
1,513 |
441 |
29.22 |
483 |
31.92 |
172 |
11.36 |
416 |
27.50 |
| 壮族 |
1,487 |
316 |
21.25 |
410 |
25.57 |
58 |
3.90 |
703 |
47.28 |
| 回族 |
1,355 |
369 |
27.23 |
384 |
28.34 |
115 |
8.48 |
487 |
35.94 |
| 哈萨克族 |
885 |
202 |
22.82 |
264 |
29.83 |
83 |
9.38 |
336 |
37.97 |
| 锡伯族 |
344 |
86 |
25.00 |
138 |
40.12 |
36 |
10.46 |
84 |
24.42 |
| 乌孜别克族 |
129 |
33 |
25.58 |
50 |
38.76 |
13 |
10.08 |
33 |
25.58 |
| 柯尔克孜族 |
124 |
23 |
18.54 |
49 |
39.52 |
9 |
7.26 |
43 |
34.68 |
| 塔塔尔族 |
37 |
15 |
40.54 |
13 |
35.14 |
1 |
2.70 |
8 |
21.62 |
| 彝族 |
1007 |
288 |
28.60 |
303 |
30.09 |
82 |
8.14 |
334 |
33.17 |
| 白族 |
500 |
170 |
34.00 |
117 |
23.40 |
56 |
11.20 |
157 |
31.40 |
| 傣族 |
507 |
112 |
22.08 |
150 |
29.59 |
40 |
7.89 |
205 |
40.44 |
| 景颇族 |
201 |
70 |
34.83 |
41 |
20.39 |
14 |
6.97 |
76 |
37.81 |
| 佤族 |
520 |
200 |
38.46 |
112 |
21.54 |
73 |
14.04 |
135 |
25.96 |
| 土家族 |
960 |
362 |
37.71 |
219 |
22.81 |
61 |
7.19 |
310 |
32.29 |
上海生物制品研究所血型组:<<血型与血库>>第9页。上海人民出版社第1版1977年 湖南医学院生理教研组调查报告
3.ABO血型的检测正确测定血型是保证输血安全的基础。在一般输血中只有ABO系统的血型相合才能考虑输血。测定ABO系统的方法是:在玻片上分别滴上一滴抗B、一滴抗A和一滴抗A-抗B血清,在每一滴血清上再加一滴红细胞悬浮液,轻轻摇动,使红细胞和血清混匀,观察有无凝集现象(图3-10)。
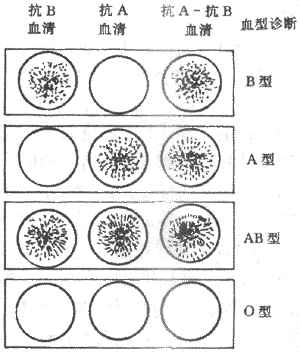
图3-10 ABO血型的测定
(二)Rh血型系统
1.Rh血型系统的发现和在人群中的分布在寻找新血型物质的探索中,当把恒河猴(Rhesus monkey)的红细胞重复注射入家兔体内,引起家兔产生免疫反应,此时在家兔血清中产生抗恒河猴红细胞的抗体(凝集素)。再用含这种抗体的血清与人的红细胞混合,发现在白种人中,约有85%的人其红细胞可被这种血清凝集,表明这些人的红细胞上具有与恒河猴同样的抗原,故称为Rh阳性血型;另有约15%的人的红细胞不被这种血清凝集,称为R h阴性血型,这一血型系统即称为Rh血型。在我国各族人中,汉族和其它大部分民族的人,属Rh阳性的约占99%,Rh阴性的人只占1%左右。但是在另一些少数民族中,Rh阴性的人较多,如苗族为12.3%,塔塔尔族为15.8%。
2.Rh血型系统的基因型及其表达利用血清试验提示了人类红细胞上的Rh血型系统包括着5种不同的抗原,分别称为C、c、D、E、e。从理论上推断,有3对等位基因Cc、Dd 、Ee控制着6个抗原。但实际上未发现单一的抗d血清,因而认为d是“静止基因”,在红细胞表面不表达d抗原。在5个抗原中,D抗原的抗原性最强。因此通常将红细胞上含有D抗原的,即称为Rh阳性;而红细胞上缺乏D抗原的,称为Rh阴性。
3.Rh血型的特点及其在医学实践中的意义前述ABO血型时曾指出,从出生几个月之后在人血清中一直存在着ABO系统的凝集素,即天然抗体。但在人血清中不存在抗Rh的天然抗,只有当Rh阴性的人,接受Rh阳性的血液后,通过体液性免疫才产生出抗Rh的抗体来。这样,第一次输血后一般不产生明显的反应,但在第二次,或多次再输入Rh阳性血液时即可发生抗原-抗体反应,输入的Rh阳性红细胞即被凝集。
Rh系统与ABO系统比较时的另一个不同点是抗体的特征。ABO系统的抗体一般是完全抗体IgM。而Rh系统的抗体主要是不完全抗体IgG,后者分子较能透过胎盘。因此,当阴性的母亲怀有阳性的胎儿时,阳性胎儿的小时红细胞或D抗原可以进入母体,通过免疫反应,在母体的血液中产生免疫抗体,主要是抗D抗体。这种抗体可以透过胎盘进入胎儿的血液,可使胎儿的红细胞民生凝集和溶解,造成新生儿溶血性贫血,严重时可致胎儿死亡。但一般只有在分娩时才有较大量的胎儿红细胞进入母体,而母体血液中的抗体浓度是缓慢增加的,一般需要数月的时间,因此,第一次妊娠常不产生严重反应。如果Rh阴性母亲再次怀有Rh阳性胎儿时,此时,母体血液中高浓度的Rh抗体将会透过胎盘,破坏大量胎儿红细胞。
三、白细胞与血小板血型
白细胞与血小板上与有A、B、H、MN、P等红细胞抗原,此外还有它们所特有的抗原,这些抗原具有临床意义,特别是组织兼容性抗原对选择器官组织的移植和血液成分的输注的合适供应者(donor)有重要意义。白细胞与血小板的抗原可使受者(recipient)产生免疫反应,这时,输血可引起发热反应,移植的器官组织受破坏的速度加快,在体内的生存期缩短。
人白细胞抗原( human leukocyte antigen,HLA)是人类白细胞上最强的同种抗原。HLA系统由数量众多的抗原所组成,是一个极为复杂的抗原系统,控制这些抗原的基因位于第6号染色体的短臂上,在这一部位的染色体上分布着A、B、C、D4个基因位点,它们控制着7组HLA抗原即:HLA-A、HLA-B、HLA-C、HLA-D、HLA-DR、HLA-DQ和HLA-DP,每一组又包括许多种抗原。例如HLA-A组有20多种抗原,HLA-B组有50种以上不同的抗原,HLA-C组则有11种抗原。根据抗原发现的顺序,又对抗原作编号,如HLA-A1、A2……A19等。它们的数量随着新抗原的认定还在继续扩大。
HLA是镶嵌在细胞膜上的糖蛋白,根据HLA的结构和分布特征,将它们分成两类:即I类和Ⅱ类抗原,HLA-A、B、C属I类抗原,分子量为56000,由一条重肽链和一条轻肽链所组成,它们的抗原特异性是由重肽链上氨基酸列所决定的。这类抗原总称 为I类抗原;它们除了分布在白细胞和血小板上,还广泛分布在各种正常组织器官和肿瘤组织的有核细胞膜上。其余的HLA抗原即D、DR、DP和DQ属于Ⅱ类抗原,分子量为63000,它们只分布在B细胞、巨噬细胞、单核细胞和内皮细胞上。
HLA系统除了在医学上与器官移植、植皮、骨髓移植和输轿有密切的关系外,还可应用于亲子鉴定和人类学研究。在应用于亲子鉴定时,由于HLA的数目极多,HLa –A和HLA-B相结合的形式极多,要有相同表现型的机会极少。例如,15个HLA-A和20个HLA-B能够产生20246种表现型。因此,在作亲子关系的否定判定时,HLA测定可过到90%以上的可靠性。各种HLA出现的频率具有明显的种族差异。例如,高加索人种中,HLA-A-A30和B42抗原的出现频率较其它人种为少,而在北美印地安人种,HLA-B51抗原出现频率较高。因此,HLA系统是人类学研究的一个重要指标。
血小板还有一些特有的抗原,如PI、Zw、Ko等系统,它们与红细胞或白细胞上的同种抗原没有关系。这些抗原可因输血和妊娠而产生免疫抗体。约有50%的病人在长期重复输注血小板后,在血清中可出现抗输入血小板的抗体。它们可引起发热反应,使输入的细胞缩短生存期,还以掩盖抗红细胞的特异抗体的存在,因而影响血型测定的正确性。当妊娠母亲血清中出现抗血小板抗体时,可导致新生儿血小板减少症。
四、输血的原则
输血已经成为治疗某些疾病、抢救伤员生命和保证一些手术得以顺利进行的重要手段。但是,由于输血发生差错,造成病人严惩损害,甚至死亡的事故并不鲜见。美国的统计资料报道,在1976年至1985年的10年间。美国共发生输血死亡事故159例,其中由于ABO系统的错误为137例,占86%。为了保证输血的安全性和提高输血的效果,必须注意遵守输血的原则。
随着医学和科学技术的进步,输血疗法已经从原来的单纯输全血,发展为输全血和成分输血(transfusion or blood components)。成分输血,就是把人血中的各种有效成分,如红细胞、粒细胞、血小板和血浆分别制备成高纯度或高浓度的制品再输入。这样既能提高疗效,减少不良反应,又能节约血源。
在准备输血时,首先必须保证供血者与受血者的ABO血型相合,因为这一系统的不相容输血常引起严重的反应。对于在生育年龄的妇女和需要反复输血的病人,还必须使供血者与受血者的Rh血型相合,以避免受血者在被致敏后产生抗Rh的抗体。
即使在ABO系统血型相同的人之间进行输血,在输血前必须进行交叉配血试验(corss-match test),即不仅把供血者的纸细胞与受血者的血清进行血清配合试验(这称为试验主侧);而且要把受血者的约细胞与供血者的血清作配合试验(这称为试验的次侧)。这样,既可检验血型测定是否有误,又能发现他们的红细胞或血清中,是否还存在一些其它的凝集原或凝集素,足以引起红细胞凝集反应。在进行并叉式配血试验时,应在37℃下进行,以保证可能有的凝集反应得以充分显示。
如果交叉配血试验的两侧都没有凝集反应,即为配血相合,可以进行输血;如果主侧有凝集反应,则为配血不合,不能输血;如果不侧不起凝集反应,而次侧有凝集反应,只能在应急情况下输血,输血时不宜太快太多,并密切观察,如发生输血反应,应立即停止输注。
以往曾经把O型的人称为“万能供血者(universal donor)”,认为他们的血液可以输给其他血液的人。但目前认为这种输血是不足取的,因为,虽然O型的红细胞上没有A和B凝集原,因而不会被受血者的血浆凝集,然而O型人的血浆中的抗A和抗B凝集素能与其它血型受血者的红细胞发生凝集反应。当输入的血量较大时,供血者血浆中的凝集素未被受血者的血浆足够稀释时,受血者的红细胞会被广泛凝集。
总之,输血是一个多环节的过程,每个环节上的失误都可能造成严重事故。因此,大进行输血操作时,必须严格遵守输血原则,密切注意观察;而且只在确实需要时才进行输血。决不可盲目滥用。
参考资料
1.吴祖泽主编,造血干细胞移植基础,第1-4章,北京,人民卫生出版社,1988
2.BrizziMF,Avauzi GC,Pegoraro L.Hematopoitic growth factor receptors.Int J Cell Cloning1991;9:274-300
3.Colman RW,Jack H ed.Hemostasisand Thrombosis 2nd ed,Churchill Livingstone,New York,1987
4.Dainiak N.Surfacemembrane-associated regulation of cell assembly,differentiation and growth.Blood 1991;78: 264-276
5.Dessypris EN,Krantz SB.Erythropoietin:regulation of erythropoiesis and clinical use .Adv Pharmacol1990;21:127-147
6.Harian JM.Leukocyte-endothelialinteractions.Blood 1985;65:513-526
7.Jandl JH.Blood-Testoodk ofHematology.Llttle,Brown Co,Boston,1978
8.Murphy MJ Jr ed.b Blood CellGrowth Factors.Alpha Med Press,Dayton ,1991
9.Pittilo RM,Machin SJed.Platelet-vessel Wall Interactions.Springer-Verlag,London,1988
10.Williams WJ, BeutlerE.Hematology 4th ed,McGraw-Hill Publishing Co,New York,1990