血液由有形成分红细胞、白细胞和血小板,以及无形的液体成分血浆(plasma)组成。血液凝固后析出淡黄色透明液体,称为血清(serum)。血清与血浆的区别在于血清中没有纤维蛋白原,但含有一些在凝血过程中生成的分解产物。
生理情况下,血液经血管在全身不断流动,转运各种物质与组织之间。血浆,组织间液以及其它细胞外液共同构成机体的内环境。因此血液在沟通内外环境,维持内环境的相对稳定(如pH、渗透压、各种化学成分的浓度等),物质的运输(营养物、代谢产物、代谢调节物),免疫防御及凝血与抗凝血作用等方面都起着重要作用。
第一节 血浆蛋白质
血浆蛋白是血浆中最主要的固体成分,含量为60~80g/L,血浆蛋白质种类繁多,功能各异。用不同的分离方法可将血浆蛋白质分为不同的种类。最初用盐析法只是将血浆蛋白分为白蛋白和球蛋白,后来用分段盐析法可细分为白蛋白、拟球蛋白、优球蛋白和纤维蛋白等组分。用醋酸纤维薄膜电泳法可分为白蛋白、α1球蛋白、α2球蛋白、β-球蛋白和γ-球蛋白等5条区带,而用分辨力较高的聚丙烯酰胺凝脉电泳法则可分为30多条区带。用等电聚焦电泳与聚丙烯酰胺电泳组合的双向电泳,分辨力更高,可将血浆蛋白分成一百余种。目前临床较多采用简便快速的醋酸纤维薄膜电泳法,所获得的血浆蛋白种类及正常含量见表10-1。
表10-1 血浆蛋白的种类、生成部位、主要功能和正常含量
| 血浆蛋白种类 |
生成部位 |
主要功能 |
正常含量 (克/100毫升血浆) |
|
| 白蛋白 |
肝脏 |
维持血浆渗透 压、运输、营养 |
|
| 3.8-4.8 |
|
| α球蛋白 |
α1球蛋白 |
主要在肝脏 |
运输 |
1.5-3.0 |
|
| α2球蛋白 |
|
| β球蛋白 |
大部分在肝脏 |
运输 |
|
| γ球蛋白 |
主要在肝外 |
免疫 |
|
| 纤维蛋白原 |
肝脏 |
凝血 |
0.2-0.4 |
|
近年来已知的血浆蛋白质有二百多种,有些蛋白质的功能尚未阐明。将其中主要的血浆蛋白质含量及功能归纳如表10-2。
表10-2 血浆蛋白各组分的名称、浓度及生物学活性
| 名称 |
符号 |
正常血浆中浓度(毫克/100毫升) |
生物学活性 |
| 白蛋白: |
| 前白蛋白 |
PA/Pre-AL |
28-35 |
结合甲状腺素 |
| 白蛋白 |
AIb |
4,200±700 |
维持血浆胶体渗透压、运输、营养 |
| α1球蛋白: |
|
|
|
| α脂蛋白(HDL) |
aLP |
217-270 |
磷酯、甘油三酯、胆固醇、脂溶性维生素的运输 |
| α1酸性糖蛋白 |
α1AGP |
75-100 |
又称乳清类粘蛋白、感染初期活性物质,抑制黄体酮 |
| α1抗胰蛋白酶 |
α1AT |
210-500 |
抗胰蛋白酶和糜蛋白酶 |
| 运钴胺素蛋白Ⅰ |
|
|
与维生素B12结合 |
| 运皮质醇蛋白 |
TSC |
5-7 |
运输皮质醇 |
| 甲胎蛋白 |
AFP |
0.5-2.0×10-3 |
? |
| α2球蛋白: |
| α2神经氨酸糖蛋白 |
C1s I |
24±10 |
抑制补体第一成分C1s |
| (C1s酯酶抑制物) |
|
|
酯酶的抑制物 |
| 甲状腺素结合球蛋白 |
TBG |
1-2 |
和甲状腺素(T4)结合 |
| α2HS糖蛋白 |
α2HS |
? |
炎症时被激活 |
| 铜兰蛋白 |
CP |
27-63 |
有氧化酶活性,与铜结合,参与铜的代谢,急性时权反应物 |
| 凝血酶原 |
|
5-10 |
参加凝血作用 |
| α2巨球蛋白 |
α2M |
200±60 |
抑制纤溶酶和胰蛋白酶,活化生长激纱和胰岛素,也可和其它低分子物质结合,急性时相反应物 |
| 胆硷酯酶 |
ChE |
1±0.2 |
水解乙酰胆碱 |
| 缚珠蛋白(结合珠蛋白) |
Hp |
100(30-190) |
和Hb结合 |
| 血管紧张素原 |
|
|
使血管收缩,升高血压;促进醛固 |
| 红细胞生成素 |
|
|
酮分泌促进RBC生成 |
| α2脂蛋白(VLDL) |
α2Lp |
28-71(随年龄性别而异) |
运输脂类(主要是甘油三酯)、脂溶性维生素和激素 |
| β球蛋白: |
| β脂蛋白(LDL) |
βLp |
219-340(随年龄性别而异) |
运输脂类(胆固醇、磷脂等)脂溶性维生素、激素 |
| 运铁蛋白 |
Tf |
250±40 |
运输铁、抗菌、抗病素 |
| 运血红素蛋白 |
Hpx |
80-100 |
与血红素结合 |
| C反应蛋白 |
CRP |
<1.2 |
与肺炎球菌的C多糖起反应 |
| 运钴铵素蛋白Ⅱ |
|
|
与维生素B12结合 |
| 纤溶酶原 |
Pm |
30±2 |
有纤溶酶活性 |
| 纤维蛋白原 |
Fib |
350(200-00) |
凝血因子Ⅰ,急性时相反应物 |
| γ球蛋白: |
| 免疫球蛋白A |
IgA |
247±87 |
抗体活性,分泌型抗体 |
| 免疫球蛋白D |
IgD |
3(0.3-40) |
抗体活性 |
| 免疫球蛋白E |
IgE |
0.033 |
反应素活性 |
|
|
(0.01-0.13) |
|
| 免疫球蛋白M |
IgM |
146±56 |
抗体活性 |
| 免疫球蛋白G |
IgG |
1280±260 |
抗体活性 |
血浆蛋白质多种多样,各种血浆蛋白有其独特的功能,除按分离方法分类外。目前亦采用功能分类法。可分为以下8类:①凝血系统蛋白质,包括12种凝血固子(除Ca2+外)。②纤溶系统蛋白质,包括纤溶酶原、纤溶酶、激活剂及抑制剂等。③补体系统蛋白质。④免疫球蛋白。⑤脂蛋白。⑥血浆蛋白酶抑制剂,包括酶原激活抑制剂、血液凝固抑制剂、纤溶酶抑制剂、激肽释放抑制剂、内源性蛋白酶及其他蛋白酶抑制剂。⑦载体蛋白。⑧未知功能的血浆蛋白质。
血浆蛋白质具有以下共同特征:
1.血浆蛋白质绝大部分由肝脏合成。除γ球蛋白由浆细胞合成,内皮细胞合成少量血浆蛋白质外。
2.血浆蛋白质为分泌型蛋白质。在与肉质网结合的多核糖体(pllyribosome)上合成,分泌入血浆前经历了剪切信号肽、糖基化、磷酸化等翻译后修饰加工过程,成为成熟蛋白质。
3.血浆蛋白质几乎都是糖蛋白,含有N-或O-连接的寡糖链。仅白蛋白、视黄醇结合蛋白和C-反应蛋白等少数不含糖。糖链可参与血浆蛋白分子的三级结构的形成,具有多种功能。
4.各种血浆蛋白质都具有其特征性的循环半衰期。
5.许多血浆蛋白质有多态性(polymorphism)。多态性指在同种属人群中,有两种以上,发生频率不低于1%的表现型。最典型的是ABO血型物质。此外,α1抗胰蛋白酶、结合珠蛋白、铁转运蛋白、血浆铜蓝蛋白等都显示多态性。研究血浆蛋白多态性对遗传学及临床医学均有重要意义。
6.当急性炎症或组织损伤时,某些血浆蛋白水平增高。这些血浆蛋白被称为急性期蛋白质(acute phaseprotein)。包括C?反应蛋白(CRP)、α1抗胰蛋白酶、α2酸性糖蛋白及纤维蛋白原等。急性期蛋白在人体炎症反应中发挥一定作用。
血浆蛋白的主要功能可归纳为以下几个方面:
1.维持血浆胶体渗透压。主要靠血浆白蛋白,因其含量多而分子小,血浆胶体渗透压的75~80%由它维持。
2.调节血浆pH值,维持酸碱平衡。血浆蛋白的等电点大部分在pH4~6,血浆中蛋白多以负离子形式存在,以

(Pr表示血浆蛋白)形式构成血浆中的缓冲对。
3.运输 血浆蛋白中许多组分具有运输功能,可送输营养物质、代谢物、激素、药物及金属离子等。
4.凝血和抗凝血作用。各种凝血因子及抗凝血因子在减少出血,防止循环阻塞中发挥重要作用。
5.免疫作用,抵御感染。主要靠抗体和补体系统发挥作用。
一、白蛋白
人血浆白蛋白(albumin)是人血浆含量最多的蛋白质,约45g/L,占血浆总蛋白的60%。肝脏每天合成12g白蛋白,占肝脏分泌蛋白的50%。人血浆白蛋白基因位于第4号染色体上,其初级翻译产物为前白蛋白原(preproalbumin)。在分泌过程中切除信号肽,生成白蛋白原(proalbumis)。继而在高尔基氏体经组织蛋白酶B切除N末端的一个6肽片断(精-甘-缬-苯丙-精-精),成为成熟的白蛋白。由585个氨基酸组成的一条多肽链,含17个二硫键,分子量约为69,000。白蛋白的分子呈椭园形,其长短轴分别为150?和38?,较球蛋白和纤维蛋白原分子对称,故白蛋白粘性较低。白蛋白等电点为pH4.7,比血浆蛋白其他组分的PI低,所以在常用的弱碱性电泳缓冲液中所带负电荷多,加之分子量小,故电泳迁移速度快。
血浆白蛋白主要有两方面生理功能:①维持血浆胶体渗透压。因血浆中白蛋白含量最高,且分子量较小,故血浆中它的分子数最多。因此在血浆胶体渗透压中起主要作用,提供75-80%的血浆总胶体渗透压。②与各种配体(ligands)结合,起运输功能。许多物质如游离脂肪酸、胆红素、性激素、甲状腺素、肾上腺素、金属离子、磺胺药、青霉素G、双香豆素、阿斯匹林等药物都能与白蛋白结合,增加亲水性而便于运输。
二、金属结合蛋白
1.结合珠蛋白(haptoglobin;Hp)是一种血浆糖蛋白,分子量约为90.000。能与红细胞外血红蛋白(Hb)结合形成紧密的非共价复合物Hb-Hp。每100ml血浆中具有足以结合40?80mg血红蛋白的Hp。每天降解的Hb约有10%释入血循环中,成为红细胞外游离的Hb,Hb与Hp结合成Hb-Hp复合物后分子量可达155.000,不能透过肾小球,从而防止游离血红蛋白从肾脏丢失,避免Hb所含铁的丢失。保证铁再用于合成代谢。
溶血性贫血患者血浆结合珠蛋白浓度下降。由于溶血时大量的Hb释出,Hp与游离Hb结合成复合物而被肝细胞摄取、清除。此外,Hp也是一种急性期蛋白,患各种炎症时其血浆中含量升高。
2.铁转运蛋白(transferrin;Tf) 铁转运蛋白属β球蛋白。是由肝脏内合成的糖蛋白,分子量约80.000。具高度多态性,目前已发现20多种不同类型的Tf。每分子Tf可结合2分子的Fe3+。铁转运蛋白的生理功能是将铁运送到需要铁的组织与细胞。每天血红蛋白分解代谢,释出25mg左右的铁。游离铁有毒性,它与Tf结合后不仅毒性降低而且还将铁运送到需铁部位。铁是许多含铁蛋白质生物活性的发挥所必不可少的,如血红蛋白、肌红蛋白、细胞色素、过氧化物酶等。因此,任何生长、增殖细胞的膜上都有铁转运蛋白的受体。携带Fe3+的Tf与受体结合后经内吞作用进入细胞内,供细胞内合成利用。
三、铜蓝蛋白(ceruloplasmin;Cp)
铜蓝蛋白(ceruloplosminCp)属α2球蛋白。也是由脏脏合成的一种糖蛋白、分子量为160,000,由8个分子量1.8万的亚基组成。每分子Cp可牢固地结合6个铜离子,并因携铜而呈蓝色。Cp除作为铜的载体外,还具有氧化酶的活性,可将Fe2+氧化为Fe3+,利于铁掺入铁转运蛋白,促进铁的运输。
正常人体内含铜约100?50mg,主要位于骨、脏脏和肌肉中。血浆中的铜90%由Cp转运,10%与白蛋白结合而送输。成人每日摄取铜2mg,主要在小肠上段吸收,同白蛋白结合送输到肝,即掺入肝细胞合成Cp。部分铜可从胆汁中排出。肝病时铜蓝蛋白合成减少,血浆Cp含量降低。肝豆状核变性(wilso病)是一种遗传病,可能因为肝细胞溶酶体不能将来自铜蓝蛋白的铜排入胆汁,导致铜在肝、肾、脑及红细胞中聚积,发生铜中毒。肝中铜含量增加,抑制铜和Cp结合,血中Cp含量下降(<20mg/dl)。可出现溶血性贫血、慢性肝病,以及神经系统症状。由于角膜内铜的沉着,在角膜周围出现绿色或金黄色的色素环,称为Kayse?Fleischer环,是肝豆状核变性的一种特征性改变,具有诊断价值。减少铜摄入,服用D青霉胺鳌合铜离子,可对肝豆状核变性进行治疗。
第二节 血液凝固
血液的可凝固性质对机体有重要保护作用。当血管系统受伤时,必须迅速可靠地封闭起来,以尽可能减少出血。血小板变形(粘性变态)参于封闭作用,此种封闭作用要靠纤维蛋白凝结物的支持,而后者的形成是多种凝血因子相互作用,发生一系列酶促反应的结果。目前已发现的凝血因子有14种(表10-3)。
这些凝血因子除Ca2+外均为蛋白质,大多是由肝脏合成的血浆糖蛋白,它们大多属蛋白水解酶类。有7种为蛋白酶原,在凝血过程中被激活。无活性的凝血因子用罗马数码表示,其活性型以附加的下角码a字来表示。
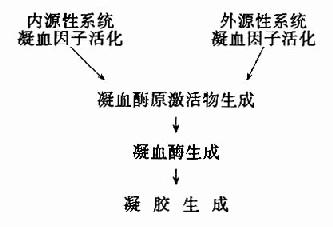
图10-1 血液凝固过程
一、血液凝固的机理
血液凝固的化学本质是溶胶状态的纤维蛋白原转变为凝胶状态的纤维蛋白,催化此反应的主 要是凝血酶。而正常血液中以无活性的凝血酶原形式存在,在一定条件下被激活而成为凝血酶。凝血酶原激活物是由活化的凝血固子与磷脂胶粒和钙形成的复合物。因此,凝血因子的活化是导致血液凝固的触发机制。据触发凝血过程的方式不同,又有内源性(intrinsic)与外源性(extrinsic)凝血之分。内源性凝血指因心血管内膜受损或血液抽出体外接触异物表面而触发的,仅有血管内凝血因子参与的凝血过程;而外源性凝血则指有受损组织释放的组织凝血活素所参与的凝血过程。血液凝固过程的梗概可图解如下:(图10-1)
二、凝血酶原激活物的生成
凝血酶原激活物由活化的凝血因子Xa、Va、Ca++及磷脂胶粒构成的复合体。因子X被激活为Xa是此过程的关键步骤。因子X的激活有两条途径:即内源性和外源性途径。
表10-3 凝血因于命名及其部分特性
| 凝血因子 |
同义名 |
合成场所 |
分子量 |
亚基数目 |
含糖量% |
血浆浓度mg% |
衍生物 |
功能 |
| Ⅰ |
纤维蛋白原(Fibrinogen) |
肝 |
340,000(人,牛) |
3×2 |
3-4 |
200-400 |
纤维蛋白 |
形成凝胶 |
| Ⅱ |
凝血酶原(Prothrombin) |
肝 |
68,700(人) 72,000(牛) |
1 |
8.2(人) 10-14(牛) |
10-15 |
凝血酶 |
蛋白酶 |
| Ⅲ |
组织凝血活素(Tissue Thromboplastin) |
各组织细胞 |
330,00 220,000(牛) |
|
|
|
|
辅因子 |
| Ⅳ |
钙离子(Calcium Ion) |
|
|
|
|
|
|
辅因子 |
| Ⅴ |
前加速素(Proaccelerin) |
肝 |
290,000-400,000 |
多聚 |
11-18 |
5-10 |
Ⅳ(Va) |
辅因子 |
| Ⅶ |
血清凝血活酶转变加速素(Convertin)又称SPCA) |
肝 |
63,000(人) |
1 |
9.1 |
0.4-0.7 |
Ⅶa |
蛋白酶 |
| Ⅷ |
抗甲种箇以病球蛋白(Antihemotpilic Globulin简写AHG) |
肝为主 |
1,100,000(人,牛) |
? |
6(人) 9(牛) |
15-20 |
Ⅷa |
辅因子 |
| Ⅸ |
血浆凝血活素成分(Plasma Thromboplastin简写PTC)又名抗乙种血友病因子 |
肝 |
55,400(人,牛) |
1 |
26 |
3-5 |
Ⅸa |
蛋白酶 |
| Ⅹ |
Stuart-Prower因子 |
肝 |
55,000(人,牛) |
1 |
10 |
5-10 |
Ⅹa |
蛋白酶 |
| Ⅺ |
血浆凝血活素前质(Plasma Thro mboplastin Antecedent简写PTA)又名抗丙种血友病因子 |
肝?网状内皮系统? |
160,000(人,牛) |
2 |
12 |
0.5-0.9 |
Ⅺa |
蛋白酶 |
| Ⅻ |
接因子(Hageman因子) |
网状内皮系统? |
90,00(牛) 82,000(人) |
3 |
15 |
0.1-0.5 |
Ⅻa |
蛋白酶 |
| XⅢ |
纤维蛋白稳定因子(Fibrin Stabilizing Factor简写FSK) |
血水板?肝? |
320,000(血浆) 146,000-165,000 (血小板) |
5(血浆) |
1-2 |
Ⅻa |
形成桥键 |
|
|
前激肽释放酶(Prekallidrein) |
肝 |
80,000 |
1 |
10 |
1-2 |
激肽释放酶 |
蛋白酶 |
|
高分子量激肽原(High Molecular Weight Kininogen HMWK) |
|
110,000-15,000 |
1 |
? |
7 |
缓激肽 |
辅因子 |
罗马数字后的a表示活化的意思(activated),因子Ⅵ实际上就是Ⅴa。
(一)内源性途径
内源性途径涉及多种凝血因子活化,可分为二步:
1.接触活化 是因子Ⅻ,也称Hagemann?因子的激活作用。此蛋白质在接触到荷负电的表面,如玻璃或在体内接触到胶原蛋白时,发生构象改变,激活的因子Ⅻa为一蛋白酶,能将激肽释放酶原转变为激肽释放酶,又可活化因子Ⅻ,形成一个正反馈。同时因子Ⅻa还可激活下一个因子Ⅺ,将它转变为Ⅺa。此外,在Ⅻ因子活化中还有高分子量激肽原(high molecular weightkininogen,HMWK)的参与(图10-2)。
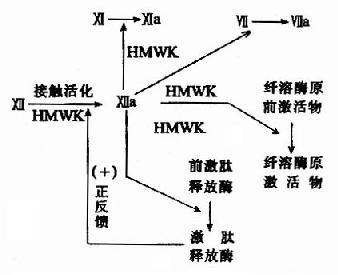
图10-2 内源性凝血的接触活化阶段
2.磷脂胶粒反应阶段:活化的Ⅻ即Ⅻa作用于因子Ⅺ,在Ca++的存在下水解因子Ⅺ产生Ⅺa,因子Ⅺa无酶活性,但可使因子X的活化反应速度提高1000倍。活化的因子X(即Xa)及凝血酶都有激活因子Ⅷ和Ⅴ的作用。活化的因子Xa、Va和Ca++结合在磷脂胶粒上形成凝血酶原激活物。磷脂胶粒是由血小板提供的富含丝氨酸磷脂的脂蛋白,对凝血因子和Ca++有较强的亲和力,从因子Ⅺ的活化到凝血酶原激活物的生成一系列反应均在磷胶胶粒上进行,故称磷脂胶粒反应阶段。(图10-3)
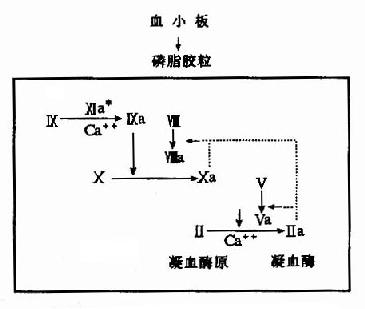
图10-3 内源性凝血的磷脂胶粒反应阶段
(*主要在外源性凝血中起作用因子Ⅶa亦可使因子活化·虚线……示正反馈回路)
(二)外源性途径
组织损伤后释放因子Ⅲ(组织凝血活素),它是一种脂蛋白,在脑、肺、胎盘等组织中含量最丰富,它的磷脂部分类似血小板所提供的磷脂胶粒,能把血浆中凝血因子Ⅶ和X通过Ca++桥而结合在其表面上。因子Ⅶ可由Ⅻa和凝血酶激活、亦可被Xa激活、Ⅶa可激活因子X产生Xa,而组织凝血活素的蛋白部分可使此反应加速16,000倍。未活化的因子Ⅶ也具有催化作用,但仅有Ⅶa的2%(图10-4)。
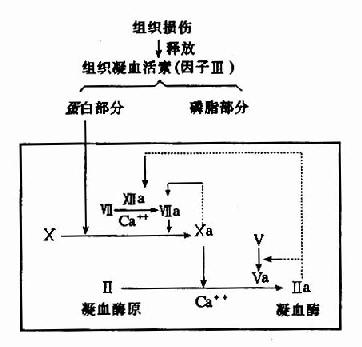
图10-4 外源性凝血中凝血酶原激活物的生成及凝血酶生成(虚线示正反馈回路)
三、凝血酶原的激活
凝血酶原(Ⅱ,prothrombin)是含582氨基酸残基的酶原,被因子Xa在Arg-Thr及Arg-Ile处切开,切除N?端274个氨基酸残基,余下308个氨基酸残基分成A、B两条肽链,由一个二硫键相连,即为凝血酶(thrombin)。(图10-5)因子Va无酶活性,但可使Xa的活性增强350倍,加速凝血酶的生成。磷脂胶粒与酶(Xa)和底物(凝血酶原)之间借Ca++作为桥相连。因凝血酶原肽链的N?未端含有10个γ?羧基谷氨酸残基。相邻的羧基可与Ca++形成复合体。另一方面,Ca++又可与磷脂中磷酸基结合,这样使Xa和Va与凝血酶原接触在一起,于是Xa将凝血酶原水解为凝血酶(图10-6)。
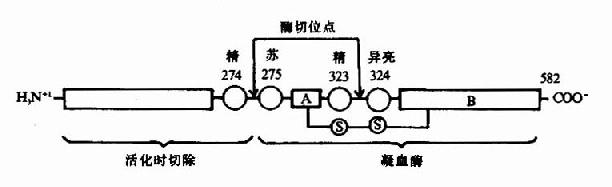
图10-5 因子Xa激活凝血酶原示意图
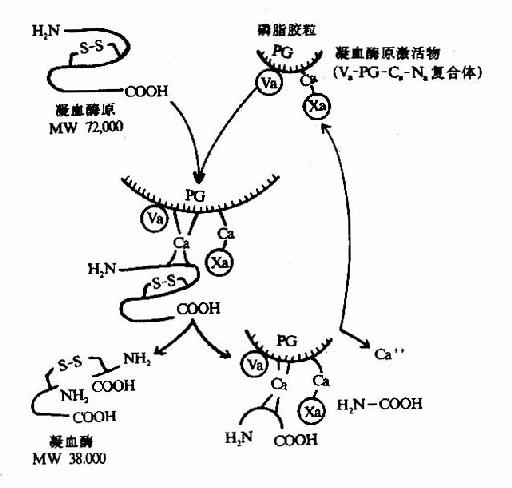
图10-6 凝血酶的生成
凝血酶原及因子Ⅶ、Ⅺ、Ⅹ均由肝合成,合成过程中需要维素K作为辅因子。缺乏Vitk则生成异常凝血酶原,只有正常活性的1?%。研究表明Vitk参与凝血酶原γ?羧基谷氨酸的生成。Vitk参与羧基化的机理为:氢醌型Vitk在酶的催化下夺去γ?C上的一个质子,使γ-C呈阴离子,而和CO2结合。2,3?环氧Vitk则在酶催化下被硫辛酸还原而重复利用,因而Vitk在此羧化反应中起辅酶的作用。(图10-7)
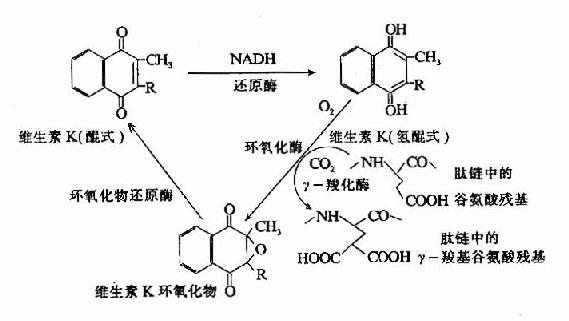
图10-7 维生素K在谷氨酸残基r-羧化反应中的作用(维生素K循环)
四、纤维蛋白原转变为纤维蛋白
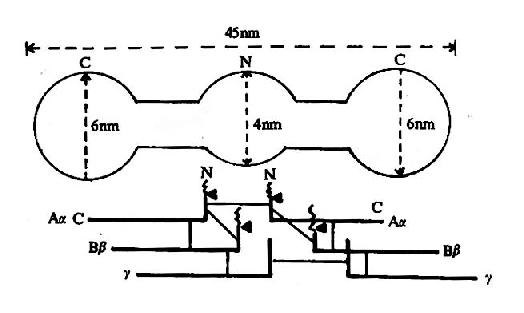
图10-8 纤维素蛋白原分子示意图
上半为电镜下的分子形状 下半示6条多肽链,
一为双硫键,▲为凝血酶作用点
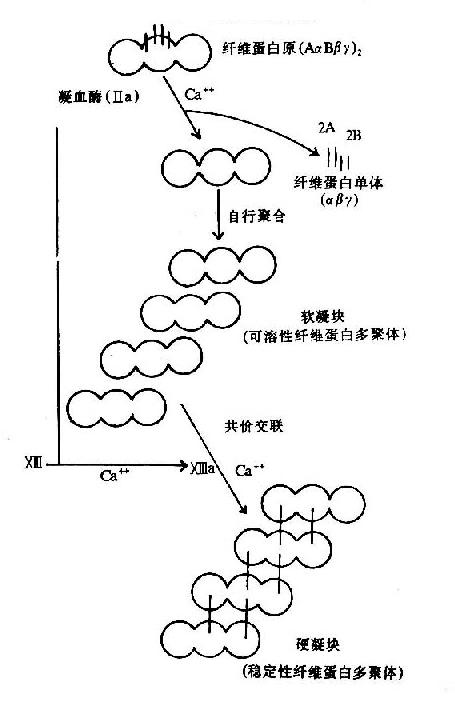
图10-9 纤维素蛋白凝胶的生成
血液凝固的实质是纤维蛋白凝胶的生成,它是血浆中纤维蛋白原(fibrinogen)在凝血酶作用下降解为纤维蛋白并聚合成不溶性的网状结构。
纤维蛋白原分子由两对α?链、β-链及γ-链组成,每3条肽链(α、β、γ)绞合成索状,形成两条索状肽链,在N末端有二硫键使态个分子得到稳定。α及β肽链的N-端分别有一段16个及14个氨基酸的小肽,称为纤维肽A及B。因此,纤维蛋白原可写为(AαBβγ)2(图10-8)。
凝血酶的本质为一种蛋白水解酶,能特异性作用于Aα和Bβ链上的精-甘肽键。切除A、B纤维肽。因纤维肽A及B均为酸性肽,带较多负电荷。由于电荷排斥作用阻碍纤维蛋白原之间聚合。切除纤维肽A及B转变为纤维蛋白后负性减小,同时暴露了互补结合位点,有利于自动聚合,纤维蛋白单位通过边靠边、端靠端的聚合形成聚合链。此种多聚体不稳定,称为软凝块(soft clot)。它再通过因子XⅢa的作用结成牢固的网。因子XⅢa为转肽酶,能催化一个单体的谷氨酸残基的γ-羧基与另一单体的赖氨酸残基的氨基之间形成共价结合,其间释出NH3(图10-9,10)。因此,因子XⅢa称为纤维蛋白稳定因子(fibrin stabilizingfactor,FSF)。因子XⅢ存在于血小板及血浆中,经凝血酶切除部分肽段后被激活为XⅢa。
由此产生的稳定纤维蛋白网与软凝块不同,它们在5M的脲及1%氯乙酸溶液中不溶解。在血小板的血栓收缩蛋白作用下,此网状结构收缩,于是伤口边缘彼此靠近,易于伤口闭合。成纤维细胞的表面带有一种类似纤维蛋白的蛋白质,称粘连蛋白,它由Ⅻa催化与纤维蛋白结成网。并将纤维蛋白固定下来。所以,因子Ⅻa还直接参与伤口的愈合。
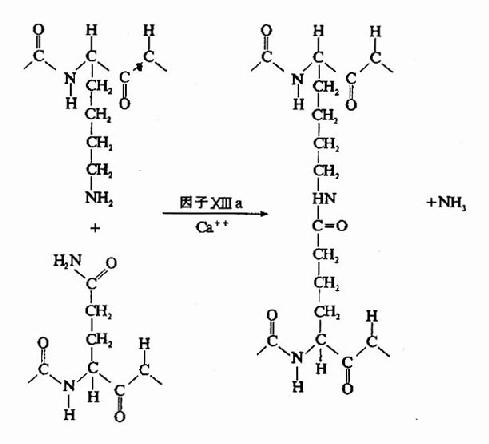
图10-10 因子XⅢa作用机理
总结上述凝血过程可归纳出以下特点:
1.凝血因子的活化本质上为蛋白质的有限水解,而许多凝血因了本身既是蛋白酶,又是酶作用的底物。这些本质为蛋白酶的凝血因子(Ⅱ、Ⅵ、Ⅺ、Ⅹ、Ⅻ)的氨基酸顺序很相似,与许多丝氨酸蛋白酶同源;活性中心的丝氨酸残基参与肽键的水解。C-端约250个氨基酸残基同源性很高,是具有催化活性的结构域。而N?端的氨基酸序列变化较大,决定各凝血因子作用底物的专一性。它们催化的反应需Ca++和磷脂参加。
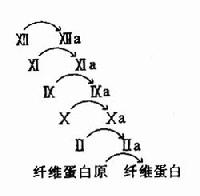
图10-11 血液凝固的瀑布效应
2.磷脂胶粒(内源性途径由血小板,外源性途径由组织凝血活素提供)使活化反应在胶粒表面进行,大大提高反应速度,而Ca++的作用在于促进酶和底物与磷脂表面的结合。
3.凝血因子活化呈瀑布效应(cascade)使血液凝固具有高效率和精密调控的特征。如图10-11所示。
4.维生素K在内、外源性凝血中均有重要作用。
5.凝血过程中的正反馈使反应不断加速,但终产物纤维蛋白有抗凝血作用。机体内凝血与抗凝血是密切联系的。
五、凝血作用的调节
由上所述,凝血过程是一个级联放大的瀑布效应,加之正反馈作用,可把最初生成的酶活性极大增强,把所有步骤加起来可增强106倍。如此高的激活速度会对机体构成危险,就是说,此过程一旦启动,整个血液就会凝固起来。此外,血凝可造成心肌梗死、脑血栓等严重疾病。因此,机体内的凝血作用必须保持适度。实事上,血浆及血管内皮等处存在着多种抗凝物质,凝血过程中生成的纤维蛋白(抗凝血酶Ⅰ)有强烈吸附凝血酶的作用。血浆中抗凝血蛋白(antithrombin抗凝血酶Ⅲ)是一种分子量约58,000的糖蛋白,能与具有蛋白酶作用的凝血因子(Ⅱa、IXa、Xa、Ⅺa、Ⅻa)以1:1分子比结合形成复合物,从而封闭酶的活性中心。肝素(heparin)能加速复合体的形成,使抗凝血酶的活性提高数百倍。肝素是由肥大细胞和嗜碱性粒细胞产生的高分子酸性粘多糖,是一种重要抗凝血物质、除上述作用外,尚具有抑制血小板的粘附、集聚,从而影响血小板磷脂的释放等作用。肝素作为抗凝剂已广泛应用于临床。
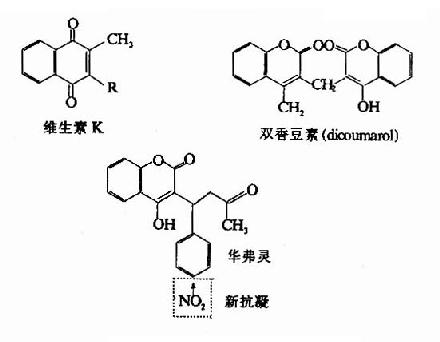
图10-12 几种抗凝物质结构
血浆中还存在另一种抗凝血的蛋白质桟蛋白。含Gla残基,是分子量约62,000的糖蛋白,以酶原形式存在,被凝血酶激活后能水解Ⅴa及Ⅶa,从而发挥抗凝血功能。先天性缺乏C蛋白者,往往在婴儿期即死于广泛的血栓。
除天然存在于血浆中的抗凝物质外,临床上常用一些人工抗凝剂如草酸盐和柠檬酸盐,它们的作用是通过螯合去除Ca?。此外还有双香豆素类化合物能拮抗Vitk,而发挥抗凝血作用(图10-12)。
六、纤维蛋白溶解
血液凝固所产生的纤维蛋白可被血浆中纤维蛋白溶酶系统重新溶解,对于防止血栓形成和保持血流通畅具有重要意义。正常人的一些分泌液(如乳汁、唾液、泪液、子宫及阴道分泌物、精液等)中均含有纤维蛋白溶酶原(plasminogen)激活物,激活纤维蛋白溶解过程,随时清除分泌管道内的纤维蛋白,以保持分泌管道的通畅及月经血液的流动性。
(一)纤维蛋白溶解机理
纤维蛋白溶解(fibrinolysis)过程可分为二相,即纤维蛋白酶原激活和纤维蛋白溶解。
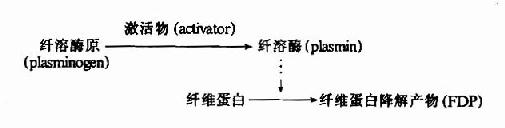
1.纤维蛋白酶原的激活
(1)纤维蛋白酶原激活物:
血液中纤维蛋白酶(plasmin,简称纤溶酶)以纤溶酶原形式存在,只有在纤溶激活物作用下转变为纤溶酶才具有活性。纤溶激活物可分为组织激活物和血液激活物两大类。
组织激活物主存在于组织细胞溶酶体中,以子宫、前列腺、甲状腺、肺、肾等含量较多。其中研究的最好的是肾中的尿激酶(urokinase),因其可少量出现在尿液中而得名。对肾小管血栓的溶解具有重要作用。
血液激活物主要来自静脉、微静脉的血管内皮细胞。在受到某些刺激(如剧烈运动、情绪紧张、创伤、休克等)时,可促使内皮细胞合成增多并释放入血。已知血小板释放5桯T对血管内皮细胞释放纤溶激活物具有重要意义。
此外,由溶血性链球菌提取的一种蛋白质称为链激酶(streptokinase),能与纤溶酶原形成复合物,后者具有纤溶激活物的性质。尿激酶和链激酶目前已广泛应用于临床溶栓治疗。
(2)纤溶酶原的激活
纤溶酶原为分子量86,000的蛋白。纤溶激活物均为蛋白水解酶,能水解纤溶酶原使之在肽链的Arg?Val间切断而活化生成纤溶酶。纤溶酶本身亦可活化纤溶酶原,同时还可水解纤维蛋白原、因子Ⅴ、Ⅶ、IX和Ⅻ等,从而抑制凝血。
2.纤维蛋白的溶解
纤维蛋白的溶解过程是分步进行的,首先被纤溶酶水解释出A、B、C小分子多肽,留下X片段仍保留凝固特性。X片断进一步水解为片断D和Y,Y再水解为D和E片断。(图10?13)最终分解产物为A、B、C、D、E五种片段。这些片断统称为纤维蛋白降解产物(fibrin degradationproduct,FDP)。FDP的生理作用是:片断X,Y可与纤维蛋白单体聚合,抑制多聚体的生成;片断D可直接抑制纤维蛋白单体的聚合;片断Y、E则可竞争抑制凝血酶。而且,大部分FDP可干扰血小板的粘附、聚集。可见FDP在抗凝中有重要作用。
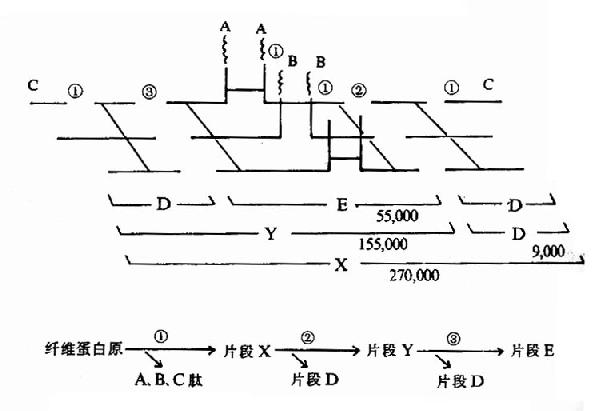
图10-13 纤溶酶对纤维蛋白(原)的降解(片段下的数字为分子量)
(二)纤溶抑制物
机体组织和体液广泛存在纤溶抑制物。按其作用可分为:纤溶酶原激活的抑制物;纤溶酶抑制物,又称抗纤溶酶(antiplasmin)。
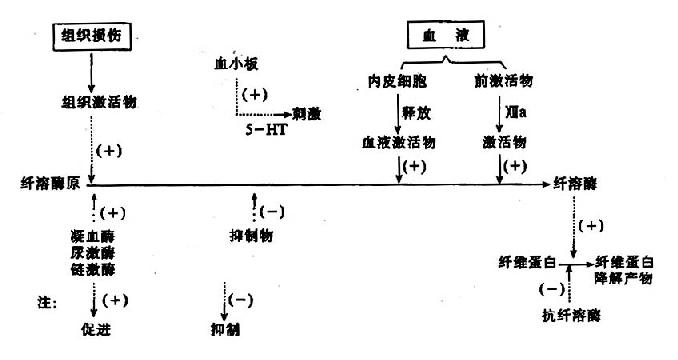
图10-14 纤维蛋白溶解过程
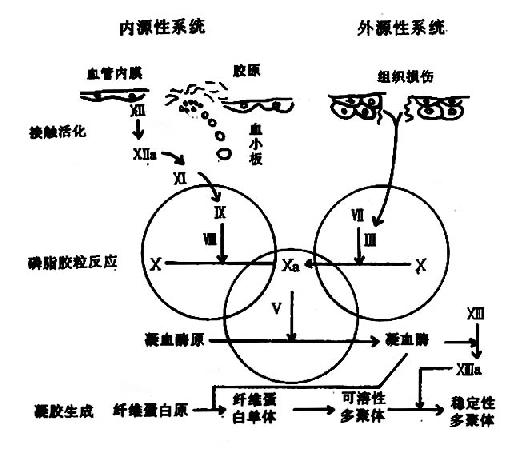
图10-15 凝血全过程示意图(→示转变或释放;→示催化作用;
除接触活化阶段外,均需Ca++参与,图中未显示)
正常血液中抗纤溶酶活性是纤溶酶活性的20?0倍。故在生理条件下,纤溶酶难以发挥作用。抗纤溶酶有两种:①慢作用的抗纤维酶,属α1抗胰蛋白酶,分子量为45,000,可与纤溶酶形成牢固的复合物。②快作用抗纤溶酶,属α2巨球蛋白,分子量80,000,是纤溶酶的竞争抑制剂。
血小板中纤溶抑制物是快速作用的抗纤溶酶。在血栓形成早期,血小板纤溶抑制作用大于纤溶激活作用;在血栓生成以后,随着血小板内5桯T的释放,则血管内皮释放血液激活物增多,又引起纤维蛋白溶解,防止血栓继续增长而阻塞血流循环。
因此可见机体内血液凝固、抗凝、纤溶与抗纤溶是相互抑制、相互协调、共同维护血液系统的正常生理功能,其相互关系可见图10-14~17。
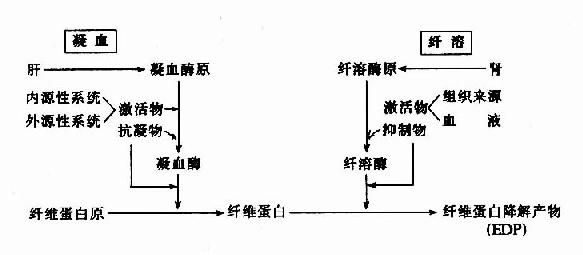
图10-16 凝血与纤溶的比较
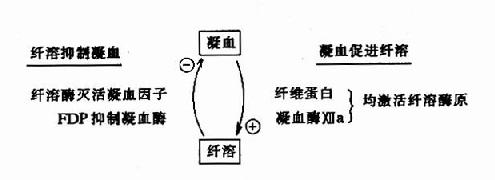
图10-17 凝血与纤溶的相互关系
第三节 红细胞的代谢
一、血红素的生物合成
成熟红细胞中,血红蛋白(hemoglolin,Hb)占红细胞内蛋白质总量的95%,它是血液运输O2的最重要物质,和CO2的送输亦有一定关系。血红蛋白是由4个亚基组成的四聚体,每一亚基由一分子珠蛋白(globin)与一分子血红素(heme)缔合而成。由于珠蛋白的生物合成与一般蛋白质相同,因此本节重点介绍血红素的生物合成。
血红素也是其它一些蛋白质,如肌红蛋白(myoglobin),过氧化氢酶(catalase),过氧化物酶(peroxidase)等的辅基。因而,一般细胞均可合成血红素,且合成通路相同。在人红细胞中,血红素的合成从早动红细胞开始,直到网织红细胞阶段仍可合成。而成熟红细胞不再有血红素的合成。
(一)血红素的合成通路(过程)
血红素合成的基本原料是甘氨酸、琥珀酰辅酶A及Fe++。合成的起始和终末过程均在线粒体,而中间阶段在胞液中进行。合成过程分为如下四个步骤:
1.δ-氨基-γ-酮戊酸(δ-aminplevulinicacid,ALA)的生成:在线粒体中,首先由甘氨酸和琥珀酰辅酶A在ALA合成酶(ALa synthetase)的催化下缩合生成ALA。ALA合成酶由两个亚基组成,每个亚基分子量为60,000。其辅酶为磷酸吡哆醛。此酶为血红素合成的限速酶,受血红素的反馈抑制。
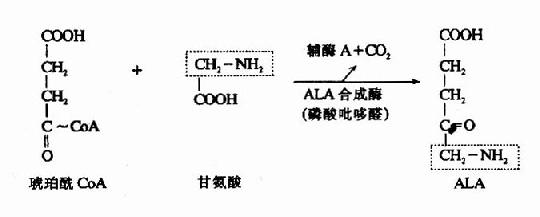
2.卟胆原的生成:线粒体生成的ALA进入胞液中,在ALA脱水酶(ALa dehydrase)的催化下,二分子ALA脱水缩合成一分子卟胆原(prophobilinogen,PBG)。ALA脱水酶由八个亚基组成,分子量为26万。为含巯基酶。
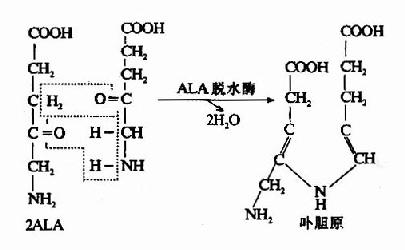
3.尿卟啉原和粪卟啉原的生成:在胞液中,四分子PBG脱氨缩合生成一分子尿卟啉原Ⅲ(uroporphyrinogen Ⅲ,UPG Ⅲ)。此反应过程需两种酶即尿卟啉原合酶(uroporphyrinogen synthetase)又称卟胆原脱氨酶(PBGdeaminase)和尿卟啉原Ⅲ同合酶(uroporphyrinogenⅢ cosynthase)。首先,PBG在尿卟啉原合酶作用下,脱氨缩合生成线状四吡咯。再由尿卟啉原Ⅲ同合酶催化,环化生成尿卟啉原Ⅲ。无尿卟啉原Ⅲ同合酶时,线状四吡咯可自然环化成尿卟啉原Ⅰ(UPG-Ⅰ),两种尿卟啉原的区别在于:UPGⅠ第7位结合的是乙酸基,第8位为丙酸基;而UPg Ⅲ则与之相反,第7位是丙酸基,第8位是乙酸基。正常情况下UPG-Ⅲ与UPG-Ⅰ为10000:1。
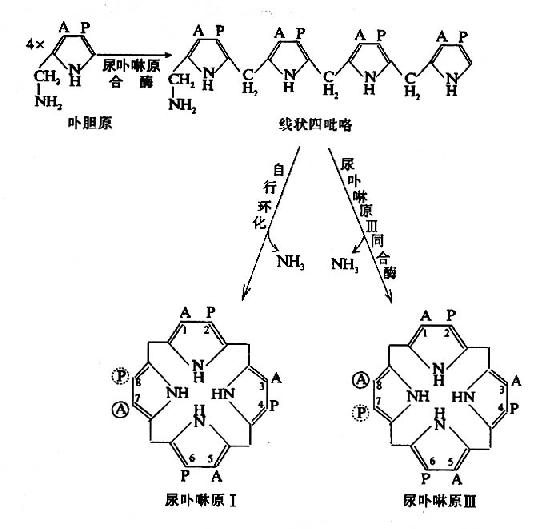
式中A代表乙酸基,P代表丙酸基
尿卟啉原Ⅲ进一步经尿卟啉原Ⅲ脱羧酶催化,使其四个乙酸基(A)脱羧变为甲基(M),从而生成粪卟啉原Ⅲ(coproporphyrinogen Ⅲ,CPG Ⅲ)。
4.血红素的生成:胞液中生成的粪卟啉原Ⅲ再进入线粒体中,在粪卟啉原氧化脱羧酶作用下,使2、4位的丙酸基(P)脱羧脱氢生成乙烯基(V),生成原卟啉原IX。再经原卟啉原IX氧化酶催化脱氢,使连接4个吡咯环的甲烯基氧化成甲炔基,生成原卟啉IX。最后在亚铁螯合酶(ferrochelatase)催化下和Fe2+结合生成血红素。(图10-18)。
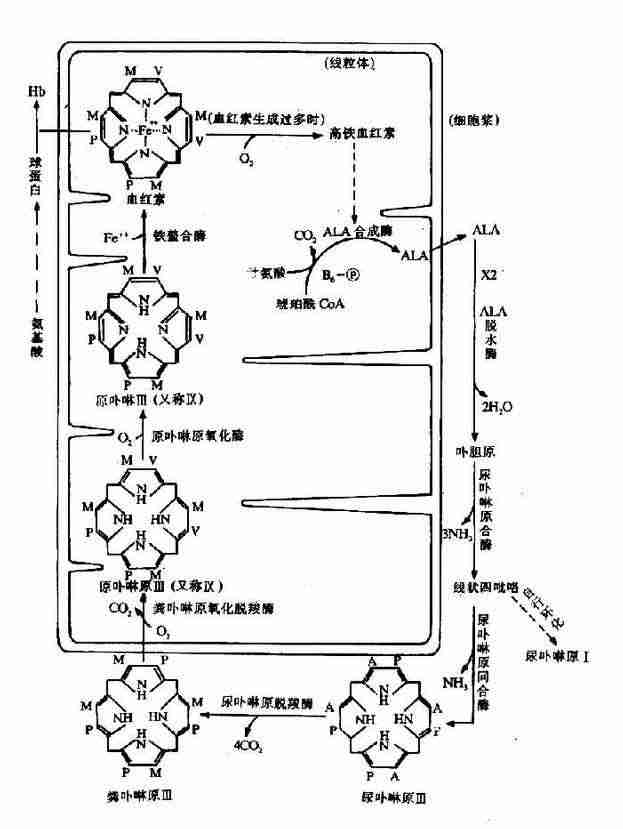
A.乙酸基 P.丙酸基 M.甲基 V.乙烯基
图10-18 血红素的生物合成及其调节
血红素生成后从线粒体转入胞液,与珠蛋白结合而成为血红蛋白。正常成人每天合成6克Hb,相当于合成210mg血红素。
(二)血红素合成的调节
血红素的合成受多种因素的调节,其中主要是调节ALA的生成。
1.ALA合成酶 血红素合成酶系中,ALA合成酶是限速酶,其量最少。血红素对此酶有反馈抑制作用。目前认为,血红素在体内可与阻遏蛋白结合,形成有活性的阻遏蛋白,从而抑制ALA合成酶的合成。此外,血红素还具有直接的负反馈调节ALA合成酶活性的作用。实验表明,血红素浓度为5×10-6M时便可抑制ALA合成酶的合成,浓度为10-5~10-4M时则可抑制酶的活性。正常情况下血红素生成后很快与珠蛋白结合,但当血红素合成过多时,则过多的血红素被氧化为高铁血红素(hematin),后者是ALA合成酶的强烈抑制剂,而且还能阻遏ALA合成酶的合成。
雄性激素——睾丸酮在肝脏5β-还原酶作用下可生成5β-氢睾丸酮,后者可诱导ALA合成酶的产生,从而促进血红素的生成。某些化合物也可诱导ALA合成酶,如巴比妥、灰黄霉素等药物,能诱导ALA合成酶的合成。
2.ALA脱水酶与亚铁螯合酶:ALA脱水酶和亚铁螯合酶对重金属敏感,如铅中毒可抑制这些酶而使血红素合成减少。
3.造血生长因子:目前已发现多种造血生长因子,如多系(multi)一集落刺激因子,中性粒细胞-巨噬细胞集落刺激因子(GM-CSF)、白细胞介素3(IL-3),及促红细胞生成素等。其中促红细胞生成素(erythropoiefin,EPO)在红细胞生长,分化中发挥关键作用。人EPO基因位于7号染色体长臂21区,由4个内含子和5个外显子组成。所编码的多肽由193个氨基酸残基组成。在分泌过程中经水解去除信号肽,成为166个氨基酸的成熟肽。分子量为18398。EPO为一种糖蛋白,由多肽和糖基两部分组成,总分子量为34000。糖基在Epo合成后分泌及生物活性方面均有重要作用。成人血清Epo主要由肾脏合成,胎儿和新生儿主要由肝脏合成。当循环血液中红细胞容积减低或机体缺氧时,肾分泌Epo增加。Epo可促进原始红细胞的增殖和分化、加速有核红细胞的成熟,并促进ALA合成酶生成,从而促进血红素的生成。
此外铁对血红素的合成有促进作用。而血红素又对珠蛋白的合成有促进作用。
血红素合成代谢异常而引起卟啉化合物或其前身体的堆积,称为卟啉症(porphyria)。先天性红细胞生成性卟啉症(congenitalerythropoietic porphyria)是由于先天性缺乏尿卟啉原Ⅲ同合酶,而使线状四吡咯向尿卟啉原Ⅲ的转变受阻,致使尿卟啉原Ⅰ生成增多。病人尿中有大量尿卟啉Ⅰ和粪卟啉Ⅰ出现。
二、成熟红细胞的代谢特点
成熟红细胞不仅无细胞核,而且也无线粒体、核蛋白体等细胞器,不能进行核酸和蛋白质的生物合成,也不能进行有氧氧化,不能利用脂肪酸。血糖是其唯一的能源。红细胞摄取葡萄糖属于易化扩散,不依赖胰岛素。成熟红细胞保留的代谢通路主要是葡萄糖的酵解和磷酸戊糖通路以及2.3一二磷酸甘油酸支路(2,3-biphosphoglycerate,2.3桞PG)。通过这些代谢提供能量和还原力(NADH,NADPH)以及一些重要的代谢物(2,3桞PG),对维持成熟红细胞在循环中约120的生命过程及正常生理功能均有重要作用。
(一)糖酵解
循环血液中的红细胞每天消耗约30g葡萄糖,其中90~95%经糖酵解被利用。一分子葡萄糖经酵解可产生2分子ATP。红细胞中生成的ATP主要用于维持红细胞膜上的离子泵(钠泵、钙泵),以保持红细胞的离子平衡;维持细胞膜可塑性;谷胱甘肽合成及核苷酸的补救合成等。缺乏ATP则红细胞膜内外离子平衡失调,红细胞内Na+进入多于K+排出、Ca++进入增多,红细胞因吸入过多水分而膨大成球状甚至破裂。同时由于ATP缺乏,可使红细胞膜可塑性下降,硬度增高,易被脾脏破坏,造成溶血。
红细胞无氧酵解中生成的NADH+H+是高铁血红蛋白还原酶的辅助因子,此酶催化高铁血红蛋白还原为有载氧功能的血红蛋白。
(二)2,3-二磷酸甘油酸(2,3-BPG)支路
在糖无氧酵解通路中,1,3-二磷酸甘油酸(1,3-BPG)有15~50%在二磷酸甘油酸变位酶催化下生成2,3-BPG,后者再经2,3-BPG磷酸酶催化生成3?磷酸甘油酸。经此2,3-BPG的侧支循环称2,3-BPG支路(图10-19)。
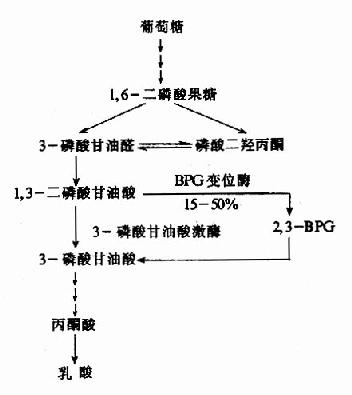
图10-19 2,3-BPG支路
红细胞中2,3-BPG磷酸酶活性远低于BPG变位酶,使2,3-BPG的生成大于分解,因而红细胞中2,3-BPG的浓度处于有机磷酸酯的巅峰,较糖酵解其它中间产物的有机磷酸酯高出数+甚至数百倍(表10-4)。
表10-4 红细胞中各种糖酵解中间产物的浓度(微克分子/升红细胞)
| 糖酵解中间产物 |
动脉血 |
静脉血 |
| 6-磷酸葡萄糖 |
30.0 |
24.8 |
| 6-磷酸果糖 |
9.3 |
3.3 |
| 1,6二磷酸果糖 |
0.8 |
1.3 |
| 磷酸丙糖 |
4.5 |
5.0 |
| 3-磷酸甘油酸 |
19.2 |
16.5 |
| 2-磷酸甘油酸 |
5.0 |
1.9 |
| 磷酸烯醇式丙酮酸 |
10.8 |
6.6 |
| 丙酮酸 |
87.5 |
143.2 |
| 2,3-DPG |
3400 |
4940 |
2,3-BPG能特异地与去氧血红蛋白(deoxy Hb)结合,2,3-BPG进入血红蛋白α2β2四聚体中心空隙两个β亚基之间,借其分子中所带5个负电荷与两个β亚基的带正带氨基酸残基以盐键及氢键结合,使两个β亚基保持分开的状态,即促使血红蛋白由紧密态向松驰态转换,从而减低血红蛋白对氧的亲和力(图10-20)。
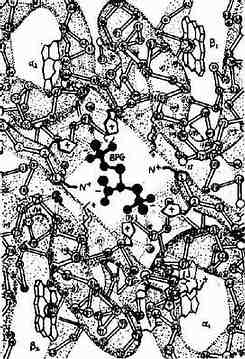
图10-20 BPG与Hb的作用示意图
当红细胞内2,3-BPG浓度升高时有利于HbO2放氧,而2,3-BPG浓度下降则有利于Hb与氧结合。BPG变位酶及2,3-BPG磷酸酶受pH值调节。在肺泡毛细血管血液pH高,BPG变位酶受抑制而2,3-BPG磷酸酶活性强。使红细胞内2,3-BPG的浓度降低,有利于Hb与O2结合。
反之,在外周组织毛细血管中,血液pH下降,2,3-BPG的浓度升高,则利于HbO2放氧,借此调节氧的运输和利用,具有重要生理意义。但2,3-BPG的生成是以减少一个ATP的生成为代价的。
(三)磷酸戊糖通路
红细胞内利用葡萄糖的5~10%通过磷酸戊糖通路代谢,为红细胞提供另一种还原力(NADPH),NADPH在红细胞氧化还原系统中发挥重要作用,具有保护膜蛋白、血红蛋白及酶蛋白的巯基不被氧化,还原高铁血红蛋白等多种功能。
1.GSH的主要生理功能是对抗氧化剂对巯基的氧化。细胞内可自发生成少量超氧阴离子(O-2),同时感染时的白细胞吞噬作用亦可产生O-2,可被超氧化物歧化酶(superoxidedismufase SOD),催化生成过氧化氢(H2O2)。
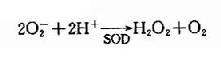
而GSH在谷胱甘肽过氧化酶作用下将H2O2还原为H2O,GSH自身被氧化为氧化型谷胱甘肽(GSSG)。后者在谷胱甘肽还原酶催化下,由NADPH+H+供氢重新还原为GSH。(图10-21)。
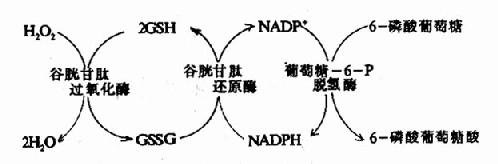
图10-21 谷胱甘肽的氧化与还原
催化NADPH生成的关键酶为葡萄糖-6-磷酸脱氢酶。此酶缺陷的病人一般情况下无症状,但有外界因素(如进食某种蚕豆)影响,即引起溶血。因吃蚕豆可诱导发病,故这种病又称蚕豆病。
2.高铁血红蛋白(methemoglobin MHb)的还原:由于各种氧化作用,红细胞内经常有少量MHb产生,而由于红细胞内有一系列酶促及非酶促的MHb还原系统(表10?),故正常红细胞中MHb只占1-2%。
表10-5 红细胞中MHb还原系统
| 还原系统 |
占总还原能力的百分比(%) |
| 酶促还原系统 |
|
| NADH脱氢酶Ⅰ |
61 |
| NADH脱氢酶Ⅱ |
5 |
| NADH脱氢酶 |
6 |
| 非酶促还原系统 |
|
| 抗坏血酸 |
16 |
| 谷胱甘肽 |
12 |
由表10-5可知,催化MHb还原的主要是NADH-脱氢酶,辅酶为NADH+H+。NADPH脱氢酶,(以NADPH+H+为辅酶)也参与MHb还作,但作用较小。除此之外,抗坏血酸和GSH可直接还原MHb,而氧化型抗坏血酸和GSSG的还原作用最终需NADPH+H+供氢。