一、组织学发展概况及研究内容与意义
组织学(histology)与胚胎学(embryology)是相互关联的两门学科,我国医学教育习惯地将它们列为一门基础课程。组织学是研究机体微细结构及其相关功能的科学,它是以显微镜观察组织切片为基本方法的,故又称显微解剖学(microanatomy)。从细胞的发现和细胞学说的建立起始,组织学发展迄今为已有300余年历史。英国人Hooke(1635~1703)用放大镜观察软木塞薄片,首先描述了细胞壁所成的小室,称之为“cell”。意大利人Malpighi(1628~1694)用放大镜观察了脾、肺、肾等的组织结构,荷兰人Leeuwenhoek(1632~1723)用较高倍的放大镜发现了精子、红细胞、肌细胞、神经细胞等,荷兰人Graaf(1641~1673)观察报道了卵泡。法国人Bichat(1771~1822)用放大镜观察肉眼解剖的组织,并于1801年发表的“膜的研究”一文,首次提出“组织”(法文tissu,原意为编织物)一词,还将人体的组织分为21种。德国人Meyer(1819)又将组织重新分类为8种,并创用Histology一词。Brown(1831)进而发现了细胞核,对细胞的结构有了初步的认识。在有机体结构长期研究和争议的基础上,德国学者Schleiden(1804~1881)和Schwann(1810~1882)于1838~1839年分别指出细胞是一切植物和动物的结构、功能和发生的重要单位,创立了细胞学说,成为组织学、胚胎学、生理学、病理学等生命科学发展的重要里程碑,被誉为是19世纪自然科学的三大发现(细胞学说、物质和能量守恒定律、达尔文进化论)之一。此后不久,德国学者Virchow(1821~1902)于1858指出细胞只源于细胞,细胞损害是一切疾病的基础,建立了细胞病理学说,使细胞学说更趋完善。19世纪中期以后,随着光学显微镜、切片技术及染色方法的不断改进与充实,推进组织学的继续发展。本世纪初至中期,陆续制成相差显微镜、偏光显微镜、暗视野显微镜、荧光显微镜、紫外光显微镜等特殊显微镜,并用之于组织学研究;与此同时,组织化学、组织培养、放射自显影等技术也渐建立和完善并广泛应用,组织学研究更趋深入,资料日益丰富。本世纪40年代电子显微镜问世,并不断改进,至今已广泛用于观察细胞和组织的微细结构及其不同状态下的变化,使人类对生命现象结构基础的认识深入到更微细的境界,其中许多重要资料已列为现代组织学的基本内容。
我国组织学研究起始于本世纪之初,组织学是从人体解剖学分化出来的一门较年轻的科学。我国老一辈组织学家如马文昭(1886~1965)、鲍鉴清(1893~1982)、王有琪(1899~)、张作干(1907~1969)、李肇特(1913~)、薜社普(1917~)等,他们在学科建设、科学研究和人才培养等方面做出了历史性贡献。
近30年科学技术发展更为迅猛,许多新技术、新设备不断涌现并用之于细胞学和组织学的研究,诸如免疫细胞化学术、单克隆技术、细胞分离术、细胞融合术、显微分光光度计、图像分析仪与立体计量术、同位素示踪术、流式细胞术、蛋白质和核酸的分离提取及原位检测、原位杂交等核酸分子杂交术、X-射线衍射技术、X-射线显微分析术,以及分子重组与基因工程等。这些新技术大多与计算机技术相结合,对细胞进行微观和微量的定性和定量分析,使组织学的研究进入更深入而广阔的境地。
组织(tissue)是由细胞(cell)和细胞间质(intercellular substance)组成,众多细胞由细胞间质组合在一起构成一细胞群体。细胞是组织的结构和功能单位,高等动物和人体的细胞有成百上千种类型,各种细胞具有一定的形态结构特点,合成与功能相关的特殊蛋白质,表达某种代谢特点和功能活动,即为细胞的表现型(phenotype)。细胞间质是由细胞产生的非细胞物质,包括纤维、基质和不断流动的体液(血浆、淋巴、组织液等),它们参与构成细胞生存的微环境(microenvironment),起支持、联系、营养和保护细胞的作用,对细胞的分化、运动、信息沟通也有重要影响。组织微环境的稳定是保持细胞增殖、分化、代谢和功能活动的重要条件,微环境成分的异常变动也可使细胞发生病理变化。组织有多种类型,每种组织具有某些共同的形态结构特点和相关的功能。一般传统性将组织分为四种,即上皮组织、结缔组织、肌组织和神经组织,称为基本组织(primary tissue)。但现代组织学的研究愈来愈多地发现,一种组织内的细胞结构和功能往往是多种多样的,它们的起源也不同;因此应认识到,组织分类是一种归纳性的相对意义的概念,不能机械僵化地理解。几种组织相互结合,组成器官(organ)和系统(system),人体的组成包括神经、内分泌、免疫、循环、皮肤、感官、消化、呼吸、泌尿、生殖等系统。
医学组织学的研究对象是人体,但人体材料来源受限,尤其是许多实验性研究的开展,需选用实验动物为材料。应用显微镜观察机体的组织结构及其形态演变,称为描述组织学。一般光学显微镜下所见的结构,称光镜结构;电子显微镜下显示的结构,称超微结构(ultrastructure)研究不同动物种系的组织结构和功能的,称为比较组织学。应用实验方法研究组织结构与功能的动态变化、理化因子或生物因子的调节或影响,以及致病、致癌等机理,秒为实验组织学。从分子水平探讨细胞和组织的功能及其异常变化的机理,则属分子生物学。
不言而喻,学习医学科学必须首先熟悉人体的结构、组成及其基本生命现象,组织学、从微观水平阐明机体的结构与相关功能,无疑是医学教育的重要入门课程之一,它为生理学、生物化学、免疫学、病理学以及临床医学等的学习奠定坚实基础。组织学是以微细结构的形态描述为其基本内容,但随着生命科学的研究不断深入,现代组织学的内容与60年代相比已发生巨大变化。它的内容不断充实、更新和扩展,不仅形态观察更微细深入,而且涉及的领域更为广阔,从整体水平、细胞水平和分子水平探索许多复杂生命现象的物质基础以及环境与生物体的相互关系;不仅与现代生物学和医学的许多重大理论进展相关,而且与人类社会面临的众多实际问题和疾病防治密切相关。诸如:细胞增殖与分化的调控,细胞突变、癌变与逆转,细胞运动与迁移,细胞识别与通讯,细胞与组织的移植,细胞与组织的衰老,细胞与免疫、组织与器官的再生,神经调节与体液调节,环境污染与组织病变等等。这些问题的研究与解决,都需要多学科的密切协作和高技术的综合应用,组织学也处于当代生命科学各学科相互交叉的网络中,与分子生物学、细胞生物学、生理学、生物化学、生物物理学、免疫学、病理学、肿瘤学、环境毒理学等,理论上相互关联渗透,技术上相互引用促进,关系日益密切。在基础医学各门课程的教学中,处处可看到现代医学的这种发展势头。
二、组织学研究方法
(一)一般光学显微镜术
应用一般光学显微镜(简称光镜)观察组织切片是组织学研究的最基本方法。取动物或人体的新鲜组织块,先用固定剂(fixative)固定(fixation),使组织中的蛋白质迅速凝固,防止细胞自溶和组织腐败。常用的固定剂如洒精、甲醛、醋酸、苦味酸、四氧化锇等,一般常将几种固定剂配制成混合固定液,以抵消或减弱单种固定剂对组织的收缩或膨胀等缺点,达到更好固定效果。固定后的组织块(约3~5mm3大小)用石蜡、火棉胶或树脂等包埋(embedding)成硬块,以切片机(microtome)切成5~10μm厚的组织切片(tissue section),切片贴在载玻片上经脱蜡等步骤后进行染色。组织块也可立即投入液氮(-196℃)内快速冻结,用恒冷箱切片机(cryostat)制成冷冻切片(frozen section),这种方法制片迅速,细胞内酶活性保存较好,常用于酶组织化学染色。血细胞和分离培养的细胞可直接涂在玻片上,制成涂片(smear)。疏松结缔组织和肠系膜等软组织可撕成薄片铺在玻片上(铺片),牙和骨等坚硬组织可磨成薄片(磨片)。组织切片等标本经染色、透明后,以封固剂和盖片封固,即可长期保存,镜下观察。
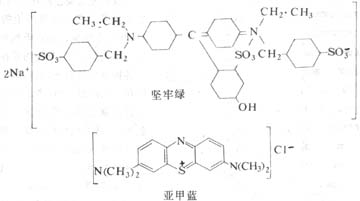
图1-1 坚牢绿(酸性染料)与亚甲蓝(碱性染料)的化学结构及其染色反应示意
染色(staining)是用染料使组织切片着色,便于镜下观察。天然和人工合成的染料甚多,它们都是含发色团的有机化合物,当染料具有助色团成为盐类物质,即可溶解于水并具电荷,与组织有亲合力,使组织着色。含氨基(-NH2)、二甲氨基〔-N(CH3)2〕等碱性助色团的染料,称碱性染料(basic dye),它的盐溶液具阳电荷;含羧基(-COOH)、羟基(-OH)或磺基(-SO3H)等酸性助色团的染料,称酸性染料(acid dye),它的溶液具阴电荷(图1-1)。组织的染色原理一般认为基于化学结合或物理吸附作用。细胞和组织的酸性物质或结构与碱性染料亲合力强者,称嗜碱性(basophilia);而碱性物质或结构与酸性染料亲合力强者,称嗜酸性(acidophilia);若与两种染料的亲合力均不强者,称中性(neutrophilia)。组织的基本成分是蛋白质,构成蛋白质的氨基酸常是即有含氨基的,也有含羧基的,是两性电解质。各种蛋白质的等电点因氨基酸成分的不同而异,其电荷性质又与溶液的pH值相关,根据研究目的选用合适的染色方法,调整好染液的pH值,即可取得良好染色效果。常用的酸性染料如伊红、坚牢绿、橙黄G等,碱性染料如苏木精、亚甲蓝、碱性品红等。组织学中最常用的是苏木精(hematoxylin)和伊红(eosin)染色法,简称HE染色法。苏木精使细胞核和胞质内的嗜碱性物质着蓝紫色,伊红使细胞质基质和间质内的胶原纤维等着红色。
物理吸附作用的染色方法,如用苏丹染料显示脂肪组织,染料溶于脂肪内,使细胞内的脂滴显色。又如用硝酸银、氯化金等重金属盐显示细胞和组织的某些结构,则是使金属微粒附着在结构表面而呈棕黑色或棕黄色。银染法中有些组织结构可直接使硝酸银还原而显示,称此为亲银性(argentaffin);有些结构无直接还原作用,需加入还原剂方能显色,则称为嗜银性(argyrophilia)。还有些组织成分如结缔组织和软骨基质中的糖氨多糖,当用甲苯胺蓝(toluidine blue)等碱性染料染色后呈紫红色,这种现象称为异染性(metachromasia),其原理可能是该染料在溶液中呈单体状态时显蓝色,当它与多阴离子的高分子物质耦合后,染料分子聚合成多聚体而显红色(图1-2)。还有些染色方法的原理至今还不清楚。
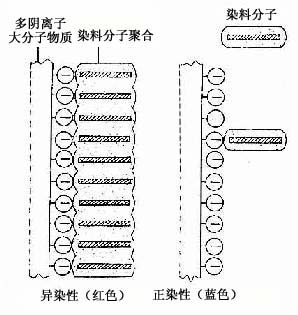
图1-2 异染性示意图
(二)几种特殊显微镜的应用
1.荧光显微镜 荧光显微镜(fluorescence microscope)是用来观察标本中的自发荧光物质或以荧光素染色或标记的细胞和结构。荧光显微镜是以高压汞灯产生的短波紫外线为光源,并配有激发、阻断、吸热和吸收紫外线等滤片系统,标本中的荧光物质在紫外线激发下产生各种颜色的荧光,借以研究该荧光物质在细胞和组织内的分布。组织中的自发性荧光物质如神经细胞和心肌细胞等内的脂褐素呈棕黄色荧光,肝贮脂细胞和视网膜色素上皮细胞内的维生素A呈绿色荧光,某些神经内分泌细胞和神经纤维内的单胺类物质(儿茶酚胺、5-羟色胺、组胺等)在甲醛作用下呈不同颜色的荧光,组织内含有的奎宁、四环素等药物也呈现一定的荧光。细胞内的某些成分可与荧光素结合而显荧光,如溴化乙锭与吖啶橙可与DNA综合,进行细胞内DNA含量测定。荧光显微镜更广泛用于免疫细胞化学研究,即以异硫氰酸或罗丹明等荧光素标记抗体(一抗或二抗),用该标记抗体直接或间接地与细胞内的相应抗原结合,以检测该抗原的存在与分布。
2.相差显微镜 相差显微镜(phase contrast microscope)是用于观察组织培养中活细胞形态结构的。活细胞无色透明,一般光镜下不易分辨细胞轮廓及其结构。相差显微镜的特点是将活细胞不同厚度及细胞内各种结构对光产生的不同折射作用,转换为光密度差异(明暗差),使镜下结构反差明显,影像清楚。组织培养研究常用的是倒置相差显微镜(inverted phase contrast microscope),它的光源和聚光器在载物台的上方,物镜在载物台的下方,便于观察贴附在培养器皿底壁上的活细胞。
3.暗视野显微镜 暗视野显微镜(dark-field microscope)主要用于观察因反差或分辨力不足的微小颗粒。此种显微镜主要是有一个暗视野集光器,使光线不直接进入物境,故呈暗视野。而标本内的小颗粒产生的衍射光或散射光进入物镜,暗视野中的颗粒呈明亮小点,如同在暗室可见一束光线中的微小尘粒一般。普通通光镜最大分辨率为0.2μm,暗视野显微镜则可分辨0.004~0.2μm的微粒,适用于观察细胞内线粒体运动及标本中细菌等微粒的运动等。
4.共集激光扫描显微镜 共焦激光扫描显微镜(confocal laser scanning microscope,CLSM)是近10年研制成的高光敏度、高分辨率的新型仪器。它以激光为光源,光束经聚焦后落在样品(组织厚片或细胞)不同深度的微小一点,并作移动扫描,通过电信号彩色显像,经过微机图像分析系统进行二维和三维分析处理。CLSM可对细胞进行三维结构图像分析,细胞内各种荧光标记物的微量分析,细胞内Ca2+、pH值等的动态分析测定,细胞的受体移动、膜电位变化、酶活性和物质转运的测定,并以激光对细胞及其染色体进行切割、分离、筛选和克隆。因此,CLSM是一种高技术产品,可对细胞的多种功能进行全自动、高效、快速的微量定性和定量测定。
其他如偏光显微镜用于研究组织晶体物质及纤维等的光学性质,紫外光显微镜用于研究细胞内核酸的分布与定量等。
(三)组织化学和细胞化学术
组织化学(histochemistry)和细胞化学(cytochemistry)技术是通过化学或物理反应原理显示组织切片细胞内某种化学成分,进行定位、定量及其与功能相关的研究。如糖类、脂类、酶、核酸等与试剂发生化学物理反应,形成有色终末产物,在光镜下观察,有的可在电镜下观察。
1.糖类显示多糖和蛋白多糖的常用方法是过碘酸-雪夫反应(periodic acid Schiff reaction,PAS反应)。基本原理是过碘酸的氧化作用先使糖分子的乙二醇基变为乙二醛基,后者继而与Schiff试剂(无色亚硫酸品红复合物)结合,形成紫红色反应产物(图1-3)。颜色反应的深浅取决于组织内多糖的乙二醇分子的多寡。
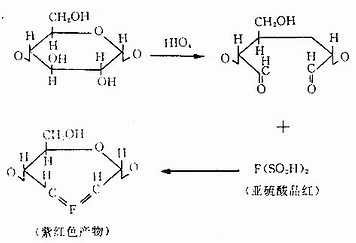
图1-3 PAS反应原理示意图
2.脂类脂类物质包括脂肪和类脂。标本用甲醛固定,冷冻切片,脂类保存较好。多用苏丹染料、油红O、尼罗蓝等溶于脂类的染料染色,使脂质呈色。也可用四氧化锇(OSO4)染色,脂肪酸或胆碱可使OSO4还原为OSO2而呈黑色。
3.酶细胞内的酶种类甚多,有氧化还原酶、水解酶、合成酶、转移酶等几类,目前已有100多种酶组织化学染色法。酶组化反应的基本原理是利用酶对其相应底物的水解、氧化等作用,然后再使底物的反应产物与某种捕获剂发生反应,形成沉淀或有色的最终产物,借此检测该酶在组织切片或细胞内的分布及活性强弱。如细胞的磷酸酶是一种重要的水解酶,碱性磷酸酶(ALP)和酸性磷酸酶(ACP)在合适的pH条件下可水解有机磷酸脂。小肠上皮细胞表面的纹状缘和肾近曲小管表面的刷状缘处,微绒毛含有丰富的ALP,与物质的吸收和转运功能相关;许多细胞的溶酶体内则含大量ACP,参与细胞内物质代谢。这两种酶均可以β-甘油磷酸钠为底物,底物被水解产生磷酸根,再以Ca2+、Co2+(显示ALP)或Pb2+(显示ACP)捕获磷酸根,最后用硫化铵处理,即形成硫化钴或硫化铅黑色最终产物,出现在组织切片中该酶存在的部位。因此,酶组化染色不是酶本身的直接显色,而是酶作用底物的化学反应产物显色的。
4.核酸 显示DNA的传统方法是Feulgen反应,切片先用稀盐酸处理,使DNA分子中脱氧核糖与嘌呤之间的连接键打开,形成醛基,再与Schiff 试剂作用,原理同PAS反应,使细胞核DNA显紫红色。还可用甲基绿-焦宁染色法同时显示DNA和RNA,这两种染料都是碱性,甲基绿使细胞核内的DNA呈蓝绿色,焦宁使细胞质和核仁内的RNA呈红色。
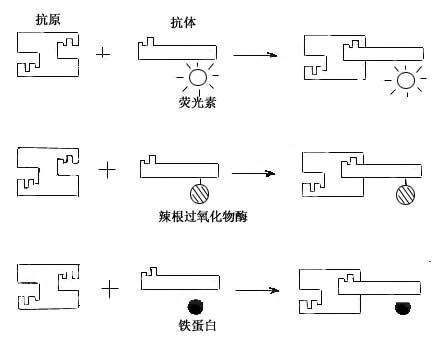
图1-4 免疫细胞化学术示意图
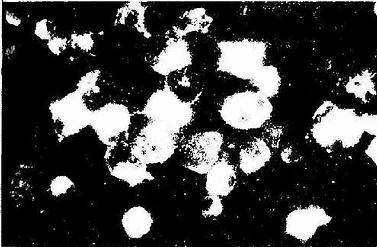
图1-5 人呼吸道分离上皮细胞粘蛋白免疫荧光像
(美国戴维斯加州大学 吴忍教授供图)
(四)免疫细胞化学术
免疫细胞化学(immunocytochemistry)术是应用抗原与抗体结合的免疫学原理,检测细胞内多肽、蛋白质及膜表面抗原和受体等大分子物质的存在与分布。这种方法特异性强,敏感度高,进展迅速,应用广泛,成为生物学和医学众多学科的重要研究手段。近年随着纯化抗原和制备单克隆抗体的广泛开展以及标记技术不断提高,免疫细胞化学的进展更是日新月异,不仅用于许多基本理论的研究,并取得重大突破,而且也用于疾病的早期快速诊断等临床实际。组织的多肽和蛋白质种类繁多,具有抗原性。分离纯化人或动物组织某种蛋白质,作为抗原注入另一种动物体内,后者即产生相应的特异性抗体(免疫球蛋白)。从被免疫动物的血清中提取出该抗体,再以荧光素、酶、铁蛋白或胶体金标记,用这种标记抗体处理组织切片或细胞,标记抗体即与细胞的相应蛋白质(抗原)发生特异性结合(图1-4)。常用的荧光素是异硫氰酸荧光素(FITC)和四甲基异硫氰酸罗丹明(TRITC),在荧光显微镜下可观察荧光抗体抗原复合物(图1-5)。常用的酶是辣根过氧化物酶(horseradish peroxidase,HRP,从辣根菜中提取的),它的底物是3,3'-二氨基、联苯胺(DAB)和H2O2,HRP使DAB氧化形成棕黄色产物,可在光镜和电镜下观察(图1-6)。铁蛋白和胶体金标记抗体与抗原的结合,也可在光镜和电镜下观察(图1-7)。
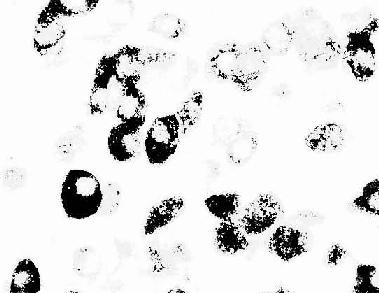
图1-6 大鼠腺垂体免疫组织化学(PAS法)示生长激素细胞
(上海医科大赵培林教授供图)
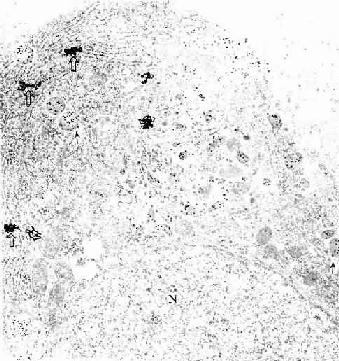
图1-7 免疫细胞化学(蛋白A-胶体金法)和原位杂交术示大鼠垂体
催乳素细胞电镜像 N催乳素细胞核
↑分泌颗粒内显示金粒
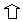
粗面内质网(RER)显示银粒
(加拿大Douglas医院研究中心童毅爱博士赠图)
标记抗体民被检抗原的结合方式有两种。一是直接法,即如上述用标记抗体与样品中的抗原直接结合(图1-8)。这种方法操作简便,但敏感度不及间接法。间接法是将分离的抗体(第一抗体简称一抗)再作为抗原免疫另一种动物,制备该抗体(抗原)的抗体(第二抗体简称二抗),再以标记物标记二抗。先后以一抗和标记二抗处理样品,最终形成抗原一抗-标记二抗复合物(图1-8)。间接法中的一个抗原分子可通过一抗与多个标记二抗相结合,因此它的敏感度较高,而且目前国内外均有多种标记二抗商品供应,使用方便。间接法中较常用的是一种称之为过氧化物酶-抗过氧化物酶复合物法(peroxidase-antiperoxidase complexmethod,PAS法),该法除需一抗和二抗外,还需制备HRP标记的抗酶抗体,即以HRP作为抗原免疫动物,制成抗HRP抗体,再以HRP标记该抗体制成由3个酶分子与2个抗酶抗体组成的相当稳定的环形PAP复合物。标本先后以一抗、二抗和PAP复合物处理后,再以DAB显色,即可检测抗原的分布。此法由于细胞内的抗原通过抗体的层层放大而与多个酶分子结合,因此敏感性很强(图1-9)。
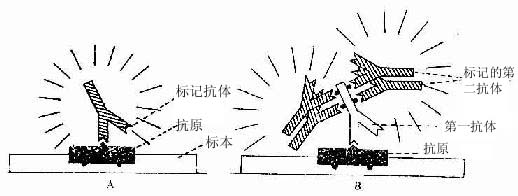
图1-8 免疫细胞化学直接法(A)与间接法(B)示意图
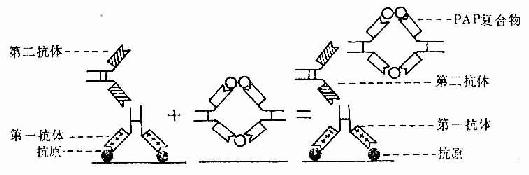
图1-9 免疫细胞化学PAP法示意图
免疫细胞化学术近10年来又有新进展,如生物素-亲合素等新颖试剂的应用,为检测微量抗原、受体、抗体开辟了新途径。生物素(biotin)又称维生素H,是从卵黄和肝中提取的一种小分子物质(分子量244.31);亲合素(avidin)又称卵白素,是从卵白中提取的一种糖蛋白(分子量68kD)。每个亲合素分子有生物素结合的4个位点,二者可牢固结合成不可逆的复合物。生物素-亲合素的应用大致有三种方法。①标记亲合素-生物素法(labelled avidin- biotin method,LAB法):将亲合素与标记物(HRP)结合,一个亲合素可结合多个HRP;将生物素与抗体(一抗与二抗)结合,一个抗体分子可连接多个生物素分子,抗体的活性不受影响。细胞的抗原(或通过一抗)先与生物素化的抗体结合,继而将标记亲合素结合在抗体的生物素上,如此多层放大提高了检测抗原的敏感性(图1-10)。②桥连亲合素-生物素法(bridged avidin-biotin method,BAB法):先使抗原与生物素化的抗体结合,再以游离亲合素将生物素化的抗体与酶标生物素搭桥连接,也达到多层放大效果(图1-10)。③亲合素-生物素-过氧化物酶复合物法(avidin-biotin-peroxidase complexmethod,ABC法);此法是前两种方法的改进,即先按一定比例将亲合素与酶标生物素结合在一起,形成亲合素-生物素-过氧化物酶复合物(ABC复合物),标本中的抗原先后与一抗、生物素化二抗、ABC复合物结合,最终形成晶格样结构的复合体,其中网络了大量酶分子,从而大大提高了检测抗原的灵敏度(图1-10)。现有配制现成的ABC药盒商品供应,操作简便,是目前广泛应用的一种方法。
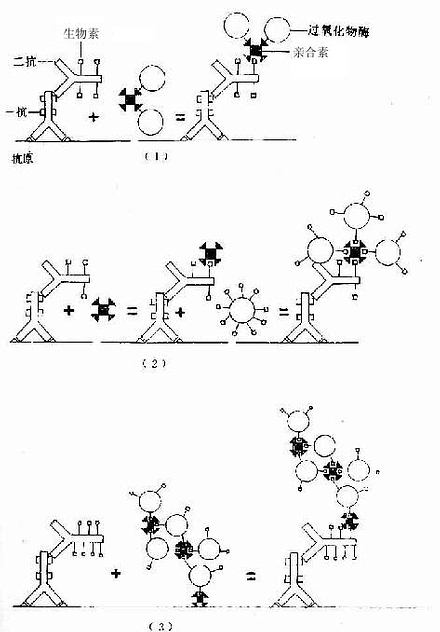
图1-10 生物素-亲合素免疫细胞化学示意图
(1)标记亲合素-生物素法
(2)桥连亲合素-生物素法
(3)亲合素-生物素-过氧化物酶复合物法(ABC法)
(五)同位素示踪术
同位素示踪术是用放射性核素的射线作用,研究细胞对某种物质的吸收、合成、转运和分泌等代谢过程。将放射性核素或其标记物注入动物体内或加入细胞培养的培养基内,细胞摄取该物质后,取被检组织制成切片或细胞涂片。可用显微镜放射自显影术(microau toradiography)检测该放射性物质在细胞内的原位分布及其代谢转归,即将薄层感光乳胶涂在切片或涂片的表面,标本在暗盒内保存一定时间后,细胞内的放射性核素产生的射线使乳胶中的溴化银还原为银粒,经显影和定影后在光镜下观察银粒的分布。β射线能量低,射程短,电离作用强,常用的β射线核素是3H、14C、32P、35S、45Ca、131I。如用3H-胸腺嘧啶核苷研究细胞DNA合成及细胞增殖动态(图1-11)。用35S-蛋氨酸研究某些腺细胞分泌物的合成与排泄,用131I-碘化钠研究甲状腺素的合成等。还可做标本中的银粒数计量或其光密度测定,进行定量分析。另外,也可用液体闪烁计数器测定分离细胞或其匀浆的放射线强度,进行定量研究。
(六)原位杂交术
原位杂交术(in situ hybridization)是一种核酸分子杂交技术,它是通过检测细胞内mRNA和DNA序列片段,原位研究细胞合成某种多肽或蛋白质的基
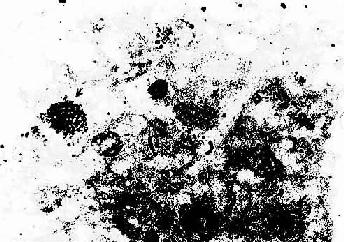
图1-11 大鼠肝大部切除后再生过程中增殖期肝细胞
摄取3H标记的胸腺嘧啶核苷放射自显影像
↑ 增殖期肝细胞核
因表达。其基本原理是根据两条单链核苷酸互补碱基序列专一配对的特点,应用已知碱基序列并具有标记物的RNA或DNA片段即核酸探针(probe),与组织切片或细胞内的待测核酸(RNA或DNA片段)进行杂交,通过标记物的显示,在光镜或电镜下观察目的mRNA或DNA的存在与定位。此项技术需首先制备某种核酸探针,其种类主要有三种:①利用大肝杆菌重组带有目的基因的质粒DNA,制成互补DNA探针(cDNA);②应用限制性核酸内切酶消化制成线性DNA模板,在体外转录获得反意RNA探针(cDNA);③依照待测核酸的核苷酸序列,应用DNA合成仪合成寡聚核苷酸探针。cRNA和cDNA的常用标记物有32S、32P、3H等放射性核素和荧光素、生物素、地高辛等非放射性物质。组织学应用的原位杂交术主要是染色体原位杂交和细胞原位杂交。前者是研究遗传基因、抗原基因、受体基因、癌基因等在染色体上的定位与表达;后者是研究细胞某种蛋白质的基因转录物mRNA在胞质内的定位与表达(图1-7,1-12)。核酸分子杂交术有很高的敏感性和特异性,它是免疫细胞化学的基础上,进一步从分子水平探讨细胞功能的表达及其调节机制的,已成为当前细胞生物学、分子生物学研究的重要手段。
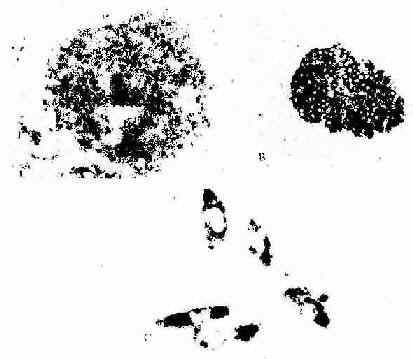
图1-12 原位杂交术光镜像
A 32P标记胰岛素cRNA探针放射自显影显示大鼠胰岛B细胞内胰岛素mRNa
B 地高辛-碱性磷酸酶标记胰岛素cRNA探针显示大鼠胰岛B细胞内胰岛素mRNA
C 地高辛-碱性磷酸酶标记心钠素cRNA探针显色示体外培养的人胎儿脐静脉
内皮细胞内的心钠素mRNA ×850
(第三军医大学蔡文教授供图)
(七)细胞和细胞化学定量术
组织和细胞形态结构及其化学成分的定量研究,是以量的测定及其数据变化阐述组织和细胞的生长、分化、代谢和功能的演变以及对环境因素和致病因素的反应。生命科学的研究不断深入,定量技术的应用日益广泛并有所进展。
1、显微镜分光亮度定量术此方法是应用显微分光亮度计(microspectrophotometer)测定组织化学和免疫组织化学染色标本的反应强弱,进行化成分的定量分析的。基本原理是细胞内某种物质的含量不同,其染色反应的深浅不一,对一定波长的光吸收也就不同,即某物质的消亮度与一定厚度和面积内的该物质浓度成正比。通过光电组合自动控制系统将消光度转换为电信号,即可得出光密度值(O、D值),进行定量分析比较。前述荧光素染色、酶和核酸组织化学染色、多肽和蛋白质免疫组化染色、放射自显影和原位杂交等标本,均可应用显微分光光度计做定量分析。
2、形态计量术 形态计量术(morphometry)是运用数学和统计学原理对组织和细胞进行二维和三维的形态测量研究,如细胞及其微细结构成分的数量、体积、表面积、周长等的相对和绝对值的测量,其中三维立体结构的研究又称体视学(stereology)。机体组织的光镜结构计量已有不少有意义的资料,如人和动物的肺泡数量和表面积,肾小体的数量和体积比,肝细胞的体积和数量,胰岛的数量及各类细胞的数量比,腺垂体各种内分泌细胞的数量比等。通过组织切片或照片(光镜和电镜)平面图像的测量,推算其立体结构数值,传统方法是将测试系统(点、线、方格等)投影或覆盖在切片上或照片上,把若干样品的平面测量数据按数学公式推算出其立体数值。目前已广泛应用图像分析仪(image analyzer)进行形态计量研究,该仪器也是光学、电子学和计算机高技术产品,它是将切片或照片图像通过摄像机显示于监示器屏幕上,并根据不同结构的颜色深浅(灰度)及各像点的大小位置,快速准确地得出所需的各种形态数据。组织化学和免疫组织化学染色标本,也可应用图像分析仪测定其光密度值,进行定量分析。
3、流式细胞术 流式细胞术(flow cytometry,FCM)是近年建立的细胞分类和定量研究技术,它是应用流式细胞仪(或称荧光激活细胞分类器,fluroescent activated cell sorter)对单个细胞生物化学和生物物理特性进行快速定量测定的。工作原理是先分离被检细胞制成悬液,并作荧光染色或标记,使单细胞液流快速通过该仪器的激光器照射分析区,被检细胞产生的不同荧光信号转变为电脉冲,分别输入计算机内贮存,并显示于示波器屏幕上,即可获得该细胞群体中不同类型细胞的有关数据,如不同细胞的数量、荧光强度以及细胞体积、表面积和内部结构等参数;还可使细胞附有不同电荷,分类收集各种细胞,该技术的特点是速度快,精确性高,灵敏度大,已成为一种重要手段广泛用于细胞动力学、遗传学、免疫学、肿瘤学等的研究。如细胞DNA,RNA或某种蛋白质的含量分析,单个染色体DNA含量及分选,淋巴细胞膜抗原或受体的分析及细胞亚群分选,杂交细胞等的分选等,也用于肿瘤临床诊断及疗效和预后的分析等。
(八)电子显微镜术
1、透射电镜术 透射电镜(transmission electron microscope,TEM)是以电子束穿透样品(组织的超薄切片),经聚合放大后,显像于荧光屏上进行观察和摄片的。电镜的放大倍数的分辨率比光镜大得多,放大倍数为几万至几十万倍,分辨率可达0.2nm。标本制备较光镜的更严格,新鲜组织切成小块(lmm3),用戊二醛,多聚甲醛、四氧化锇等固定,树脂包埋,以超薄切片机切成厚50~80nm的超薄切片,经醋酸铀和柠檬酸铅等重金属电子染色后,置于电镜下观察,标本在荧光屏上呈黑白反差的结构影像。被重金属浸染呈黑色的结构,称电子密度高(electron-dense);反之,浅染的部分称电子密度低(electron-lucent),这种染色称正染色(positive staining)。若被染结构着色浅淡,而其周围部分染成黑,是称为负染色(negative stainning)。透射电镜的电子枪加速电压50~100kV,电子束穿透力低,近年制成加速电压500kV以上的超高压电镜,电子束穿透力很强,可观察0.5~10μm厚的切片,可观察细胞内骨架等的立体超微结构。应用电镜观察细胞化学染色标本,称电镜细胞化学术(electron microscope cytochemistry);电镜观察免疫细胞化学染色标本,称免疫电镜术(immunoelectron microscopy);电镜与放射自显影结合的方法称电镜放射自显影术(electron microscopeautoradiography)。
2、扫描电镜术 扫描电镜(scanning electron microscope,SEM)是用于观察组织表面的立体结构的。组织块经固定后,置于真空镀膜仪内于燥,在标本表面先后喷镀一层碳膜和合金膜,即可置于镜下观察。扫描电镜的景深长,样品表面的金属膜可提高其导电性和图像反差,在荧光屏上扫描成像,呈现富有立体感的表面图像,如细胞表面的突起、微绒毛、纤毛及细胞的分泌与吞噬行为等(图1-13)。

图1-13大鼠分离肝巨噬细胞粘着吞噬羊红细胞扫描电镜像
M肝巨噬细胞,R羊红细胞
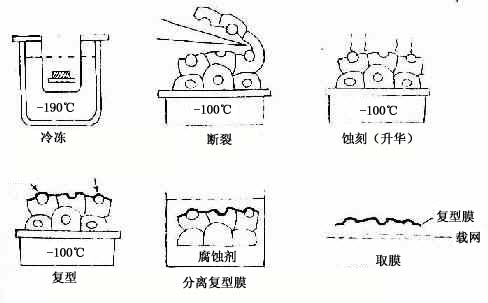
图1-14 冷冻蚀刻标本制备示意图
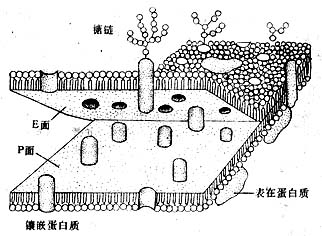
图1-15 细胞单位膜从中间层劈开示意图
3、冷冻蚀刻复型术和冷冻割断术
冷冻蚀刻复型术(tfeeze etch replica):是在透射电镜下观察组织或细胞断裂面的金属复制膜,显示细胞微细结构的立体影像。组织块先经甘油生理盐水处理(防止形成冰晶)后投入液氮快速冷冻,在低温下用钢刀将样品劈开,形成凹凸不平的断裂面:-100℃真空下使断裂面的冰晶升华,暴露不平整表面;在断裂面上先后喷镀一层合金膜和碳膜,用次氯酸等组织腐蚀掉;将反差的凸凹不平的金属复型膜置于镜下观察(图1-14)。此项技术尤适用研究生物膜的内部结构,如从单位膜的脂质分子疏水端劈开(图1-15),经蚀刻镀膜,镜下可见质膜断裂面复型膜结构状态(图1-16),其凹凸影像恰与实物相反。

图1-16小鼠肾近曲小管微绒毛冷冻蚀刻复型电镜像 ×38300
MV微绒毛 E E面,P P面(白求恩医科大学尹昕、朱秀雄教授供图)
冷冻割断术(freeze cracking):是将固定组织包埋在树脂内,低温下割断,断面喷镀合金,在扫描电镜下观察断面的立体构型。该技术适于研究组织内部微细结构的相互关系,如肝细胞与肝血窦和胆小管的关系,肾小体的肾小囊与血管球的关系等(图1-17)。
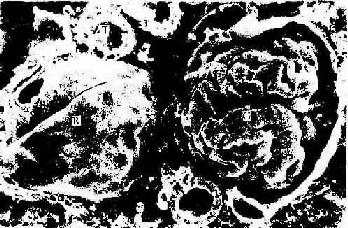
图1-17 大鼠肾冷冻割断扫描电镜示肾小体
R肾小囊外表面,G血管球,T肾小管
(白求恩医科大学尹昕、朱秀雄教授供图)
4、电镜X-射线显微分析术X-射线显微分析术(X-ray microanalysis)是研究细胞和组织内元素的种类、分布和含量的新技术。它是利用高速电子束轰击电镜内生物标本的微小区域,使该区所含的元素发射了一定波长的X-射线,通过检测器对X-射线进行波谱或能谱分析,即可测定微区内元素的性质、含量和分布。如测定细胞内Na、K、Ca、Fe、P、Cl等及某些微量元素的含量和分布变化,探讨各种元素与细胞生理和病理的关系。
(九)组织培养术
前述几种方法都是取人体或在体(in vivo)实验动物的组织,经固定等处理后,对已死亡的组织进行观察研究的。组织培养(tissue culture)或称体外实验(in vitro)则是取活组织或活细胞在体外适宜的环境中培养成活,进行实验研究。细胞在体外生存必须具有近似体内的生存条件,如充足营养供应,合理的O2与CO2比例,必要的电解质和适宜的渗透压,pH值、温度和湿度等,还需防止微生物污染。组织培养的特点在于可用研究各种理化因子(温度、激素、药物、毒物等)对活细胞的直接影响,并能观察记录(摄影、录像)。组织培养与前述方法结合应用,可研究某种因素对细胞增殖、分化、代谢、运动、吞噬、分泌等影响和调节的动态过程,以及细胞病变、癌变和逆转等机理,获得在体实验难达到的研究目的。
组织培养用液为平衡盐水及血清(小牛血清、胎盘血清等),羊水、腹水、组织浸出液等天然培养基(natural medium)。天然培养基成分复杂,且不稳定。目前广泛应用人工合成培养基(synthetic medium)现有多种商品供应,使用方便,但常仍需补充部分血清等。若仅用合成培养基和已制备好的几种必须因子与激素,称此为无血清培养基(serum-free medium),其成分和含量均是已知的,可精细研究某种因子对细胞的生物效应。
组织培养的方法甚多,常用容器有凹玻片、培养皿、培养瓶、培养板、流动小室等。取组织块贴于瓶底进行培养,可观察从组织块生长迁移出的细胞。取胚胎某器官原基或器官的一部分进行培养,称器官培养(organ culture)。更精细的方法是分离和纯化组织中的某种细胞,使之贴附在瓶底形成单层细胞(图1-18),称此为细胞培养(cell culture)。首次培养的细胞,称原代培养(primary cultrue;细胞增殖而密集再传代培养,称传代培养(subculture)。经长期培养而成的细胞群体,称细胞系(cell line);用细胞克隆(cell clone)或单细胞培养而建成的某种纯细胞群体,称细胞株(cell strain)。它们均可在液氮内长期冻存,供随时应用。现已建成多种肿瘤细胞株,广泛用于实验研究。
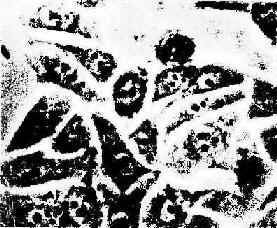
图1-18 体外培养的上皮细胞在相差显微镜下的图像(北京肿瘤研究所鄂征教授供图)
(十)细胞融合术
2个或2个以上的细胞融合成为一个细胞,称为细胞融合(cell fusion)。正常人体内也有细胞融合现象,如两性生殖细胞结合而成受精卵,多个巨噬细胞融合成一个体积很大的多核异物巨细胞。体外用人工方法使两种细胞融合,制成一种新品系的杂交细胞(hybrid cell),筛选出的此种杂交细胞有很强的生命力,增殖也很旺盛。常用的细胞融合诱导物是仙台病毒(Sendai virus)和聚乙烯二醇(polythyleneglycol,PEG)。细胞融合术是细胞遗传术、细胞免疫学、病毒学、肿瘤学等研究的一种重要手段,如将受抗原刺激后的小鼠脾淋巴细胞分离出来,与已建立的小鼠骨髓瘤(浆细胞瘤)细胞融合,筛选出的杂交瘤细胞可长期存活和增殖,成为制备单克隆抗体的细胞株。
三、组织学与胚胎学学习方法的几个要点
学习组织学与胚胎学应注意以下几方面:
1.平面与立体的关系切片和照片所显示的是细胞、组织和器官的平面结构,同一结构由于切面不同而呈现一定形态差异;通过细胞、组织、器官的平面结构的观察,还应建立对它们立体的整体结构的认识。因此应注意从平面结构的观察,树立整体结构的概念。一种传统的方法是将标本制成连续切片,观察记录每张切片中的结构,然后累积起来进行分析,或制成模型以表达其整体结构。目前则应用微机图像处理技术,在荧光屏上显示细胞和组织的三维重建图像。
2.结构与功能相联系每种细胞、组织和器官都有一定的形态结构特点。这些特点往往是它们行使一定功能的结构基础,两者密切相关。例如分泌蛋白质的腺细胞富有粗面内质网和发达的高尔基复合体,巨噬细胞则有较多的溶酶体;构成肌组织的肌细胞,形态细长,含有大量纵行肌丝,是细胞收缩的物质基础;上皮组织则细胞排列紧密,具有吸收和保护等功能相关结构。又如消化管是连续的管道,而食管、胃、小肠和大肠的粘膜又各有特点,它们与各段的相应功能相关。因此,结构与功能相结合既能达到深入理解,融会贯通,又可抓住要点,掌握规律。
3.从静态结构了解动态变化生活的细胞和组织是始终处于动态变化之中,在细胞分化,代谢和功能活动过程,其微细结构也有相应变化,细胞还不断增殖、运动、死亡和更新。即使是非细胞的间质成分包括坚硬的牙和骨的间质,也不断地被吸收和重建。胚胎时期的生长发育变化则更为显著。但在切片中所见的结构都是某一时刻的静态形象,所以要善于从组织的静态时相理解其动态变化。在动物实验中,可在不同实验时期取材观察,分析其动态过程。
4.纵横联系深化认识组织学从基本组织至各器官系统是阐述有机体统一整体的不可分割的部分,许多内容前后关联,相互印证。如细胞的结构与功能是组织学的基础,贯穿于全书始末;由细胞和细胞间质构成的各种组织组成不同的器官,器官的功能不仅建立在相关细胞特性的基础上,也与细胞间质及血管和神经的分布密切有关。又如细胞间连接结构不仅存在于上皮组织内,而且也分布在其它组织的细胞之间,并参与组织和器官的重要功能活动;淋巴细胞、内分泌细胞、神经细胞等更是在机体生命活动的整体网络中起广泛而重要的作用。
前已述及,现代医学和生物学研究进展迅速,使各学科的内容相互渗透和交叉,联系日益密切。组织学中研究方法的应用和许多基本理论的验证,都不可避免地要涉及其他学科的新技术和新成就,尤其是细胞生物学、分子生物学、免疫学、生物化学和生物物理学等。如细胞间连接、通讯及相互关系与调节,肌纤维的超微结构及其收缩机制的分子水平原理,血细胞发生中的造血干细胞学说的实验依据,淋巴细胞和抗原呈现递细胞的起源、分化及其在免疫应答中的抗原、抗体和受体的关系,许多新的内分泌细胞的发现和内分泌系统的展开,各种激素和调节因子的产生、作用及其相互关系,心血管、肺、肝、肾等器官一些细胞的结构和功能的新发现,神经元的信息传递与递质和受体的关系,生殖细胞的起源、分化和成熟等。随着组织学的进展,本书的修订在阐述基本内容的基础上,必然要有更新、充实和适当的扩展,有的内容以小字形式叙述,作为学习参考。因此在学习中应注意在掌握基本形态结构与功能的基础上,要善于自学钻研,扩充知识,纵横联系,深化认识,奠定坚实宽厚的基础,方能适应新世纪医药卫生事业发展的要求。