呼吸系统包括鼻、咽、喉、气管、支气管和肺等器官。从气管至肺内的肺泡,是连续而反复分支的管道系统。吸呼系统可分为导气部和呼吸部。导气部从鼻腔开始直至肺内的终末细支气管,无气体交换功能,但具有保持气道畅通和净化吸入空气的重要作用。鼻还有嗅觉功能,鼻和喉等又与发音有关。呼吸部是从肺内的呼吸细支气管开始直至终端的肺泡,这部分管道都有肺泡,行使气体交换功能。此外,肺还参与机体多种物质的合成和代谢功能 。
一、鼻腔
鼻以软骨和骨构成支架,表面的皮肤较厚,皮脂腺和汗腺较发达。为痤疮和疖的好发部位。鼻腔内面覆以粘膜,粘膜下方为软骨、骨或骨骼肌。鼻粘膜分前庭部、呼吸部和嗅部三部分。
(一)前庭部
前庭部(vestibular region)是邻近外鼻孔的部分。粘膜表面为复层扁平皮上皮,近外鼻孔处为角化型上皮,其余为未角化上皮。固有层为致密结缔组织。近外鼻孔的粘膜含鼻毛和皮脂腺,鼻毛无立毛肌。可阻挡胃吸入空气中的大尘粒。近呼吸部的粘膜固有层内有少量混合腺及弥散淋巴组织。
(二)呼吸部
呼吸部(respiratory region)的面积较大,占鼻粘膜的大部,包括下鼻甲、中鼻甲、鼻道及鼻中隔中下份等粘膜。生活状态的粘膜呈淡红色,表面为假复层纤毛柱状上皮,杯状细胞较多(图14-1)。上皮纤毛向咽部快速摆动,将粘液及粘着的尘粒推向咽部而被咳出。固有层结缔组织内有较多粘液腺、浆液腺和混合腺,分泌物经导管排入鼻腔,与上皮内杯状细胞分泌物共同形成一层粘覆于纤毛上。呼吸部粘膜的血液供应较丰富,并有丰富的静脉丛,中、下鼻甲处尤多,使粘膜形成许多小隆起。静脉丛管壁薄,腔大似窦状,它们随动静脉吻合的开放和关闭而有周期性充血变化,通过散热和渗出,对吸入空气起加温和湿润作用,患鼻炎时,静脉丛异常充血,粘膜肿胀,分泌物增多,鼻道变窄。固有层内淋巴组织较多,还可见嗜酸性粒细胞、嗜碱性粒细胞和肥大细胞,患过敏性鼻炎时,鼻分泌物中可见此类细胞。
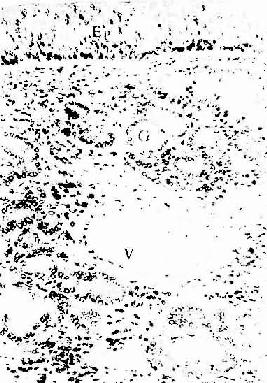
图14-1 人鼻呼吸部粘膜HE × 100
Ep假复层纤毛柱状上皮 G腺泡 V小静脉
(三)嗅部
嗅部(olfactory region)粘膜面积小,位于上鼻甲和相对的鼻中隔上份及鼻腔顶部,人两侧嗅粘膜的总面积约2cm2,某些动物的嗅粘膜面积大,如狗为100cm2。活体的嗅粘膜呈棕黄色,与淡红色的呼吸部分界明显.嗅粘膜表面的嗅上皮为假复层柱状上皮,无纤毛细胞和杯状细胞,由支持细胞、基细胞和嗅细胞组成(图14-2)。
1.支持细胞 细胞呈高柱状,顶部宽大,基部较细,游离面有许多微绒毛。核卵圆开,位于细胞上部,胞质内含有黄色色素颗粒。支持细胞分隔嗅细胞,使每个嗅细胞为一个功能单位,两者之间形成连接复合体,起支持和保护嗅细胞的作用。
2.基细胞 细胞呈圆形或锥形,位于上皮深部。细胞有细小突起,伸于上皮内其他细胞之间。基细胞有分裂和分化能力,能分化为支持细胞和嗅细胞。
3.嗅细胞 嗅细胞(olfactory cell)呈细长梭形,是一种双极神经元,它是唯一的一种存在于上皮内的感觉神经元。嗅细胞分散于支持细胞之间,人约有107个,狗有2.2×108。嗅细胞分胞体、树突和轴突三部分,含核的胞体部位于上皮的中部。顶部的树突呈细棒状,伸向上皮表面,突起末端膨胀大呈球状,称嗅泡(olfactory vesicle),从嗅泡伸出10~30根纤毛,称嗅毛(olfactory cilia)。嗅毛较长,向一侧倾倒,平铺在上皮表面,埋于较厚的浆液层内。嗅毛的结构不同于动纤毛,基内的微管无动力臂,故嗅毛无摆动性。胞体基部伸出细长轴突,穿过基膜,在固有层内由施万细胞包裹,形成无髓神经纤维,组成嗅神经(图14-2)。嗅神经穿过颅骨筛板,与嗅球内的神经元树突构成突触。嗅毛为嗅觉感受器,可能具有不同的受体,分别接受不同化学物质的刺激,使嗅细胞产生冲动,传入中枢,产生嗅觉。
嗅粘膜固有层为薄层结缔组织,与深部骨膜相连。固有层内的血管较丰富,并有许多浆液性嗅腺。嗅腺腺泡分泌的浆液经导管排至上皮表面,可溶解吸入空气中的化学物质,刺激嗅毛。浆液的不断分泌,又可清洗上皮表面,保持嗅细胞感受刺激的敏锐性。
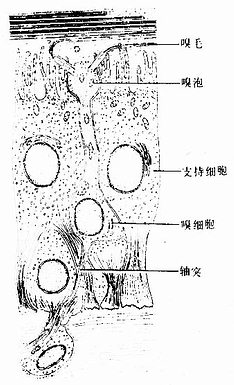
图14-2 嗅粘膜上皮细胞超微结构模式图
二、喉
喉以软骨为支架,软骨之间借韧带、肌肉或关节相连,会厌表面覆以粘膜,内部为会厌软骨(弹性软骨)。会厌舌面及喉面上份的粘膜上皮为复层扁平,有味蕾,喉面基部为假复层纤毛柱状上皮。固有层为疏松结缔组织,弹性纤维较丰富,并有混合腺和淋巴组织。固有层深部与会厌软骨的软骨膜相连。
喉侧壁粘膜形成上、下两对皱襞,分别为室襞和声襞。上、下皱襞之间为喉室(图14-3)。室襞粘膜表面为假复层纤毛柱状上皮,有杯状细胞,固有层和粘膜下层为疏松结缔组织,内有丰富的混合腺和淋巴组织。喉室的粘膜与粘膜下层的结构与室襞相似。声襞又称声带,游离缘为膜部,较薄,基部为软骨部。膜部粘膜表面为复层扁平上皮,固有层较厚,浅部为疏松结缔组织,炎症时易发生水肿;深部为致密结缔组织,富含与表面平行排列的弹性纤维,构成声韧带。固有层内无腺体,血管也较少,下方骼肌纤维构成的声带肌。声带振动主要在膜部。软骨部粘膜表面为假复层纤毛柱状上皮,粘膜下层内有混合腺,外膜有软骨和骨骼肌。
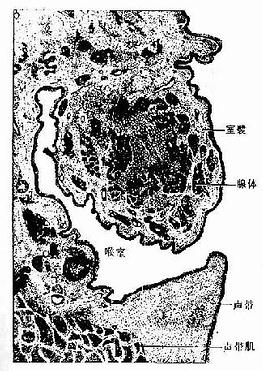
图14-3 喉纵切面
三、气管和支气管
(一)气管
气管管壁分粘膜、粘膜下层和外膜三层(图14-4)。

图14-4 人气管 HE×100
1.粘膜 表面为假复层纤毛柱状上皮,由纤毛细胞、杯状细胞、基细胞、刷细胞和弥散的神经内分泌细胞等组成(图14-5).纤毛细胞呈柱状,游离面有纤毛,每个细胞约有300根,核卵圆形,位于细胞中部。纤毛向咽侧呈快速摆动,将粘液及附于其上的尘粒,细菌等异物推向咽部被咳出,故纤毛细胞有净化吸入空气的重要作用(图14-6)。杯状细胞也甚多,其结构与肠道上皮的杯状细胞相似,顶部胞质内含大量粘原颗粒,细胞分泌的粘蛋白(mucin)是一种大分子糖蛋白,它与管壁内腺体的分泌物在上皮表面共同构成一道粘液性屏障,粘附吸入空气中的异物,溶解吸入的SO2、CO等有害气体,随粘液咳出。基细胞呈锥形,位于上皮深部,是一种未分化的细胞,有增殖和分化能力,可分化形成前述两种细胞。

图14-5 气管上皮超微结构模式图
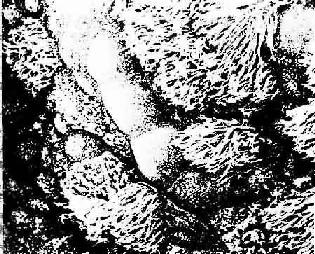
图14-6 大鼠气管上皮扫描电镜像
Ci纤毛(白求恩医科大学组织胚胎学教研室供图)
刷细胞(brush cell)呈柱状,游离面有许多排列整齐的微绒毛,形如刷状。刷细胞的功能尚不清楚,可能有一定吸收作用。细胞顶部可见基粒,因此认为它可能是一种未成熟的纤毛细胞。有的刷细胞基部可见与传入纤维构成的突触,故它还可能有感受刺激的功能。气管及其以下分支的导气部管壁上皮内还有弥散的神经内分泌细胞,细胞呈锥体形,散在于上皮深部,胞质内有许多致密核心颗粒,故又称小颗粒细胞(small granule cell)。免疫细胞化学研究证明,细胞内含有多种胺类或肽类物质,如5-羟色胺、蛙皮素、降钙素、脑啡肽等,分泌物可能通过旁分泌作用,或经血液循环,参与调节呼吸道血管平滑肌的收缩和腺的分泌。
固有层结缔组织中的弹性纤维较多,使管壁具有一定弹性。固有层内也常见淋巴组织,它与消化管管壁内的淋巴组织一样,也有免疫性防御功能。浆细胞分泌的IgA与上皮细胞产生的分泌片结合形成分泌性IgA,释放入管腔内,可抑制细菌繁殖和病毒复制,减弱内毒素的有害作用。
2.粘膜下层 为疏松结缔组织,与固有层和外膜无明显分界。粘膜下层除有血管、淋巴管和神经外,还有较多混合性腺。
3.外膜 为疏松结缔组织,较厚,主要有16~20个“C”形透明软骨环构成管壁支架,软骨环之间以弹性纤维组成的膜状韧带连接,使气管保持通畅并有一定弹性。软骨环的缺口朝向气管后壁,缺口处有弹性纤维组成的韧带和平滑肌束。咳嗽反射时平滑肌收缩,使气管腔缩小,有助于清除痰液。
(二)支气管
支气管管壁结构和功能与气管相似。气管分为左、右气管后,管径变细,管壁变薄,三层分界更不明显。支气管壁内的软骨环较少,形态也渐不规则,或环绕成环行,或体积变小呈不规则软骨片;平滑肌则逐渐增多,螺旋形排列,肌肉收缩有利于分泌物排出。
气管和支气管反复感染或受有害气体(如长期吸等)刺激,粘膜可发生慢性炎症病变。如纤毛细胞减少,纤毛运动减弱,杯状细胞增多,分泌旺盛;腺体也增生肥大,分泌增强,粘液糖蛋白成分也发生变化。以致呼吸道净化吸入空气的功能减弱,免疫性防御功能也受损害。病变严重者,假复层纤毛柱状上皮转变为复层扁平上皮,称为上皮化生。
四、肺
肺表面覆以浆膜(胸膜脏层),表面为间皮,深部为结缔组织。肺组织分实质和间质两部分,实质即肺内支气管的各级分支及其终端的大量肺泡,间质为结缔组织及血管、淋巴管和神经等。人的支气管(第1级)至肿泡约有24级分支。支气管经肺门入肺,分为叶支气管(第2级),右肺3支,左肺2支。叶支气管分为段支气管(第3~4级),左、右肺各10支。段支气管反复分支为小支气管(第5~10级)继而再分支为细支气管(第11~13级),细支气管又分支为终末细支气管(第14~16级)。从叶支气管至终末细支气管为肺内的导气部。终末细支气管以下的分支为肺的呼吸部,包括呼吸细支气管(第17~19级)、肺泡管(第20~22级)、肺泡囊(第23级)和肺泡(第24级)。支气管以下的这种分支管道,称支气管树(bronchial tree)。
每个细支气管连同它的分支至肺泡,组成一个肺小叶(pulmonary lobule)。肺小叶呈锥体形,尖向肺门,底向肺表面,小叶间为结缔组织间隔。胎儿肺小叶分界清楚,成人肺小叶分界不明显。但在肺表面仍可见小叶底部轮廓,直径约1~2.5cm,每叶肺约50~80个肺小叶。肺小叶是肺的结构单位,炎症仅累及若干肺小叶时为小叶性肺叶。
(一)肺导气部
肺导气部随分支而管径渐小,管壁渐薄,管壁结构也逐渐变化。
1.叶支气管至小支气管
管壁结构与支气管基本相似,但管径渐细,管壁渐薄,至小支气管的内径为2~3mm。管壁三层分界也渐不明显,其结构的主要变化是:①上皮均为假复层纤毛柱状,也含有前述几种细胞,但上皮薄,杯状细胞渐少;②腺体逐渐减少;③软骨呈不规则片状,并逐渐减少;④平滑肌相对增多,从分散排列渐成环形肌束环绕管壁(图14-7)。
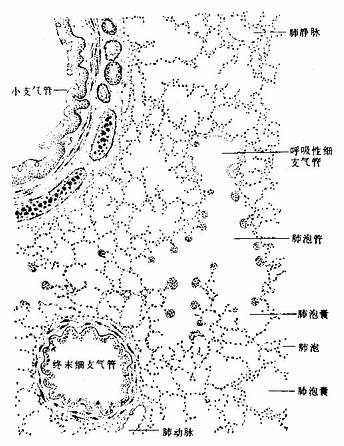
图14-7 肺
2.细支气管和终末细支气管 细支气管(bronchiole)内径约1mm ,上皮由假复层纤毛柱状渐变为单层纤毛柱状,也含有前述各种细胞,但杯状细胞减少或消失。腺和软骨也很少或消失,环行平滑肌则更明显,粘膜常形成皱襞。细支气管分支形成终末细支气管(terminal bronchiole),内径约0.5mm,上皮为单层柱状,无杯状细胞;腺和软骨均消失;环行平滑肌则更明显,形成完整的环行层,粘膜皱襞也明显(图14-7,14-8)。终末细支气管上皮内除少量纤毛细胞外,大部为无纤毛的柱状分泌细胞(称Clara细胞),细胞顶部呈圆顶状凸向管腔,顶部胞质内含分泌颗粒(图14-9)。一般认为分泌细胞的分泌物中含蛋白水解酶,可分解管腔内的粘液,利于排出;细胞内还含有较多的氧化酶系,可对吸收的毒物或某些药物进行生物转化,使其毒性减弱或便于排出。细支气管和终末细支气管的环行平滑肌,在植物神经的支配下收缩或舒张,以调节进出肺泡的气流量。正常情况下吸气时平滑肌松弛,管腔扩大;呼气末时,平滑肌收缩,管腔变小。在支气管哮喘等病理情况下,平滑肌发生痉挛性收缩,以致呼吸困难。
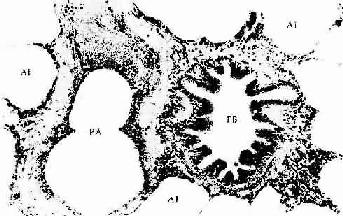
图14-8 人肺终末细支气管 HE ×400
TB终末细支气管 PA肺动脉分支 AI肺泡
图14-9 终末细支气管上皮细胞超微结构模式图
在叶支气管至细支气管的上皮内,常见神经内分泌细胞成群分布,5~10个细胞平行排列成卵圆形小体,尤多见于管道的分支处,称神经上皮小体(neuroepithelial body ,NEB),小体位于基膜上,顶端隆起突入管腔,或被其他上皮细胞覆盖。神经上皮小体的细胞分泌5-羟色胺、蛙皮素、生长抑素等胺类或肽类物质,通过旁分泌或血液循环,调节血管平滑肌舒缩,调整肺的通气,也参与调节腺体分泌和邻近上皮细胞的分泌与代谢活动。
(二)肺呼吸部
1.呼吸细支气管呼吸细支气管(respiratory bronchiole)是终末细支气管的分支,每个终末细支气管分出2支或2支以上呼吸细支气管。它是肺导气部和呼吸部之间的过渡性管道,管壁结构与终末细支气管相似。上皮为单层立方,也有纤毛细胞和分泌细胞;上皮下结缔组织内有少量环行平滑肌。呼吸细支气管不同于终末细支气管的是管壁上有肺泡相接,在肺泡开口处,单层立方上皮移行为肺泡的单层扁平上皮(图14-7,14-10)。从呼吸细支气管开始具有气体交换功能。
2.肺泡管 肺泡管(alveolar duct)是呼吸细支气管的分支,每个呼吸细支气管分支形成2~3个或更多个肺泡管。它是由许多肺泡组成,故其自身的管壁结构很少,仅存在于相邻肺泡开口之间,此处常膨大突入管腔,表面为单层立方或扁平上皮,上皮下为薄层结缔组织和少量平滑肌,肌纤维环行围绕于肺泡开口处,故在切片中可见相邻肺泡之间的隔(肺泡隔)末端呈结节状膨大(图14-7,14-10)。

图14-10 人肺示呼吸部 HE ×400
RB呼吸细支气管 AD肺泡管 AS肺泡囊 AI肺泡
3.肺泡囊 肺泡囊(alveolar sac)与肺泡管连续,,每个肺泡管分支形成2~3个肺泡囊。它的结构与肺泡管相似,也由许多肺泡围成,故肺泡囊是许多肺泡共同开口而成的囊腔。肺泡囊的相邻肺泡之间为薄层结缔组织隔(肺泡隔),在肺泡开口处无环行平滑肌,故在切片中的肺泡隔末端无结节状膨大(图14-7,14-10)。
4.肺泡 肺泡(pulmonary alveoli)是支气管树的终末部分,是构成肺的主要结构。肺泡为半球形小囊,开口于呼吸细支气管、肺泡管或肺泡囊,是肺进行气体交换的场所。肺泡壁很薄,表面覆以单层肺泡上皮,有基膜。相邻肺泡紧密相贴,仅隔以薄层结缔组织,称肺泡隔(图14-11)。成人每侧肺约有3亿~4亿个肺泡,总面积70~80m2。
(1)肺泡上皮:由Ⅰ型和Ⅱ型两种细胞组成(图14-11)。
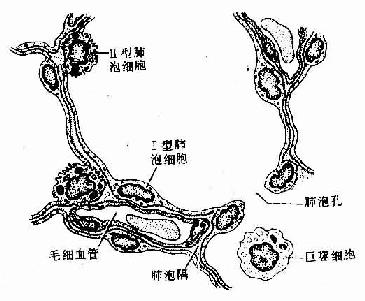
图14-11 肺泡与肺泡隔
Ⅰ型肺泡细胞(type Ⅰalveolar cell):细胞扁平,表面较光滑,含核部分略厚,其他部分很薄,厚约0.2μm,光镜下难辨认,电镜下清晰(图14-11,14-12)。Ⅰ型细胞数量较Ⅱ型细胞少,但宽大而扁薄,覆盖肺泡表面的绝大部分,参与构成气血屏障。相邻Ⅰ型细胞之间或Ⅰ型与Ⅱ型细胞之间有紧密连接。胞质内细胞器甚少,但吞饮小泡甚多,细胞以吞饮方式吞入吸入空气中的微小尘粒和上皮表面的表面活性物质,转运至间质内经淋巴转运和消除。Ⅰ型细胞无增殖能力,损伤后由Ⅱ型细胞增殖分化补充。
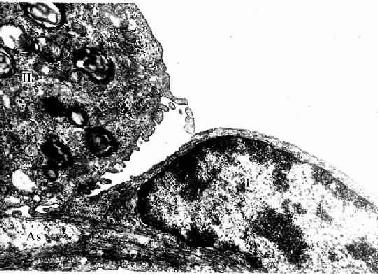
图14-12 猴肺泡电镜像 ×20800
Ⅰ Ⅰ型肺泡细胞,Ⅱ Ⅱ型肺泡细胞,Cap毛细血管 As肺泡隔
(白求恩医科大学尹昕、朱秀雄教授供图)
Ⅱ型肺泡细胞(type Ⅱalveolar cell):细胞较小,圆形或立方形,散在嵌于Ⅰ型细胞之间,细胞数量较Ⅰ型细胞多,但仅覆盖肺泡表面的一小部分。Ⅱ型细胞是一种分泌细胞,光镜观察下,核圆形,胞质着色浅,呈泡沫状,细胞略凸向肺泡腔(图14-11)。电镜下可见,细胞表面有短小微绒毛,胞质内除富含线粒体、粗面内质网、高尔基复合体和溶酶体外,还有许多分泌颗粒。颗粒大小不一,直径0.1~1μm ,电子密度高,内含同心圆或平行排列的板层结构,故称嗜锇性板层小体(osmiophilic multilamellar body)(图14-12)。免疫细胞化学和放射自显影证明,分泌颗粒内含磷脂、蛋白质和糖胺多糖等成分,由内质网合成的蛋白质在高尔基复合体内糖化,继而被组装在分泌颗粒内并与脂质结合(图14-13)。细胞以胞吐方式将颗粒内容物排出(图14-14),分泌物中的磷脂(主要是二棕榈酰卵磷脂)等成分在肺泡上皮表面铺展成一层薄膜,称表面活性物质(surfactant)。该物质在肺泡上皮表面与气体之间,形成的界面,有降低肺泡表面张力的作用,使肺泡回缩力降,减少吸气阻力,使吸气大为省力。此外,吸气末时肺泡扩大,表面活性物质分布稀薄,肺泡表面张力增大,回缩力增强,防止肺泡过于膨大;呼气末时肺泡缩小,表面活性物质相对浓厚,表面张力减小,肺泡回缩力减小,避免肺泡萎缩。故表面活性物质对稳定肺泡直径起重要作用。表面活性物质由Ⅱ型细胞不断产生,经Ⅰ型细胞吞饮转运或经呼吸道排出,保持不断的更新。Ⅱ型细胞还有分裂增殖并转化为Ⅰ型细胞的功能。
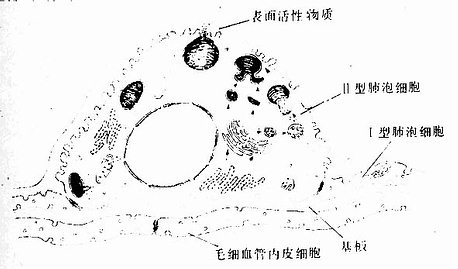
图14-13 Ⅱ型肺泡细胞超微结构模式图
↑示嗜锇性板层小体形成过程
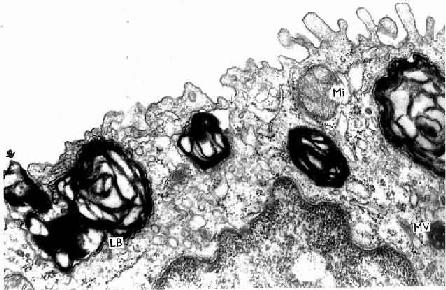
图14-14 人肺泡Ⅱ型细胞电镜像 ×42000
LB板层小体,Mi线粒体,MV多泡体,↑分泌
倘若早产儿或新生儿因先天缺陷而致肺表面活性物质产生不足或缺如,可使肺泡表面张力增大,扩张困难,导致新生儿呼吸窘迫症,患儿还因血氧不足,肺毛细血管通透性增大,血浆蛋白质漏出,在肺泡上皮表面沉积形成一层透明膜样物质,也影响肺泡的扩张和气体交换,故也称新生儿透明膜病。
(2)肺泡隔( alveolar septum):相邻肺泡之间的薄层结缔组织构成肺泡隔,属肺的间质。肺泡隔内含密集的毛细血管网,毛细血管为连续型,内皮甚薄,无孔,胞质内含较多吞饮小泡。隔的厚薄不一,弹性纤维较丰富,也有少量胶原纤维和网状纤维,并有成纤维细胞、巨噬细胞、浆细胞和肥大细胞等以及淋巴管和神经纤维。隔内丰富的弹性纤维有助于保持肺泡的弹性,老年人弹性纤维退化,炎症等病变也可破坏弹性纤维,使肺泡弹性减弱,肺泡渐扩大,导致肺气肿,肺换气功能减低。隔内的毛细血管大多紧贴肺泡上皮,上皮基膜与内皮基膜相互融合;有的部位的肺泡上皮与毛细管内有少量结缔组织(图14-15)。

图14-15 人肺泡隔电镜像 ×13500
Cap毛细血管,F成纤维细胞,
CO胶原原纤维,※基膜,↑Ⅰ型肺泡细胞
(上海医科大学电镜室供图)
(3)肺泡孔(alveolar pore):相邻肺泡之间有小孔相通、直径10~15μm(图14-11,14-16),一个肺泡可有一个或数个肺泡孔。它是沟通相邻肺泡的孔道,可均衡肺泡内气体的含量,在某个终末细支气管或呼吸细支气管阻塞时,肺泡孔起侧支通气作用,防止肺泡萎缩。但在肺感染时,病菌也可通过肺泡孔扩散,使炎症蔓延。

图14-16 人肺电镜像示肺泡孔 ×9000
A:肺泡腔,Ⅰ、Ⅱ肺泡上皮细胞(上海医科大学电镜室供图)
Cap毛细血管
(4)气血屏障(blood-air barrier):肺泡内气体与血液内气体分子交换所通过的结构称气血屏障。它由以下结构组成:肺泡表面液体层、Ⅰ型肺泡细胞与基膜、薄层结缔组织、毛细血管基膜与内皮。有的部位的肺泡上皮与血管内皮之间无结缔组织,两层基膜直接相贴而融合(图14-15)。气血屏障很薄,总厚度约0.5μm。间质性肺炎时,肺泡隔结缔组织水肿,炎症细胞浸润,以致肺气体交换功能障碍。
(三)肺间质和肺巨噬细胞
肺内的结缔组织及其中的血管、淋巴管和神经构成肺间质。结缔组织主要分布在支气管各级分支管道的周围,血管等行于其中,管道愈细,周围的结缔组织愈少,至肺泡,仅有少量结缔组织构成肺泡隔。肺间质的组成与一般疏松结缔组织相同,但弹性纤维较发达,巨噬细胞也较多。
肺巨噬细胞(pulmonary macrophage)由单核细胞分化而来,广泛分布在肺间质内,在细支气管以下的管道周围和肺泡隔内较多。有的巨噬细胞游走入肺泡腔内,称肺泡巨噬细胞(alveolar macrophage)。肺巨噬细胞的吞噬、免疫和分泌作用都十分活跃,有重要防御功能。吸入空气中的尘粒、细菌等异物进入肺泡和肺间质,多被巨噬细胞吞噬清除,故细胞胞质内常见尘粒、细菌等物进入肺泡和肺间质,多被巨噬细胞吞噬清除,故细胞胞质内常见尘粒、次级溶酶体及吞噬体等。胞质内含大量尘粒的肺巨噬细胞又称尘细胞(dust cell)。肺巨噬细胞还可吞噬衰老的红细胞,在心力衰竭患者出现肺瘀血时,大量红细胞从毛细血管溢出,被巨噬细胞吞噬,胞质内含许多血红蛋白的分解产物含铁血黄素颗粒,此种肺巨噬细胞又称心力衰竭细胞(heart failure cell)。吞噬异物的巨噬细胞,有的从肺泡腔经呼吸道粘液流动和纤毛运动而被咳出,有的进入肺淋巴管随淋巴进入肺淋巴结内。
(四)肺的血管、淋巴管和神经
1.肺的血管 肺有两组血循环管道,即肺循环和支气管循环。
(1)肺循环:肺循环是肺的功能性血循环。肺动脉为弹性动脉,它从肺门入肺后不断分支,与支气管的各级分支伴行,直至肺泡隔内形成密集的毛血管网(图14-17)。在肺泡处进行气体交换后,毛细血管汇集成小静脉,行于肺小叶间结缔组织内而不与肺动脉的分支伴行。小静脉汇集成较大的静脉后,才与支气管分支及肺动脉分伴行,最后在肺门入汇合成两条肺静脉出肺。

图14-17兔肺血管灌注示肺动脉分支及肺泡隔毛细血管网 ×400
↓肺动脉分支
(2)支气管循环:支气管循环是肺的营养性血循环。支气管动脉起自胸主动或肋间动脉,有数条,管径较细,为肌性动脉。支气管动脉沿途在肺导气部和呼吸细支气管管壁内,以及肺动脉、肺静脉管壁内和肺结缔组织内分支形成毛细血管,其内皮为有孔型,给肺组织提供营养.支气管也有终末支参与形成肺泡壁内的毛细血管网。上述毛细血管部分汇入肺静脉,部分汇集形成支气管静脉,与支气管伴行,由肺门出肺。支气管动脉还分支供应肺胸膜和肺淋巴结。
2.肺的淋巴管肺的淋巴管有浅丛和深丛两组。浅丛分布在肺胸膜内,淋巴丛汇合形成几支较大的淋巴管,将淋巴输入肺门淋结。深丛分布在肺支气管树的管壁内和肺泡隔内以及肺血管的周围,最后也汇合成几支淋巴管,将淋巴输入肺门淋巴结。
3.肺的神经肺的传出神经纤维(交感神经和副交感神经)和传入神经纤维在肺门形成丛(肺丛),神经纤维随支气管分支和血管分支入肺。传出神经末梢分布在支气管树平滑肌、血管平滑肌和腺体,交感神经纤维为肾上腺素能神经,兴奋时使支气管平滑肌松弛,血管平滑肌收缩,腺体分泌减少;副交感神经纤维为胆碱能神经,兴奋时使支气管平滑肌收缩,血管平滑肌松弛,腺体分泌增强。传入神经纤维末梢分布于支气管树管壁粘膜内及肺泡上皮,纤维出肺后行于迷走神经内,将肺内的刺激传入脑呼吸中枢。
(五)肺的代谢功能
前已述及,肺除有气体交换能外,支气管树上皮内还有弥散的神经内分泌细胞。近些年的研究还发现肺内进行着诸多物质代谢和转化作用,尤其表现在肺血管内皮细胞。全身血液均通过肺循环血管,故肺血管内皮细胞的代谢作用对机体的影响很大。内皮细胞游离面有血管紧张素转换酶,可将血液中血管紧张素Ⅰ转化为血管紧张素Ⅱ,后者的缩血管作用较前者强50倍。肺循环血内的血管紧张素Ⅰ绝大部分被转化为血管紧张素Ⅱ,它作用于中枢神经,通过交感神经的作用使体循环的小动脉收缩,升高血压。肺血管内皮细胞还含有缓激肽酶,可分解灭活血液中的缓激肽(它作用于神经系统使血管扩张),由此也使血管紧张,血压升高。肺内皮细胞内含有单胺氧化酶,细胞摄取血液中的5-羟色胺、去甲肾上腺素等,经此酶的作用而被分解灭活,肺是体内5-羟色胺灭活的主要场所。肺是产生和降解前列腺素(prostaglandin,PG)的重要器官,肺血管内皮细胞既能合成前裂腺素(PGE、PGF),又含有分解前列腺素的酶。PGE可使支气管平滑肌松弛,管腔扩大;PGF2α则使支气管平滑肌收缩,管腔缩小,还可使肿血管平滑肌收缩。肺间质结缔组织内的肥大细胞甚多,在变态反应疾病时,肥大细胞释放大量组胺等物质,可致支气管平滑肌收缩,粘膜水肿,腺体分泌粘液增多,发生支气管哮喘。