第一节 细胞免疫的概念
凡是由免疫细胞发挥效应以清除异物的作用即称为细胞免疫。参予的细胞称为免疫效应细胞。目前认为具有天然杀伤作用的天然伤细胞(NK)和抗体依赖的细胞介导的细胞毒性细胞(antibody dependentcell-mediatedcytotoxicity,ADCC)如巨噬细胞(Mφ)和杀伤细胞(K)以及由T细胞介导的细胞免疫均属细胞免疫的范畴。前二类免疫细胞在其细胞表面不具有抗原识别受体,,因此它们的活化无需经抗原激发即能发挥效应细胞的作用,故可视之为非特异性细胞免疫。而效应T细胞则具有抗原识别受体,因此它们必需经抗原激发才能活化发挥其效应细胞的作用,故可视之为特异性细胞免疫。
由T细胞介导的细胞的免疫有二种基本形式,它们分别由二类不同的T细胞亚类参予。一种是迟发型超敏性的T细胞(TDH,CD4+),该细胞和抗原起反应后可分泌细胞因子。这些细胞因子再吸引和活化巨噬细胞和其它类型的细胞在反应部位聚集,成为组织慢性炎症的非特异效应细胞。另一种是细胞毒性T细胞(TC,CD8+),对靶细胞有特异杀伤作用。
上述二种类型的效应T细胞的存在虽然均可经体外实验分别证实。但通常在体内反应过程中,二种类型的效应细胞均有不同程度的表现。
引起细胞免疫的抗原多为T细胞依赖抗原(TD抗原),与体液免疫相同,参予特异细胞免疫的细胞也是由多细胞系完成的。即由抗原呈递细胞(巨噬细胞或树突状细胞)、免疫调节细胞(TH和TS)以及效应T细胞(TDTH和TC)等。
在无抗原激发的情况下,效应T细胞是以不活化的静息型细胞形式存在。当抗原进入机体后,在抗原呈递细胞或靶细胞的作用下使静息型T细胞活化增殖并分化为效应T细胞。即由T细胞介导的细胞免疫应答也需经过抗原识别(诱导期)、活化与分化(增殖期)和效应期才能发挥细胞免疫作用。
由T细胞介导的主要细胞免疫现象有:①迟发型超敏性反应;②以胞内寄生物的抗感染作用;③抗肿瘤免疫;④同种移植排斥反应;⑤移植物抗宿主反应;⑥某些药物过敏症;⑦某些自身免疫病。
第二节 CD4+T细胞介导的细胞免疫
这是由CD4+T细胞激发的特异性细胞免疫应答,它可引起组织的慢性炎症,它是以淋巴细胞(主要是T细胞)和单核吞噬细胞系细胞浸润为主的渗出性炎症。
由于免疫细胞的激活、增殖和分化以及其它炎症细胞的聚集需要较长时间,所以炎症反应发生较迟,持续时间也长,故称此种炎症的反应为迟发型超敏反应(delayedtypehy persensitiyty,DTH)。诱发这种的反应的T细胞称为迟发型超敏性T细胞(TDTH)。
这种由CD4+T细胞介导的细胞免疫与临床传染性变态反应、接触性皮炎、移植排斥反应以及一些自身免疫病的组织损伤有关。
一、CD4+T细胞在DTH反应中的作用
Chase(1942)应用已被抗原致敏的豚鼠的淋巴细胞转移给正常豚鼠,然后用致敏抗原经皮内攻击,可引起皮肤的DTH反应,而用致敏豚鼠血清转移不能引起DTH反应,首先证明了细胞免疫存在的事实。在无丙种球蛋白患者,即体液免疫缺损患者亦可产生DTH反应,在人体内也证明了DTH反应与抗体无关。
其后在小鼠内证明参予这种反应的淋巴细胞是Lyt-1+T细胞(与人CD4+T细胞相当),其表型与辅助性T细胞(TH)相同,并且两者在识别抗原的MHC限制性上也相同。但两者在功能上完全不同,前者介导细胞免疫,而后者则参予体液免疫。近年的研究证明小鼠CD4+T细胞根据其合成和分泌的细胞因子不同,可分为TH1和TH2两种亚类。TH1介导细胞免疫,TH2参予体液免疫。
二、CD4+T细胞的活化
CD4+T细胞的活化需有抗原呈递细胞参予,主要为巨噬细胞(MФ),其次表皮内的Langerhans细胞和血管内皮细胞亦可发挥抗原呈递细胞的作用(图12-1)。
实验证明,经亚致死量X射线照射的动物只有当输入淋巴细胞和骨髓干细胞(供给巨噬细胞的来源)时才能引起DTH反应。
巨噬细胞在DTH反应中可发挥两方面作用,首先在诱导期它具有呈递抗原的作用,在效应期非致敏的巨噬细胞在活化的CD4+T细胞释放的细胞因子作用下,可成为DTH中重要的炎症细胞。
巨噬细胞通过吞噬或吞饮作用,将外源性蛋白质抗原摄取进入胞内,,经加工后产生的抗原肽片段与其自己MHCⅡ类分子结合形成复合物,然后运送至细胞表面并呈递给CD4+T细胞,自此开始了CD4+T细胞活化的诱导期。
CD4+T细胞活化需有双信号刺激,即其抗原识别受体(TCRαβ)与抗原呈递细胞上的肽-MHCⅡ的复合物结合后,可通过CD3复合分子传递第一信号。CD4+T细胞上其它辅助分子如CD2、LFA-1、CD4及CD28等分子可与APC上相应的配体分子如LFA-3、ICAM-1、MHCⅡ及B7分子等结合,不仅增强了CD4+T细胞与APC间的粘附作用,同时可向CD4+T细胞传递协同刺激信号(Costimulatory Signal)使之活化并产生多种细胞因子,它们既能促进CD4+T细胞克隆的扩增又是CTH反应的分子基础。如无辅助信号发生则CD4+T细胞处于不应答(anergy)状态。
三、迟发型超敏性炎症的形成
CD4+T细胞经抗原识别、活化和克隆增殖并合成和分泌大量各种细胞因子,其中最重要的有白细胞介素-2(IL-2)、肿瘤坏死因子(TNF)、淋巴毒素(LT)和干扰素(IFN-γ)等,它们是产生DTH反应的分子基础。
(一)IL-2
抗原活化的T细胞可借其IL-2的自分泌和旁分泌作用促进T细胞增殖,其中包括抗原特异的T细胞和邻近的旁路T细胞(bystandercell)。当淋巴细胞大量渗出时,在抗原攻击部位出现的T细胞90%以上是旁路T细胞。IL-2除能刺激t 细胞增殖外,还能促使CD4+T细胞合成细胞因子,其中包括IL-2、TNF、TFN-γ和淋巴毒素(LT)等。特别在DTH晚期LT分泌量可大于TNF。
(二)IFN-γ
由CD4+T细胞分泌的IFN-γ可作用于抗原呈递细胞如巨噬细胞和内皮细胞,增加它们MHCⅡ类分子的表达。可提高其呈递抗原效率。这是又一种重要的诱导DTH反应的放大机制。
(三)TNF和LT
肿瘤坏死因子和淋巴毒素可作用于血管内皮细胞使之表达粘附分子和分泌趋化性细胞因子如IL-8等。这些分子有利于吸引血流内白细胞如中性粒细胞、淋巴细胞以及单核细胞等与血管内皮粘附并迁移和外渗至组织内引起组织炎症反应(图12-2)。IFN-γ和IL-4对内皮细胞也有类似的作用。
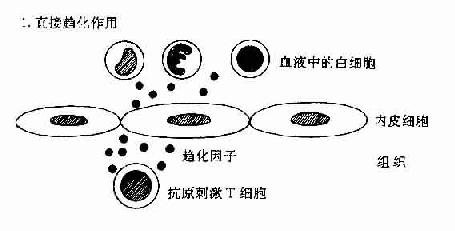
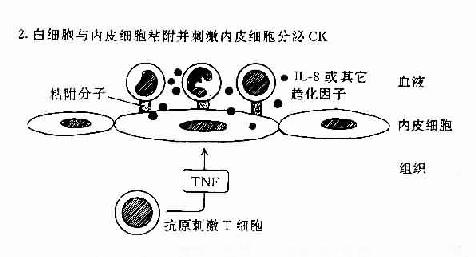
图12-2 DTH反应中动员白细胞的机制:T细胞和内皮细胞所起的作用。
T细胞可分泌作用于白细胞的趋化因子;或分泌TNF,它可增加内皮细胞-白细胞粘附分子的表达,并刺激内皮细胞分子分泌CK(如IL-8)促使白细胞游走至组织中。
(四) 自血流经内皮细胞渗出的单核细胞进入炎症部位的组织后,在细胞因子的作用下可分化为巨噬细胞,此过程可称之为巨噬细胞活化。IFN-γ是强有力的巨噬细胞活化因子,只有活化的巨噬细胞才具有杀伤胞内的微生物、杀伤肿瘤细胞的功能,而静息的单核细胞是无这些功能的。所以活化的巨噬细胞是DTh 反应中主要的清除抗原和引起炎症的效应细胞。
活化的巨噬细胞可分泌许多引起炎症的细胞因子的生长因子。如其分泌的TNF、IL-1和IL-6在急性期可通过其作用于T细胞,炎症细胞和内皮细胞以增强其细胞介导的免疫反应引起局部组织损伤。在慢性期则可刺激纤维母细胞增生和产生胶原纤维,其分泌的PDGF和TGF-β可增强这种作用。此过程称为纤维化是DTH反应的最终结局。
在慢性DTH反应中,活化巨噬细胞自身可发生变化,其胞浆和胞浆内细胞器有所增加,其形态类似皮肤上皮细胞,故称为上皮样巨噬细胞。有时它们融合形成多核巨细胞。在一些持久性细胞内细菌感染如结核杆菌感染形成的簇状活化巨噬细胞是一种可触知的结节性炎症组织称之为肉芽肿。这种内芽肿性炎症是慢性DTH的一种形成。
总之,急性DTH反应细胞介导免疫的形成之一。它的发生首先是CD4+T细胞识别可溶性蛋白质抗原或CD8+T细胞识别胞内的微生物衍生物抗原和对活化T细胞产生的细胞因子应答的结果。
在细胞因子中特别是TNF可活化衬里毛细血管后静脉的内皮细胞,它可吸引血流中中性粒细胞、淋巴细胞和单核细胞外渗至局部组织内引发炎症。其后IFN-γ可作用于聚集的单核细胞使之活化为具有杀伤功能和清除抗原能力的巨噬细胞,成为DTH的最终效应细胞。
如抗原刺激持久存在,则巨噬细胞可长期活化并继发分泌细胞因子和生长因子,造成组织纤维化形成慢性DTH反应。
在早期DTH反应中以活化CD4+T细胞和活化巨噬细胞浸润为主,这些细胞和聚集在活化的血管内皮细胞周围并外渗至局部组织内。在晚期慢性DTH反应中以簇状上皮样巨噬细胞和巨细胞为主并伴有大量纤维母细胞形成组织纤维化以替原有组织(图12-3)
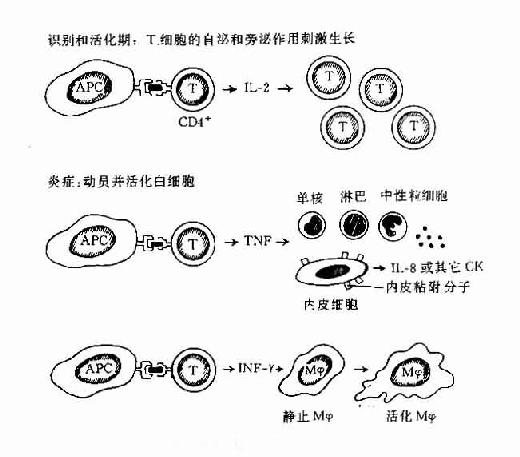
图12-3 DTH反应的过程
DTH开始由T细胞识别APC表面与MHC分子结合的抗原,这种细胞可以是CD4+T也可以是CD8+T细胞;由T细胞分泌的不同的CK在DTH不同阶段起不同的作用。
第三节 CD8+T(TC)T细胞介导的细胞免疫
CD8+T细胞(TC或CTL细胞)能杀伤表达抗原的靶细胞,它在抗毒感染、急性同种异型移植物排斥和对肿瘤细胞的杀伤作用是重要的效应细胞。
绝大多数TC细胞表达CD8分子,其抗原识别受体(TCRαβ)可识别多肽抗原与自己MHCⅠ类分子形成的复合物。这些非已多肽抗原是在靶细胞内合成经加工后与自己MHCⅠ类分子结合并运送到靶细胞表面的。少数TC细胞可表达CD4分子并识别和自己MHCⅡ类分子的结合的多肽抗原(图12-4)
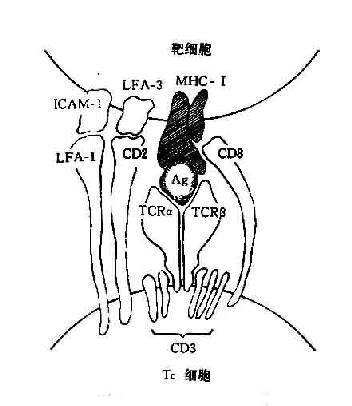
图12-4 TC细胞抗原识别
一、CD8+T(TC)T细胞的活化
在正常机体中TC细胞以不活化的静息T细胞的形式存在。因此它也必须经过抗原激活并在T辅助(TH)协同作用下,才能分化发育为效应杀伤T细胞(TC)。
杀伤T细胞(TC)的活化也需要双信号,即TCR与靶细胞膜上MHC类分子与抗原肽分子复合物结合后,可通过CD3复合分子传递第一信号;而TC细胞上的其它辅助分子(accesssory molecules)如CD2,LFA-1、CD8及CD28分子等可与靶细胞上相应的配体分子如LFA-3、ICAM-1、MHCⅠ类分子及B7分子等结合,不仅可增强TC细胞与靶细胞的粘附作用,同时也向TC细胞传递协同信号(costimulatorysignal)使之活化。在活化CD4+T细胞分泌的细胞因子(如IL-2)作用下使之克隆增殖并分化为效应杀伤T细胞(TC)(图12-5)。
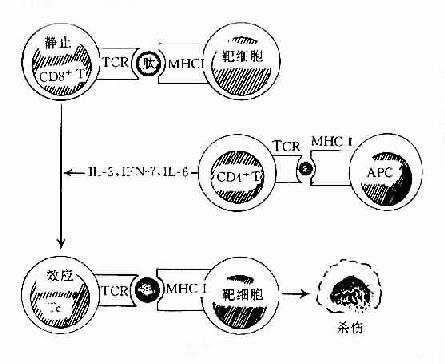
图12-5 T细胞的发生
二、TC细胞杀伤靶细胞的机制
杀伤T细胞对靶细胞的杀伤作用是抗原特异性的,只杀伤相应靶细胞而对其它细胞无损伤作用。杀伤T细胞必需与靶细胞直接触才有杀伤作用。当靶细胞被溶解时,TC细胞本身不受损伤并与之解离,因此一个杀伤T细胞可连续杀伤多个靶细胞,其杀伤机制可能是其分泌的多种细胞毒素所致。
(一)穿孔素蛋白(perferin)
杀伤T细胞活化后可诱发脱颗粒作用,排出其胞浆颗粒内已合成的一种蛋白质——穿孔素。这种蛋白在颗粒内是单体,当与胞外高浓度Ca2+接触后即发生聚合。这种聚合多发生在靶细胞膜的脂质层,并形成离子透过通道,因之大量离子和水分可进入细胞造成细胞溶解。这种细胞溶解作用类似于补体的膜攻击复合物的作用,并且穿孔蛋白的结构也与C9有同源性。此外,颗粒中的其它成分如丝氨酸酯酶和蛋白聚糖也有损伤细胞的作用。
(二)细胞毒素
杀伤T细胞可泌一种蛋白质毒素,它与颗粒内的物质不同,而类似于淋巴毒素的物质。这种细胞毒素可活化靶细胞内的DNA降解酶,导致靶细胞核DNA的裂解,引起靶细胞的程序性死亡(Programmed cell death,PCD)。
由TC细胞分泌的细胞毒素引起的靶细胞死亡并不出现由于渗透压增高引起的细胞膨胀导致的细胞溶解。而穿孔蛋白杀伤靶细胞也不引起DNA裂解导致的细胞程序性死亡。这两种杀伤机制在TC的杀伤作用中可能是互补的(图12-6)。
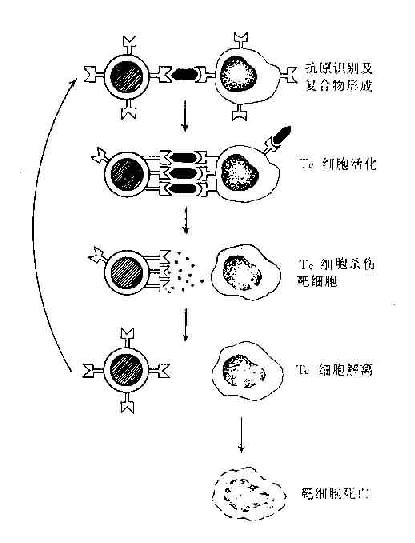
图12-6 T细胞杀伤靶细胞过程