呼吸的主要功能是不断地给机体提供氧气和从机体排出多余的二氧化碳
■[此处缺少一些内容]■
);根据主要的发病机制不同,也可将呼吸衰竭分为通气性和换气性两大类;根据原发病变部位不同又可分为中枢性和外周性;根据病程经过不同还可将呼吸衰竭分为急性和慢性。
1kPa=7.5006mmHg,下同。
第一节 呼吸衰竭的病因
很多疾病都能直接或间接影响肺的呼吸功能而导致呼吸衰竭。重要的病因如下:
一、神经系统疾病
(一)中枢或周围神经的器质病变 如脑或脊髓外伤、脑肿瘤、脑血管意外、脑部感染、脑水肿、脊髓灰质炎、多发性神经炎等。
(二)呼吸中枢抑制如镇静药、安眼药或麻醉药过量等。
二、骨骼、肌肉和胸膜疾病
(一)胸廓骨骼病变 如脊柱后侧凸、多发性肋骨骨折等。
(二)呼吸肌活动障碍如重症肌无力症、有机磷中毒、多发性肌炎、肌营养不良、低钾血症以及腹压增大或过度肥胖膈肌活动受限等。
(三)胸膜病变如胸膜纤维化、胸腔大量积液、张力性气胸等。
三、肺和气道的疾病
(一)气道病变 如异物、肿瘤、炎症使中央气道狭窄或阻塞。更为多见的是细支气管炎、支气管哮喘、慢性支气管炎、慢性阻塞性肺气肿等引起的外周气道阻塞。
■[此处缺少一些内容]■
第二节 呼吸衰竭的发病机制
外呼吸包括通气和换气两个基本环节。各种病因不外乎通过引起肺泡通气不足、弥散障碍、肺泡通气与血流比例失调、肺内短路增加等机制,使通气和/或换气过程发生严重障碍而导致呼吸衰竭。不同的病因常通过相似的机制引起呼吸衰竭,因而使不同病因引起的呼吸衰竭具有共性;但由于病变的部位、性质以及机体反应性不同,故其发病又往往存在特殊性。
一、肺泡通气不足
肺泡通气量即有效通气量,正常成人静息时约为4L/min。除死腔通气量增加可直接减少肺泡通气量外,凡能减弱呼吸的动力或增加胸壁与肺的弹性阻力或非弹性阻力的任何原因,都可引起肺泡通气不足而导致呼吸衰竭。
(一)限制性通气不足
肺泡扩张受限制所引起的肺泡通气不足称为限制性通气不足(restrictivehypoventilation),其发生机制如下:
1.呼吸肌活动障碍当脑部病变或药物使呼吸中枢受损或抑制,或神经肌肉疾患累及呼吸肌时,均可因吸呼肌收缩减弱或膈肌活动受限,以致肺泡不能正常扩张而发生通气不足。呼吸肌的病变往往需同时累及肋间肌和膈肌时才会引起明显的血气变化。
2.胸壁和肺的顺应性降低呼吸肌收缩使胸廓与肺扩张时,需克服组织的弹性阻力,肺的弹性回缩力使肺趋向萎陷(collapse)。胸廓的弹性在静息呼气末时是使胸廓扩大的力量,但当吸气至肺活量的75%以上时,胸廓对吸气也构成弹性阻力。故弹性阻力的大小直接影响肺与胸廓在吸气时是否易于扩张。肺与胸廓扩张的难易程度通常以顺应性(Compliance)表示,它是弹性阻力的倒数。
胸廓顺应性降低见于胸廓骨骼病变或某些胸膜病变时。肺顺应性除直接与肺容量有关(肺容量小,肺顺应性也低)外,主要取决于其弹性回缩力。肺泡的弹性回缩力是由肺组织本身的弹性结构和肺泡表面张力所决定。肺淤血、水肿、纤维化等均可降低肺的顺应性,增加吸气时的弹性阻力。肺泡表面张力有使肺泡回缩的作用。生理情况下,由肺泡Ⅱ型上皮细胞产生的表面活性物质覆盖于肺泡、肺泡管和呼吸性细支气管液层表面,它能降低肺泡表面张力。降低肺泡回缩力,提高肺顺应性,维持肺泡膨胀的稳定性。它与维持肺泡的干燥也有关。Ⅱ型肺泡上皮受损(如循环灌流不足、氧中毒、脂肪栓塞)或发育不全(婴儿呼吸窘迫综合征)以致表面活性物质的合成与分泌不足,或者表面活性物质被大量破坏或消耗(如急性胰腺炎、肺水肿、过度通气)时,均可使肺泡表面活性物质减少,肺泡表面张力增加而降低肺顺应性,从而使肺泡不易扩张而发生限制性通气不足。
限制性通气不足时,由于病变往往并不均匀对称,故不仅有肺泡通气不足,而且往往伴有肺泡通气与血流比例失调,故换气功能也遭到损害(详后文)。
(二)阻塞性通气不足
气道狭窄或阻塞引起的肺泡通气不足称为阻塞性通气不足(obstructivehypoventilation)。气道阻力是通气过程中主要的非弹性阻力,正常约为0.1~0.3kPa(1~3cmH2O)/L·sec-1呼气时略高于吸气时。其中80%以上发生于直径大于2mm的支气管与气管,直径小于2mm的外周小气道的阻力仅占总阻力的20%以下。
影响气道阻力的因素有气道内径、长度和形态、气流速度和形式(层流、湍流)、气体的密度和粘度,其中最主要的是气道内径。气道内外压力的改变,管壁痉挛、肿胀或纤维化,管腔被粘液、渗出物、异物或肿瘤等阻塞,肺组织弹性降低以致对气道管壁的牵引力减弱等,均可使气道内径变窄或不规则而增加气流阻力,引起阻塞性通气不足。气道阻塞有中央性外周性两类:
1.中央气道阻塞指声门至气管隆凸间的气道阻塞。急性阻塞较慢性的多见,可立即威胁生命。气道阻塞有的是固定不变的,有的是可变的。固定阻塞见于疤痕形成。可变阻塞若位于胸外(如声带麻痹、炎症等),则吸气时气流经病灶引起的压力下降,可使气道内压明显小于大气压,故可使气道狭窄加重;呼气时则因气道内压力大于大气压而可使阻塞减轻,故此类患者吸气更为困难,表现出明显的吸气性呼吸困难。可变阻塞如位于中央气道的胸内部分,则由于吸气时气道内压大于胸内压,故可使阻塞减轻,用力呼气时则可因胸内压大于气道内压而加重阻塞(图13-1)。
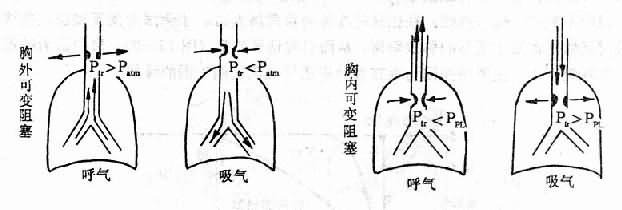
图13-1 不同类型中央气道阻塞呼气与吸气时气道阻力变化
Ptr气管内压;Patm大气压;Ppl胸膜腔压
2.外周气道阻塞 内径小于2mm的细支气管无软骨支撑,管壁薄,与管周的肺泡结构又紧密相连,因此随着吸气与呼气,由于跨壁压的改变,其内径也发生动力学变化。吸气时胸内压降低,而且随着肺泡的扩张,细支气管受到周围弹性组织的牵拉,故其口径可变大,管道伸长。呼气时则相反,小气道缩短变窄。慢性阻塞性肺疾患主要侵犯这些小气道,不仅可使管壁增厚或平滑肌紧张性升高和管壁顺应性降低,而且管腔还可因分泌物潴留而发生狭窄阻塞;此外,由于肺泡壁损伤,对细支气管周围的弹性牵引力也大大减弱。因此,管腔也变得狭窄而不规则,气道阻力大大增加。尤其是在用力呼气时,由于胸内压增高,而小气道内压力却因肺泡弹性回缩力减弱而降低,当气流通过狭窄部位时,气道内压降低更加明显,甚至低于胸内压,因而小气道被压而易于闭合阻塞,故患者常发生呼气性呼吸困难。
外周气道阻塞时除有肺泡通气不足外,还因为阻塞的部位与程度几乎都是不均匀的,所以往往同时有肺泡通气与血流比例失调而引起换气功能障碍。
二、弥散障碍
肺泡与血流经肺泡-毛细血管膜(下简称肺泡膜)进行气体交换的过程是一个物理性弥散过程。单位时间内气体的弥散量取决于肺泡膜两侧的气体分压差、肺泡的面积与厚度和气体的弥散常数。弥散常数又与气体的分子量和溶解度相关。此外,气体总弥散量还决定于血液与肺泡接触的时间。肺的病变引起弥散障碍(diffusion impairment)可发生于下列情况:
(一)肺泡膜面积减少 正常成人肺泡总面积约为80m2,静息呼吸时参与换气的肺泡表面积约仅35~40m2,运动时增加。由于储备量大,因此只有当肺泡膜面积极度减少时,才会引起换气功能障碍,肺泡膜面积减少可见于肺实变、肺不胀、肺叶切除等时。
(二)肺泡膜厚度增加肺泡膜的薄部为气体交换的部位,它是由肺泡上皮、毛细血管内皮及二者共有的基底膜所构成,其厚度小于1μm。虽然气体从肺泡腔到达红细胞内还需经过肺泡表面的液体层、管内血浆层和红细胞膜,但总厚度也不到5μm。故正常气体交换是很快的。当肺水肿、肺泡透明膜形成、肺纤维化、肺泡毛细血管扩张或稀血症导致血浆层变厚等时,都可因肺泡膜通透性降低或弥散距离增宽而影响气体弥散。
(三)血液与肺泡接触时间过短 正常静息时,血液流经肺泡毛细血管的时间约为0.75sec,由于肺泡膜很薄,与血液的接触面又广,故只需0.25sec血红蛋白即可完全氧合。当血液流经肺泡毛细血管的时间过短时,气体弥散量将下降。上述肺泡膜面积减少和厚度增加的病人,虽然肺毛细血管血液中氧分压上升较慢,但一般在静息时肺内气体交换仍可达到平衡,因而不致产生低氧血症,往往只是在体力负荷增大时,才会因为血流加快,血液和肺泡接触时间缩短而发生明显的弥散障碍,从而引起低氧血症(图13-2)。目前认为肺泡膜病变时发生呼吸衰竭,主要还是因为存在着肺泡通气血流比例失调的缘故。
三、肺泡通气与血流比例失调
有效的换气不仅取决于肺泡膜面积与厚度、肺泡总通气量与血流量,还要求肺泡的通气与血流配合协调。肺部疾病时肺的总通气量与总血流量有时可以正常,但通气与血流的分布不均匀以及比例的严重失调(ventilation-perfusion imbalance)却可使患者不能进行有效的换气。这是肺部疾病引起呼吸衰竭最常见的机制。
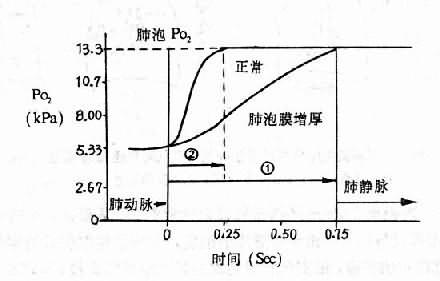
图13-2 正常人与肺泡膜增厚时肺循环中血红蛋白氧合的时间过程
①休息时红细胞经过肺毛细血管的时间;
②运动时红细胞经过肺毛细血管的时间
正常人在静息状态下,肺泡每分通气量(VA)每分约为4L,肺血流量(Q)约为每分5L,二者的比率(VA/Q)约为0.8左右。但是即使在健康人,肺的各部分通气与血流的分布也都不是均匀的。直位时,肺泡的通气量和血流量都是自上而下递增的,而血流量的上下差别更大,其结果是各部肺泡的V/Q比率自上而下递减。在正常青年人VA/Q比率的变动范围自上而下约为0.6~3;随着年龄增大,变动范围扩大。尽管如此,PaO2和PaCO2最终仍可维持在正常范围。肺部疾病时,若肺泡通气不足与血流量减少发生于同一部位(如肺叶切除、大叶性肺炎灰色肝变期),其功能可由其余的健肺以适当的比例加强通气与血流来代偿,因而对换气功能影响可以不大。但大多数呼吸系统疾病时肺泡通气和血流量的改变多不相平行配合,使部分肺泡V/Q比率降低或增高,而且VA/Q比率的变动范围也扩大,因而使肺泡通气血流比例严重失调,不能保证有效的换气而导致呼吸衰竭。肺泡通气血流比例失调有两种基本形式:
(一)部分肺泡V/Q比率降低支气管哮喘、慢性支气管炎、阻塞性肺气肿等引起的气道阻塞或狭窄性病变,以及肺与胸廓顺应性降低在肺的各个部分所造成的影响,往往都不是均匀一致,而是轻重不一的。因此都可导致肺泡通气分布的严重不均。如肺泡通气明显降低而血流无相应减少甚至还增多,即VA/Q比率降低,则流经这部分肺泡的静脉血未经充分氧合便掺入动脉血内。这种情况类似肺动-静脉短路,故称功能性分流增加。正常成人由于肺内通气分布不均形成的功能性分流约仅占肺血流量的3%。慢性阻塞性肺疾患严重时,功能性分流明显增加,可相当于肺血流量的30~50%,因此可以严重地影响换气功能而导致呼吸衰竭(图13-3(3))。
(二)部分肺泡V/Q比率增高某些肺部疾患,如肺动脉压降低、肺动脉栓塞、肺血管受压扭曲和肺壁毛细血管床减少等时,VA/Q比率增高。患部肺泡血流少而通气多,吸入的空气没有或很少参与气体交换,因而与气道的情况类似,即犹如增加了肺泡死腔量,故这种情况又称死腔样通气。此时肺脏总的有效通气量必然减少,因而也会引起血气异常。正常人的生理死腔量(VD)约占潮气量(VT)的30%,上述疾病时可使死腔气量明显增多,VD/QT可高达60~70%(图13-3(4))。
总之,在通气分布不均或血流分布不均以及通气和血流配合不当时,有的肺泡通气与血流比率明显降低,可低至0.01;有的肺泡通气血流比率明显增高,可高达10以上,也有的仍接近0.83,各部分肺泡的V/Q比率的变动范围明显扩大,严重偏离正常的范围。这样就可引起换气障碍并从而导致呼吸衰竭。
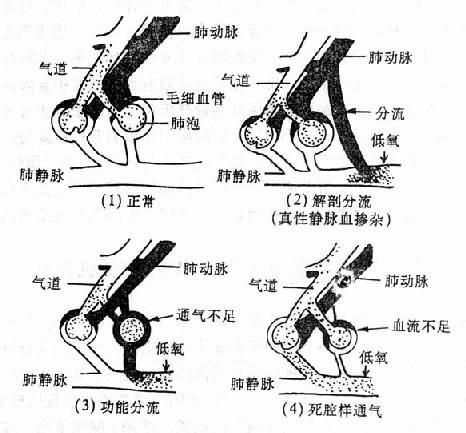
图13-3 肺泡通气与血流比例失调模式图
四、肺循环短路增加
生理情况下肺内有一部分静脉血经支气管静脉和极少数的肺内动-静脉交通支直接流入肺静脉,称“短路”(shunt)或右-左分流。此外,心内最小静脉的静脉血也直接流入左心。这些都属解剖分流,其血流量约占心输出量的2~3%。因为静脉血未经动脉化即掺入动脉血中,故又称静脉血掺杂。支气管扩张(伴支气管血管扩张)、先天性肺动脉瘘、肺内动静脉短路开放等病变,可增加解剖分流,使静脉血掺杂显着增多而引起血液气体异常(图13-3(2))。有人将肺内病变所引起的肺泡完全不通气但仍有血流者也视为短路,见于肺实变、肺不张等。
呼吸衰竭的发病机制中,单纯的通气不足、单纯的弥散障碍、单纯的肺内短路增加或单纯的肺泡通气与血流比例失调是较少的,这些因素往往同时存在或相继发生作用。现以成人呼吸窘迫综合征(adult respiratory distress syndrome, ARDS)为例概要说明之。
成人呼吸窘迫综合征是在原无心肺疾患的病人因急性弥漫性肺泡-毛细血管膜损伤,以致外呼吸功能严重障碍而发生的急性呼吸衰竭,常见于休克、创伤、败血症、过量输液、体外循环术和氧中毒等时。其早期病变主要为肺严重水肿、出血、透明膜形成、肺不胀、微血栓形成、肺血管内皮细胞及肺泡Ⅰ型上皮细胞肿胀变性与坏死等。此时呼吸衰竭的发生可有下述多种机制参与:①由于肺水肿、肺不胀等使肺顺应性降低而引起限制性通气障碍,也可因支气管痉挛和气道内液体增加而导致阻塞性通气障碍,但因患者多有呼吸加速,故肺泡总通气量可无明显减少,但其分布则不均匀。②肺泡膜增厚引起弥散障碍。③肺小动脉内微血栓或脂肪栓塞,使部分肺泡血流不足,形成死腔样通气。另一方面,因肺顺应性降低、肺不胀、肺泡内充满水肿液或气道受阻等原因,使部分肺泡通气减少而血流未相应减少,故可造成大量肺内短路或功能性分流增加,这些因素均导致肺泡的通气与血流比例失调。
第三节 呼吸衰竭时机体的主要机能代谢变化
外呼吸功能障碍引起的直接效应是血液气体的变化,即PaO2降低或同时伴有PaCO2增高或降低。呼吸衰竭时机体各系统的机能变化的最重要的原因就是低氧血症,高碳酸血症和酸碱平衡紊乱。低氧血症和高碳酸血症对机体的影响取决于其发生的急缓、程度、持续的时间以及机体原有的机能代谢状况等。在发病过程中,尤其是在病程迁延的慢性呼吸衰竭病人,常出现一系列代偿适应反应,可改善组织的供氧,并调节酸碱平衡,或改变组织器官的机能代谢以适应新的环境。严重时,呼吸系统以外的器官也可发生功能紊乱,甚至成为死亡的直接原因。
一、气体代谢变化
呼吸衰竭时必定有血液气体的变化,有时因原发疾病的掩盖,呼吸衰竭本身引起的临床表现可不明显,但根据血液气体的变化可判断是否发生了呼吸衰竭。由于病变部位、性质与程度以及机体反应性和代偿功能的不同,呼吸衰竭时的血液气体变化也可不全相同,大致有下列四种类型:
(一)PaO[XB]2[/XB]下降PaCO[XB]2[/XB]上升,二者成一定比例关系
各种原因只要引起总肺泡通气量不足,就会使肺泡气氧分压(PAo2)下降和肺泡气二者氧化碳分压(PAco2))增高,流经肺泡毛细血管的血液不能充分动脉化,因而必然导致(Pao2)降低和PAco2增高。PAco2取决于每分肺泡通气量(VA)与体内每分钟产生的二氧化碳量(Vco2),可以下式表示之,PAco2=0.86×Vco2/VA。如Vco2不变,只要通气减少,PAco2必增,而肺泡毛细血管末端血液的二氧化碳分压几乎和PAco2相等,故Paco2增高是全肺通气不足的特征。根据肺泡气体公式(Pao2=Pio2-PAco2/R,如吸入气氧分压(Pio2)为150mmHg,当通气减少一半时,PAco2即由正常的5.33kPa(40mmHg)增至10.7kPa(80mmHg)。在R(即RQ,呼吸商)为0.8时,PAo2就由15.3kPa(100mmHg)降至6.67kPa(50mmHg)。这种变化反映在动脉血液气体分压也有相似的变化,即Pao2下降和Paco2上升,二者呈一定比例地加重(图13-4A)。通常见于呼吸中枢抑制与中央气道狭窄阻塞等所引起的通气不足时。
(二)PaO[XB]2[/XB]下降而Paco[XB]2[/XB]变动不大
这种血液气体的变化可见于下列情况:
1.肺泡通气血流比例失调肺功能分流增加时,流经此处的静脉血不能充分动脉化,因此氧分压降低二氧化碳分压增高。由于Paco2升高剌激中枢化学感受器以及PaO2降低剌激主动脉体,颈动脉体化学感受器,故呼吸快速,每分通气量增加,代偿性过度通气的肺泡的PAo2增高而PAco2降低,血液流经这些肺泡,其氧分压也会有所增高,二氧化碳分压也必然降低。混合的肺静脉血最终往往是氧分压低于正常,而二氧化碳分压正常或略有降低。死腔样通气增多时,病变区域的血液固然可以充分氧合,但浪费了通气,其余肺泡就会相对通气不足,因而也出现功能分流增加,其血液气体变化也是PaO2降低而PaCO2变动较小(图13-4C)。
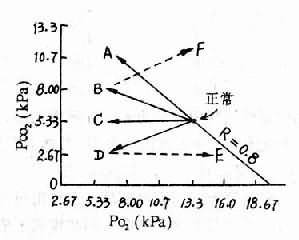
图13-4 呼吸衰竭时不同类型的血气变化A. PaO2↓PaCO2↑,二者变动值呈一定比例B. PaO2↓PaCO2↑,二者变动值不呈一定比例C.PaO2↓PaCO2,不变E. D用氧后D.PaO2↓PaCO2明显降低 F. B用氧后
部分肺泡通气血流比例失调时,往往只引起低氧血症而无高碳酸血症,主要是由血液二氧化碳解离曲线和氧离曲线的特性所决定。在PaCO2相当于5.00-8.00kPa(40-60mmHg)时,血液二氧化碳分压改变与二氧化碳的含量改变几乎呈直线关系(图13-5),在代偿性过度通气的肺泡,只要PAco2降低,血液中二氧化碳就可得到更多的排除,因此可以代偿那些通气不足的肺泡所造成的二氧化碳潴留。而氧离曲线的特点则与此不同。当氧分压为13.3kPa(100mmHg)时,血氧饱和度已达95~98%,过度通气的肺泡即使提高了氧分压,流经的血液氧饱和度和氧含量的增加也是极微少的,因此不能代偿通气不足的肺泡所造成的低氧血症(图13-6)。
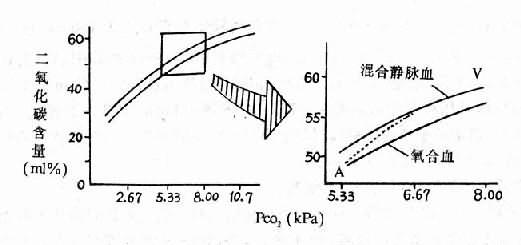
图13-5 血液二氧化碳解离曲线图中kPa相当于mmHg的数值kPa mmHg
| 2.67 |
20 |
| 5.33 |
40 |
| 8.00 |
60 |
| 10.7 |
80 |
| 13.3 |
100 |
| 16.0 |
120 |
| 18.67 |
140 |
肺顺应性降低引起的限制性通气障碍的患者,呼吸常加快,总通气量可增加。同时因其病变常不是均匀一致的,还有肺泡通气血流比例失调,故体内二氧化碳可化偿性地排出增多,其血液气体变化亦常为Pao2下降,而Paco2不变或略低。
功能性分流增加和死腔样通气增多引起的缺氧,都可用吸入高浓度氧治疗得到缓解。肺内短路也可引起类似功能分流的血气变化,唯吸入高浓度氧不能改变缺氧。
2.弥散障碍肺泡膜面积减少、厚度增加或通透性降低时,除因同时存在的肺泡通气血流比例失调可引起低氧血症外,严重时本身也可因氧从肺泡弥散到血液的过程受阻而使PaO2下降。但因二氧化碳的弥散能力很强(约比氧大20倍)其排出受影响较小,故PaCO2多正常,甚至因为代偿性通气过度而有所下降。这类病人吸入高浓度氧也可解除低氧血压。
弥散障碍与肺泡通气血流比例失调都使换气不能有效地进行,因此Pao2低于PAo2,PAo2和Pao2的差值增大是它们的共同特征。
(三)PaO[XB]2[/XB]下降,Paco[XB]2[/XB]升高,二者变化不成一定比例关系
这种血液气体变化可见于下列情况:
1.胸廓顺应性降低引起的限制性通气不足 由于胸廓的病变常不对称均匀,故此时呼吸衰竭的发病机制,不仅是肺泡通气不足,还有肺泡通气血流比例失调。此时,胸廓的的病变又限制了通气反应,使之不能充分加强,二氧化碳虽可代偿性排出一部分,但又排出不足,故血液气体变化为Pao2降低,PaCO2上升,但二者的变化不是一致的比例关系,其中以Pao2下降程度较为严重(图13-4B)。
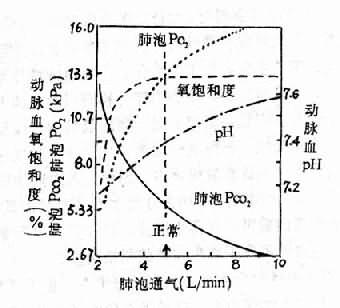
图13-6 肺泡通气与肺泡PO2、肺泡Pco2、
动脉血氧饱和度和动脉血pH的关系
2.慢性阻塞性肺疾患由于此时外周小气道阻塞等病变也不均匀一致,故肺泡通气血流比例明显失调。这是导致血液气体异常的重要机制。血液气体变化除可表现为Pao2降低Paco2不变外,在有些患者可能因中枢神经系统反应性不同而使增强通气的反应有所减弱,故不仅有Pao2降低,而且早期就有Paco2升高,只是Paco2变动程度小于Pao2变动的程度,二者不呈固定的比例关系。这些慢性呼吸衰竭患者因肺泡通气血流比例失调而CO2增强呼吸的作用又减弱,故Paco2升高,直到每分钟产生的CO2全由通气良好的肺泡排出,则又可使二氧化碳的生成和排出在高Paco2水平上达到新的平衡,因此Paco2可较长期维持于较高水平,患者尚能继续生存。
(四)Pao[XB]2[/XB]下降,Paco[XB]2[/XB]也明显下降
在肺泡通气血流比例失调引起呼吸衰竭的患者中,有些在Pao2下降的同时Paco2也明显降低(图13-4D)。这种情况可见于成人呼吸窘迫综合征和肺广泛纤维性变等。血液气体的这种变化,可能是由于此时肺间质中感受器受到强烈刺激而反射性引起通气极度加强所致,故即使纠正缺氧,通气过度仍可持续存在。
二、酸碱平衡及电解质紊乱
呼吸衰竭时,不仅因外呼吸障碍可引起酸碱平衡紊乱,而且还可因并发肾功能障碍、感染、休克以及某些治疗措施不当等因素而出现不同类型的酸碱平衡紊乱。因此患者的表现可能是多样的。由于外呼吸功能严重障碍本身引起的有呼吸性酸中毒、呼吸性碱中毒、代谢性酸中毒或呼吸性酸中毒合并代谢性酸中毒。
(一)呼吸性酸中毒 Ⅱ型呼吸衰竭时,大量二氧化碳潴留,可造成原发性血浆碳酸过多。发病急骤者,往往代偿不全而出现失代偿性呼吸性酸中毒,如发病较缓慢,则可出现代偿性呼吸性酸中毒。此时血液电解质主要有如下的变化。①血清钾浓度增高:急性呼吸性酸中毒时,主要是由于细胞内外离子分布改变,细胞内钾外移而引起血清钾浓度增高;慢性呼吸性酸中毒时,则是由于肾小管上皮细胞泌氢和重吸收碳酸氢钠增多而排钾减少,故也可导致血清钾浓度增高。②血清氯浓度降低,碳酸氢根增多;当血液中二氧化碳潴留时,在碳酸酐酶及缓冲系统作用下,红细胞中生成碳酸氢根增多,因而进入血浆的碳酸氢根也增多,同时发生氯转移,血浆中氯离子进入红细胞增多,因此血清氯离子减少而碳酸氢根增加。另一方面,由于肾小管泌氢增加,碳酸氢钠重吸收和再生增多,而较多氯离子则以氯化钠和氯化铵的形式随尿排出,因而也可引起血清氯离子减少和碳酸氢根增多。
(二)代谢性酸中毒或呼吸性酸中毒合并代谢性酸中毒 由于严重缺氧,无氧代谢加强,酸性代谢产物增多,可引起代谢性酸中毒,或呼吸性酸中毒合并代谢性酸中毒。如患者合并肾功能不全或感染、休克等、则因肾脏排酸保碱功能障碍或体内固定酸产生增多,将更加重代谢性酸中毒。此时血清钾浓度增高可更明显。
(三)呼吸性碱中毒 Paco2明显下降的患者,可因原发性碳酸过低而发生呼吸性碱中毒,由于发病急骤,故多为失代偿性呼吸性碱中毒。此时因细胞外钾离子进入细胞内,可发生血清钾浓度降低。由于二氧化碳排出过多,血浆中碳酸氢根移入红细胞增多,氯离子则转移至红细胞外,加之肾排出氯也减少,故血清氯浓度增高。血浆碳酸氢根则因移入红细胞以及肾小管重吸收和再生碳酸氢钠减少而浓度降低。
此外,某些呼吸衰竭患者可以发生代谢性碱中毒,多属医源性,发生于治疗过程中或治疗后。如使用人工呼吸机,过快排出大量二氧化碳,而原来代偿性增加的碳酸氢根又不能迅速排出,因此发生代谢性碱中毒;由于钾摄入不足、应用排钾利尿剂和肾上腺皮质激素等可导致低钾症性碱中毒等。
三、呼吸系统变化
呼吸衰竭病人的呼吸功能变化,很多是由原发疾病引起的。如阻塞性通气障碍时,由于气流受阻,呼吸可减慢。随着阻塞部位的不同,以及阻塞是可变还是固定,呼气与吸气困难的程度亦可不一。在肺顺应性降低的疾病,则因牵张感受器或肺-毛细血管旁感受器(juxtapulmonary-capillary receptor,J感受器)兴奋而反射地引起呼吸浅快。中枢性呼吸衰竭可出现呼吸浅慢,或出现潮式呼吸、间歇呼吸、抽泣样呼吸、吸气样呼吸、下颌呼吸等呼吸节律紊乱。
外呼吸功能障碍造成的低氧或高碳酸血症可进一步影响呼吸功能。Pao2降低作用于颈动脉体与主动脉体化学感受器(其中主要是颈动脉体化学感受器),反射性增加通气,但此反应要Pao2低于8.0kPa(60mmHg)时才明显。二氧化碳潴留主要作用于中枢化学感受器,使呼吸中枢兴奋,从而引起呼吸加深加快,增加肺泡通气量。但Pao2低于4.0kPa(30mmHg)时或Paco2超过12.0kPa(90mmHg)时,将损害或抑制呼吸中枢。
在慢性Ⅱ型呼吸衰竭病人,随着低氧血症和高碳酸血症发展的逐渐严重,其呼吸调节也将发生变化:此类病人的中枢化学感受器常被抑制而对二氧化碳的敏感性降低,此时引起通气的冲动大部来自缺氧对外周化学感受器的剌激。如果给予高浓度的氧吸入,则虽可缓解低氧血症,但却因此解除了缺氧反射性兴奋呼吸中枢的作用,故易招致呼吸进一步的抑制,使通气更减弱而二氧化碳的潴留更加重。此外,吸入高浓度氧使血氧饱和度回升后,由于霍尔登(Haldane)效应使二氧化碳解离曲线向右下移动(图13-5),也可引起Paco2进一步增高。
四、中枢神经系统变化
呼吸衰竭时,由于低氧血症与高碳酸血症的作用,中枢神经系统的功能可发生明显变化,轻度时可使兴奋性升高,严重时将发生一系列中枢神经系统的功能障碍,直接威胁生命。低氧血症和高碳酸血症的作用很难截然分开。
中枢神经对缺氧很敏感,故最易受损。Pao2为8.0kPa(60mmHg)时可出现智力和视力轻度减退。如Pao2迅速降至5.33~6.66kPa(40~50mmHg)以下时,就会引起一系列神经精神症状,如头痛、不安、定向与记忆障碍、精神错乱、嗜睡,以致惊厥和昏迷,Pao2低于2.67kPa(20mmHg)时,只需几分钟就可造成神经细胞的不可逆性损害。
二氧化碳潴留发生迅速而严重时,也能引起严重的中枢神经系统功能障碍,称为二氧化碳麻醉。一般认为,当Paco2超过10.7kPa(80mmHg)时,可引起头痛,头晕、烦躁不安、言语不清、扑翼样震颤、精神错乱、嗜睡、昏迷、抽搐等。其可能的作用机制如下:
(一)二氧化碳直接作用于脑血管,使之扩张。一般认为Paco2升高1.33kPa(10mmHg),脑血流量约可增50%;由此可以影响脑循环,并引起毛细血管通透性增高,其结果是脑血管充血、间质水肿、颅内压升高和视神经乳头水肿。严重时还可导致脑疝形成。
(二)正常脑脊液的缓冲作用较血液为弱,其pH也较低(7.33~7.40),而Pco2却比动脉血的高,血液中的碳酸氢离子及氢离子又不易进出脑脊液,故后者的酸碱调节需时较长。Ⅱ型呼吸衰竭病人的脑脊液中二氧化碳也增多,但因脑脊液缓冲能力差,故氢离子浓度增高的程度大于血液,继而又可加重细胞内酸中毒,使神经细胞的功能发生障碍,细胞膜结构受损,通透性增高。这些变化一方面改变神经细胞内外离子分布,另一方面使溶酶体膜稳定性降低,释出的各种水解酶,能促使蛋白分解与细胞死亡。细胞内外离子分布的改变和细胞内蛋白分解又可使细胞内渗透压升高,促使脑细胞肿胀,颅内压升高。
目前国内已普遍地将呼吸衰竭时由于中枢神经功能障碍而出现一系列神经精神症状的病理过程称为肺性脑病。
五、循环系统变化
一定程度的缺氧可反射性兴奋心血管运动中枢,从而使心率加快,心输出量增加,皮肤及腹腔内脏血管收缩,因而发生血液重分布和血压轻度升高。此外,缺氧时也可间接地因通气加强,胸腔负压增大,回心血量增加而影响循环功能。这种变化在急性呼吸衰竭时较为明显,且有代偿意义。严重低氧血症时,因循环中枢与心血管受损,可发生低血压,心收缩力降低,心律失常等后果。缺氧尤其是肺泡气氧分压降低可使肺小动脉收缩,这是呼吸衰竭时引起肺动脉高压与右心衰竭的主要原因。
一定程度的二氧化碳潴留可与缺氧协同作用,反射性地引起循环功能的代偿性变化。二氧化碳可反射性地引起外周血管收缩,但其直接作用,则除肺动脉外多为引起血管扩张,故二氧化碳潴留的最终效应通常为:①皮肤血管扩张,因而肢体皮肤温暖红润,常伴大量出汗;②睑结膜血管扩张充血;③脑血管扩张,脑血流量增加;④广泛的外周血管扩张,可引起低血压;⑤肾与肺小动脉收缩。
呼吸衰竭可伴发心力衰竭,尤其是右心衰竭,其发生原因为肺动脉高压和心肌受损。目前认为,不论是急性或慢性呼吸衰竭,肺血管功能性改变在肺动脉高压的发病中都具有极重要意义。缺氧(主要是肺泡气氧分压降低)可引起肺血管收缩,若合并二氧化碳潴留,血液氢离子浓度增高,就更可增加肺血管对缺氧的敏感性,使肺血管收缩进一步加重,从而大大增加肺循环的阻力。如原发肺部疾病引起肺小动脉壁增厚、管腔狭窄或纤维化、肺毛细血管网受压破坏与减少、毛细血管内皮细胞肿胀或微血栓阻塞等变化,则亦可增加肺循环阻力而导致肺动脉高压。有的慢性呼吸衰竭患者血液中的红细胞增多,因而血液粘滞性增高,而后者又可因合并酸中毒而加重,这也是肺动脉高压发病的一个因素。某些患者可因血量增多,或因呼吸深快以致胸腔负压增大,或因体循环外周血管扩张,阻力降低,以致静脉回流增加而加重右心负荷。呼吸衰竭引起右心衰竭的另一发病因素是心肌受损。缺氧,高碳酸血症、酸中毒和电解质代谢紊乱均可损害心肌。长期持续缺氧还可引起心肌变性、坏死、纤维化等病变。心肌受损加上负荷过重,就可导致右心衰竭。
六、肾功能变化
呼吸衰竭时肾功能也可遭到损害,轻者尿中出现蛋白、红细胞、白细胞及管型等。严重时可发生急性肾功能衰竭,出现少尿、氮质血症和代谢性酸中毒等变化。此时肾脏结构往往无明显变化,故常为功能性肾功能衰竭。只要外呼吸功能好转,肾功能就可较快恢复。肾功能衰竭的基本发病机制在于缺氧与高碳酸血症反射性引起肾血管收缩,从而使肾血流量严重减少。若患者并发心力衰竭、播散性血管内凝血或休克,则肾脏的血液循环障碍将更严重而肾功能障碍也将加重。
七、胃肠道变化
严重缺氧可使胃壁血管收缩,因而能降低胃粘膜的屏障作用。二氧化碳潴留可增强胃壁细胞碳酸酐酶活性,使胃酸分泌增多,而且有的患者还可合并播散性血管内凝血、休克等,故呼吸衰竭时可出现胃肠道粘膜糜烂、坏死、出血与溃疡形成等变化。
第四节 呼吸衰竭的防治原则
一、防治原发病
针对引起呼吸衰竭的原发疾病进行预防,或在发病后及时进行积极处理。
二、防止与去除诱因的作用
对于可能引起呼吸衰竭的疾病,还必须同时防止诱因的作用。例如对于创伤、休克患者,要避免吸入高浓度氧、输给久存血库的血液或输液过量等,以免诱发成人呼吸窘迫综合征。有呼吸系统疾病的患者必须作手术时,应先检查病人的肺功能储备力。对肺功能已有损害或慢性呼吸衰竭的病人更应积极防止及去除各种诱因的作用,以免诱发急性呼吸衰竭。
三、畅通气道和改善通气
常用的方法有:①清除气道内容物或分泌物;②解除支气管痉挛;③用抗炎治疗减轻气道的肿胀与分泌;④必要时作气管插管或气管切开术;⑤给以呼吸中枢兴奋剂;⑥掌握适应症,正确使用机械辅助通气。
四、改善缺氧
呼吸衰竭时必定有严重缺氧,因此纠正缺氧,提高Pao2水平对每个患者都是必要的。其目的在于短期内争取使Pao2升至6.67~8.0kPa(50~60mmHg),动脉血氧饱和度升至85%左右。
Ⅰ型呼吸衰竭有缺氧而无二氧化碳潴留,可吸入较高浓度的氧(一般不超过50%)。慢性Ⅱ型呼吸衰竭时,由于呼吸中枢反应性的变化,一般认为给氧原则上以持续低浓度低流量为宜。应使Pao2达到安全水平8.0~9.33kPa(60~70mmHg),以求能供给组织以必要的氧而不致引起二氧化碳麻醉,然后根据病人情况调整并逐渐提高吸入氧的浓度及流量。如在给氧时出现二氧化碳分压进行性上升,则须助以人工通气以促进二氧化碳的排出。
五、密切观察监护,综合治疗
注意纠正酸碱平衡紊乱与水电解质紊乱;维持心、脑、肾等重要器官的功能;防治常见的严重并发症。
[附]:成人呼吸窘迫综合征
成人呼吸窘迫综合征(adultrespiratory distress syndrome, ARDS)是指在某些疾病过程中(例如创伤、烧伤、感染等)。特别是在休克初期复苏后,突然出现以进行性缺氧和呼吸困难为特征的急性呼吸衰竭综合征。此时即使吸入高浓度氧,也难于纠正低氧血症。Ashbaugh于1967年首先报导了这种综合征。由于其临床过程与新生儿呼吸窘迫综合征类似,故命名为成人呼吸窘迫综合症。
一、其临床主要表现及诊断依据为:
1.败血症、休克、创伤或误吸等患者突然发生进行性呼吸困难,呼吸频率在20次/分以上。
2.顽固性低氧血症 Pao2<8kPa(<60mmHg),吸纯氧15分钟后Pao2仍低于46.7kPa(350mmHg)[正常人吸纯氧可使Pao2高达73.3kPa(550mmHg)]、动脉血二氧化碳分压也降低,Pao2<4.7kPa(<35mmHg)。晚期Paco2也可高于正常。
3.胸廓肺顺应性降低 低于50ml/98Pa,正常约为100ml/98Pa。
4.胸部X光检查 可见肺纹理增加,发展为斑片状阴影,甚至弥漫性呈毛玻璃样。
5.必须排除由慢性肺部疾病及左心疾病引起肺水肿,肺动脉楔压小于Pao2为1.76kPa(18cmH2O)。
成人呼吸窘迫综合症发病率高,病死率也很高,大多数病人在发病后二周内死亡。
二、成人呼吸窘迫综合征的原因
ARDS是由许多原因引起的急性肺泡-毛细血管膜损伤。有些原因可直接损伤肺:如①吸入烟雾、毒气、胃内容物及溺水;②服用过量海洛因或水杨酸盐;③细菌、病毒及真菌等所致肺部感染;④脂肪、羊水及血栓等引起肺栓塞;以及⑤肺挫伤、放射线损伤与氧中毒等。有些全身性病理过程可引起肺损伤,如败血症、休克、弥散性血管内凝血、过敏反应、创伤及烧伤等。烧伤面积超过40%就可能导致Pao2明显降低。有些治疗措施也可能引起ARDS,如血液透析、体外循环、用尼龙丝去除白细胞等。根据病因的不同及病变特点,ARDS曾有20多个名称,如创伤后湿肺、败血症肺、休克肺、输血后肺、微血管漏出综合征,充血性肺不张、透明膜病、出现性肺综合征、僵肺综合症、进行性肺实变等。 二、成人呼吸窘迫综合征的病理变化各种原因所致急性肺泡-毛细血管膜损害伤的病理变化均类似,可分为急性阶段与慢性阶段病变:
(一)急性阶段病变
主要为广泛肺泡血管内皮和肺泡上皮损伤所致肺水肿,首先是肺间质水肿,后出现肺泡水肿,肺重可达正常值之三倍。肺泡腔内液体蛋白质含量高,甚而是血性液体,并有血细胞、巨噬细胞、细胞碎片、无定形物质、纤维蛋白条和表面活性物质的残存物,偶而可见细胞碎片和蛋白等物质在纤维蛋白网眼中形成透明膜。
(二)慢性阶段病变
发病数天后进入慢性阶段,病变以细胞增生为主,两周后即可出现纤维化。Ⅱ型上皮细胞增生取代了变性坏死的Ⅰ型肺泡上皮细胞,加上各种细胞的浸润使肺泡间隔增厚,肺泡腔与肺泡管内富含蛋白质的的液体机化而形成纤维化。
三、成人呼吸窘迫综合征的发病机制
ARDS的病变主要是肺泡-毛细血管膜损伤引起肺水肿和继后的细胞增生和纤维化。细胞增生反应和纤维化的机制和炎症修复过程相同。故此处着重讨论急性肺损伤的机制。ARDS病人均有肺动脉高压,故有人强调肺微血管内高压为肺水肿的原因。但病人肺动脉楔压往往并不高,说明毛细血管压并不一定高。水肿液蛋白质含量丰富,动物实验也证明,类似ARDS的动物模型肺淋巴液流量增大,肺淋巴液中蛋白质浓度与血浆蛋白质浓度之比值大于0.7;此时,静脉注入的高分子右旋糖酐(分子量500,000)可透入肺泡液,均说明ARDS时的肺水肿主要是渗透性肺水肿,由于肺泡-毛细血管膜损伤使其通透性增高所致。ARDS中肺泡毛细血管膜通透性增高的机制并未完全阐明。有些原始病因能直接损伤肺泡毛细血管膜使其通透性增高,如吸入胃酸、毒气,烟熏、放射性损伤及细胞毒素作用等。大量实验表明,更主要的是继发性损伤,即通过白细胞和血小板在肺内聚集引起肺泡-血管膜损伤使其通透性增高。
(一)中性粒细胞在ARDS发病中的作用
ARDS病人外周血液中中性粒细胞数减少。肺活检可见肺内有中性粒细胞聚集和浸润。支气管肺泡洗出液中中性粒细胞可增加20~100倍。现在一般认为中性粒细胞在肺中聚集、激活、释放氧自由基、蛋白酶和脂质代谢产物,从而导致肺微血管膜及肺泡上皮的损伤,是ARDS肺水肿的主要发病机制。
1.中性粒细胞在肺血管中聚集 正常人在直立体位时约有10~20%的中性粒细胞聚集在肺毛细血管床中,这是一种物理性扣留。由于一个肺泡有近千节(segment)毛细血管,每节毛细血管长1~30μm(平均8μm),直径1~15μm(平均5μm),一个血细胞从肺动脉流入肺静脉要经过100个以上的毛细血管节,中性粒细胞直径大于毛细血管口径,其形状与红细胞相比更接近球形,故变形能力较差,变形速度较慢,所以中性粒细胞易被扣留在肺毛细血管床中。由于肺毛细血管床容量较大,白细胞的扣留对肺血管的阻力和肺动脉压的影响不大。物理性扣留的中性粒细胞一般不进入肺泡腔,故正常人支气管肺泡洗出液中的细胞90~95%是巨噬细胞。
ARDS时中性粒细胞在肺血管中的聚集是化学性粘附(adhesion),是由于趋化因子作用的结果。实验证明,中性粒细胞经趋化因子激活后与血管内皮细胞之间的亲和力显著增强。肺泡毛细血管总面积达60m2,可粘附大量中性粒细胞,以至使外周血液中白细胞数减少。
趋化因子种类很多,主要有补体激活产物C5a、纤维蛋白降解产物(FDP),花生四烯酸代谢产物如白三烯B4(LTB4)、羟花生四烯酸(HETE)和血栓素A2(AXA2),血小板活化因子(PAF),以及其他具趋化作用的蛋白质、多肽和脂质。其中研究较多的是补体的作用。在临床确诊ARDS前8小时血浆C5a往往已升高。激活的补体本身并不直接损伤肺血管内皮细胞,它是通过激活中性粒细胞起损伤作用。给出羊灌注激活的补体可导致肺水肿,如先用氮芥使粒细胞减少后再灌注激活之补体,则肺水肿的发生明显较经。激活的中性粒细胞可浸润入肺间质和进入肺泡腔。ARDS病人支气管肺泡洗出液中存在补体碎片及大量中性粒细胞。近年来发现中性粒细胞表面有一组糖蛋白,后者与粒细胞的的粘附和吞噬功能有关,它们是巨噬细胞分子-1(macrophage-1,Mac-1)淋巴细胞功能相关抗原-1(lymphocyte function associatedantegen-1,LFA-1),其中Mac-1与粘附功能关系最密切。正常中性粒细胞表面仅有少量Mac-1表达,在病理情况下,趋化因子的作用使中性粒细胞表面Mac-1表达量增加,促进中性粒细胞与血管内皮细胞间的粘附。
2.中性粒细胞对肺泡-毛细血管膜的损伤动物实验中静脉注入内毒素、空气等可复制急性肺微血管损伤的模型,用佛波豆蔻醚乙酸盐(phorbol myristate acetate,PMA)激活的中性粒细胞灌注离体肺也可使肺毛细血管通透性增高。如先用羟基脲、氮芥等使动物中性粒细胞数减少,则内毒素、空气栓子等对肺微血管的损伤明显减轻。细胞培养中发现,中性粒细胞秘须紧密粘附于内皮细胞才能使单层肺动脉内皮的通透性增高。以上说明减轻。细胞培养中发现,中性粒细胞必须紧密粘附于内皮细胞才能使单层肺动脉内皮的通透性增高。以上说明,中性粒细胞的粘附与激活在ARDS发病中具有重要作用,很可能是中性粒细胞激活时释放的氧自由基、蛋白酶、脂质代谢产物和肽类物质等造成肺泡-毛细血管膜的损伤。
(1)氧自由基的作用:中性粒细胞被激活时,耗氧量急剧上升,比静息时增加数倍至数十倍。此时细胞膜上的NADPH氧化酶(NADPhoxidase)被激活,将还原型辅酶Ⅱ(NADPH)转变为氧化型(NADP),氧分子则获得电子形成超氧阴离子O2-,由O2-又可生成H2O2和OH·。将正常中性粒细胞和其激活剂PMA一起灌注离体肺可引起肺水肿,水肿液蛋白质含量高;如将遗传性慢性肉芽肿病患者的中性粒细胞与PMA灌注则不引起肺水肿,因为慢性肉芽肿病患者的中性粒细胞缺乏NADPH氧化酶、氧自由基的生成少。另外,静脉内注射氧自由基清除剂,如超氧化物歧化酶(SOD)、过氧化氢酶、过氧化物酶、二甲本硫脲等,可减轻实验动物的急性肺损伤。可见,中性粒细胞激活时通过释放氧自由基引起肺损伤。
氧自由基损伤肺微血管内皮及肺泡上皮细胞的作用可能有以下几个方面:①作用于细胞膜和细胞器膜,使其脂质过氧化,从而损害细胞膜和细胞膜的结构和功能;②作用于酶,使之失活;③作用于α1—蛋白酶抑制物,使之失活,从而增强溶酶体释放的蛋白酶对组织的破坏作用;④作用于血浆成份,可形成一种很强的趋化物,引起更多的中性粒细胞在肺内聚集与激活,产生更多的氧自由基,由此形成阳性反馈,加重肺的损伤。
(2)蛋白酶的作用:中性粒细胞中溶酶体含有多种中性蛋白酶和酸性蛋白酶。当中性粒细胞被激活或破坏时,释出的这些酶可引起周围蛋白质的分解和组织结构的破坏,使肺泡-毛细血管膜的通透性增高。其中研究较多的是中性粒细胞弹性蛋白酶。例如实验中发现,ARDS病人支气管肺泡洗出液中弹性蛋白酶活性很高,给动物注射内毒素或油酸复制ARDS模型时,其血浆及肺泡洗出液中弹性蛋白酶含量也增多;给动物注射中性粒细胞弹性蛋白酶可引起肺血管内皮及肺泡上皮的通透性增高;组织培养中加入弹性蛋白酶导致内皮细胞分散等,说明中性粒细胞弹性蛋白酶与ARDS中的肺损伤有关。弹性蛋白酶可降解弹性蛋白、胶原蛋白、纤维连接蛋白(fibronectin,FN)等。纤维连接蛋白在内皮细胞之间和内皮细胞与基底膜之间起“锚连”作用。纤维连接蛋白受损,则血管通透性增高。
肝脏和肺泡巨噬细胞能合成α1-蛋白酶抑制物(α1-protease inhibitor,α1-PI),后者能抑制弹性蛋白酶。虽然ARDS病人血浆α1-PI可正常,支气管肺泡洗出液中α1-PI活性却降低,可能由于中性粒细胞产生的自由基使其氧化灭活所致。蛋白酶与蛋白酶抑制物间的失衡更加重了蛋白酶对组织的损伤,使肺泡-毛细血管膜通透性增高。
3.脂类代谢产物的作用内毒素等许多致病因素激活中性粒细胞、巨噬细胞、肥大细胞、内皮细胞等细胞膜上的磷脂酶A2,使膜磷脂裂解为花生四烯酸,后者通过环加氧酶途生成前列腺素,通过脂加氧酶途径生成白三烯。一般认为白三烯,TXA2、和PGF2α既可收缩肺小动脉引起肺动脉高压,也能增加肺微血管的通透性;而PGI2和PGE1则有扩张血管、降低血压,和使血管通透性降低的作用。急性肺损伤的动物及病人肺泡洗出液及血液中TXA2、PGF2α和LTs均增多。有实验证明PGI2和PGE1对急性肺损伤有一定的治疗作用。白细胞、巨噬细胞、肥大细胞和内皮细胞等激活后还可释放血小板活化因子(PAF)。PAF可促使血小板聚集和TXA2合成,从而导致微血管通透性增高。
4.蛋白类物质的作用巨噬细胞等激活后尚可释放蛋白类物质,其中较重要的有肿瘤坏死因子(TNF)及白细胞介素ⅠIL-1)。人及动物在内毒素血症时血浆中TNF和IL-1增多。TNF能使肺血管通透性增高,并促使中性粒细胞在肺中聚集;IL-1剌激T淋巴细胞产生白细胞介素2(IL-2),后者也可使肺血管通透性增高。
总之,现在一般认为,中性粒细胞巨噬细胞在肺内聚集、激活释出大量氧自由基和蛋白酶及脂类代谢产物和蛋白类,引起肺泡-毛细血管膜的损伤和通透性增高,导致肺水肿,这是ARDS的主要发病机制。虽然有报导白细胞减少的病人患败血症时也可发生急性肺损伤,用药物使动物中性粒细胞减少对注油酸引起肺损伤并无明显影响,但这些事实并不足以否定中性粒细胞的致病作用,因为外周血液中的中性粒细胞数不一定能反映肺循环中的粒细胞数。而且究竟需要多少中性粒细胞激活就足以引起急性肺损伤尚不了解,也可能正常聚集在肺血管中的中性粒细胞只有一部分被激活就足以损伤肺而导致ARDS。
(二)凝血系统在ARDS发病中的作用
ARDS病人肺活检及死后尸解发现,肺小动脉血栓可发生于肺充血、水肿、出血及透明膜的形成之前。ARDS病人合并有弥散性血管内凝血者,其低氧血症和肺顺应性降工远较未合并DIC者为重,中性粒细胞激活和肺组织损伤所释放的促凝物质,肺血管内皮损伤和血液停滞,可导致血小板聚集和血管内凝血形成微血栓。肺内广泛微血栓形成可能引起:①肺循环阻力增加使肺动脉压升高,未堵塞的肺血管则血液量增大和毛细血管压升高,导致压力性肺水肿;②血栓损伤血管壁和血小板释放的血管活性物质以纤维蛋白降解产物,可使血管通透性增高致渗透性肺水肿;③血小板的消耗、纤维蛋白降解产物的抗凝作用、和血管壁的损伤可引起肺内出血;④血小板释放的5-HT等介质使支气管收缩,影响肺通气。近年特别引人注目的是纤维蛋白降解产物(FDP)的作用,发现严重创伤烧伤或感染病人中,已合并ARDS者血中FDP水平比未发生ARDS者高得多,而且ARDS病情与FDP浓度有一定平行关系。将纤维蛋白碎片D(FD)注入家兔血管,可引起进行性外周血液血小板减少、肺间质内白细胞浸润,肺血管通透性增高和肺功能不全;如注入血浆白蛋白、纤维蛋白及纤维蛋白碎片E,则不出现以上病变。很可能小板上有FD特异的膜受体,后者与FD结合可激活血小板,引起血小板聚集和释放反应。另外,FD也是趋化物,能促使中性粒细胞在肺内聚集、粘附和激活,由此加重肺的损害。
正常肺毛细血管内皮的通透性比肺泡上皮高10倍。ARDS中肺毛细血管通透性的变化早于肺泡上皮,故先发生肺间质水肿,后出现肺泡水肿。肺泡上皮的损伤使Ⅱ型上皮细胞生成的表面活性物质减少,可导致肺不张,形成功能性分流。
在全身性病理过程如败血症、休克等,中性粒细胞粘附于血管内皮以及血管内凝血引起的组织损伤,不仅发生于肺内,也可发生于肝、肾、肠、心、内分泌器官等处,故不能把ARDS看成仅仅是肺的损伤。但肺的血流量最大,毛细血管床面积也最大,故肺受累最重,使病人主要表现为急性呼吸衰竭.
四、成人呼吸窘迫综合征时肺呼吸功能变化
ARDS所致外呼吸功能障碍以肺泡通气-血流比例失调为主,加上弥散功能障碍,表现为低氧血症性呼吸衰竭。极严重病例有总的肺泡通气量减少时可出现高碳酸血症性呼吸衰竭。
(一)肺泡通气-血流比例失调
由于Ⅱ型肺泡上皮细胞受损致表面活性物质的生成减少,肺泡水肿使表面活性物质被稀释和破坏,和肺泡过度通气引起的表面活性物质消耗,以致肺泡表面张力升高,肺顺应性降低,导致肺不张,由此形成功能性分流和真性分流。中性粒细胞等释出的白三烯等介质使支气管收缩,和水肿液堵塞小气道,气可造成肺通气障碍而形成功能性分流。ARDS病人分流量可达肺血流量的30%。肺血管内微血栓形成、血管活性物质引起不均匀的肺血管收缩、以及肺间质水肿对血管的压迫,不仅可增加肺血管阻力使肺动脉压升高。尚可增加死腔样通气。因此,肺泡通气-血流比例失调是病人发生呼吸衰竭最主要的原因。
(二)弥散功能障碍
肺间质和肺泡水肿、透明膜的形成和慢性阶段细胞的增生及肺纤维化,均可增加弥散膜的厚度,导致弥散功能障碍。
(三)肺泡通气量减少
ARDS时肺部病变的分布是不均的。肺顺应性降低引起的限制性通气障碍和小气道阻塞引起的阻塞性通气障碍,造成部分肺泡通气量减少,未受累或病变较轻的肺泡反而代偿性通气增强,排出过多的二氧化碳,故病人Paco2反而降低。当肺泡-毛细血管膜损伤更广泛更严重时,全肺总的肺泡通气量将减少,CO2将潴留而发生高碳酸血症,此时Pao2将进一步下降。
肺通气障碍、Pao2降低对血管化学感受器的剌激、肺充血和肺水肿对J感觉器的剌激,导致病人呼吸窘迫。[J感受器(juxtapulmonary capillaryreceptor)位于肺泡毛细血管旁,能感受毛细血管压力剌激,肺充血、肺水肿受剌激反射性地引起呼吸加快。
五、成人呼吸窘迫综合征的防治原则
(一)治疗原发疾病
消除ARDS的原因,如抗感染、抗休克治疗等。
(二)吸氧与呼气末正压呼吸
ARDS病人发生低氧血症的主要机制是肺内功能性分流,所以吸氧疗法对提高其Pao2的作用较小。吸呼高浓度氧可提高Pao2,但吸入氧浓度在60%以上2~3天就可能引起氧中毒,反而加重ARDS。呼气末正压(positiveend expiratory pressure, PEEP)呼吸使呼气末时气道及肺泡压大于大气压,可将原来萎陷的气道和肺泡张开,恢复其气体交换功能,从而减少肺内分流,提高Pao2用PEEP呼吸尚可降低吸入气的氧浓度。但呼气末压力过高会压迫肺血管和心脏,使心输出量减少,导致循环性缺氧。
(三)维持液体平衡,控制肺水肿
如适当限制入水量、利尿等。
(四)用药物减轻肺泡-毛细血管膜的损伤和降低膜通透性
针对肺泡-毛细血管膜损伤的机制,采用相应的药物进行发病学治疗,有的已取得一定疗效,有的还处于实验阶段。曾试用的药物有:抗氧化剂(如超氧化物歧化酶)、蛋白酶抑制剂、磷脂酶A2抑制剂(如阿的平)、TXA2合成酶抑制剂(如咪唑)、脂加氧酶抑制剂(如U-60,257)、肝素和右旋糖酐、C5a及TNF的抗体、钙通道阻滞剂(如戊脉安)、其他扩血管药(如腺苷)、PGE和PGI2、以及肾上腺皮质激素等。